30. 利用工业废气 CO
2或 CO 和 H
2在一定条件下可制备燃料甲醇。
Ⅰ.利用工业废气 CO 合成甲醇,其能量变化示意图如下:
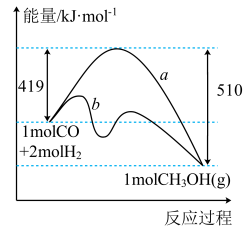
(1)图中曲线 a 到曲线 b 的措施是
_______。该反应 ΔS
________0(填“>”或“<”)
(2)一定条件下,在 2 L 密闭容器中充入 1 mol CO 和 2 mol H
2,10 min 后达到平衡,放出热量 45.5kJ,则 10 min 内 H
2的转化率为
_____;该温度下反应的平衡常数
K=
_____;达到平衡后,再向容器中充入 CO、H
2、CH
3OH 各 1 mol,则此时 υ
正_____υ
逆 (填“>”“<”或“=”)
(3)下列措施可以提高甲醇产率的是
_____。
a.压缩容器体积
b.将 CH
3OH (g)从体系中分离
c.恒容条件下充入He,使体系总压强增大
d.恒压条件下再充入 10mol CO 和 20mol H
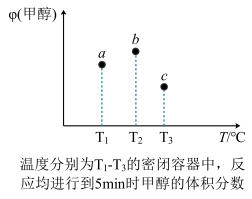
2(4)现有容积均为 1L 的 a、b、c 三个密闭容器,向其中分别充入 1molCO 和 2molH
2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b 中甲醇体积分数大于 a 中的原因是
_______达到平衡时,a、b、c 中 CO 的转化率大小关系为
_______。
Ⅱ.用工业废气中的 CO
2制取甲醇和水蒸气
(5)一定条件下,往2L恒容密闭容器中充入1mol CO
2和3mol H
2,在不同催化剂作用下发生反应 I、反应II与反应III,相同时间内CO
2的转化率随温度变化如图所示:

①催化剂效果最佳的反应是
_____(填“反应 I”,“反应 II”,“反应 III”)。
②b 点υ
正_____υ
逆(填 “>”, “<”, “=”)。
③若此反应在 a 点时已达平衡状态,a 点的转化率比 c 点高的原因是
_____。
④c点时该反应的平衡常数
K=
_____。