30. KI可用于分析试剂、感光材料、制药和食品添加剂等。制备原理如下:
反应①3I
2+6KOH=KIO
3+5KI+3H
2O;反应②3H
2S+KIO
3=3S↓+KI+3H
2O。该实验的主要步骤如下:
步骤a:关闭活塞K
1,打开K
3,碘单质充分反应后,关闭K
3。
步骤b:打开K
1,通入足量硫化氢气体,然后再关闭K
1。
步骤c:打开K
2,加入硫酸同时加热,关闭K
2。
步骤d:将反应液转移到烧杯中,加入碳酸钡,充分反应后过滤、洗涤。
步骤e:合并滤液和洗涤液,处理后得到产品。
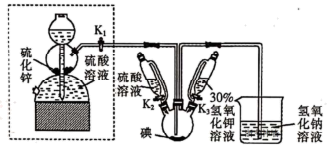
按照下列实验过程,请回答有关问题。
(1)步骤a中,当观察到
______(填现象)时才能关闭K
3。
(2)实验过程中,下列说法错误的是
______________。
A.虚线框中的仪器为启普发生器,还可以用来制备SO
2B.步骤b中,当观察到三颈烧瓶中硫化氢气泡的逸出速度与烧杯中的接近时可关闭K
1C.步骤c中,溶液酸化后加热,有利于H
2S溢出,除去H
2S
D.步骤d中,加入碳酸钡的作用是除去多余的硫酸,过滤得到的沉淀中只含有硫酸钡和过量碳酸钡
(3)根据碘化钾的溶解度随温度变化情况,选择恰当的选项对步骤e中实验操作进行排序:a→
____ →b。
| 碘化钾的溶解度/g |
| 6°C | 20℃ | 60°C | 100°C |
| 128 | 140 | 176 | 206 |
a.将滤液和洗涤液混合后加入蒸发皿中
b.取出晶体,用干净滤纸吸干,称重
c.减压过滤
d.酒精灯加热浓缩至溶液中出现大量晶体,停止加热
e.用少量蒸馏水洗涤晶体2-3次
f.沸水浴加热蒸发浓缩至溶液表面出现晶膜,停止加热
g.室温条件下放置自然冷却
h.用少量酒精溶液洗涤晶体2-3次
(4)在实验所需溶液配制过程中,下列说法正确的是
__________ 。
A.检漏时发现容量瓶漏水,可以在瓶塞和瓶口内侧涂抹少量凡士林以防漏水
B.容量瓶在检漏和洗净后,可以放置在烘箱内低温烘干备用
C.转移和洗涤操作后,应将容量瓶按下图方式摇晃初步混匀,再进行定容
D.配制完成的溶液应转移至试剂瓶中贮存,洗净的试剂瓶应先用该溶液润洗2-3次
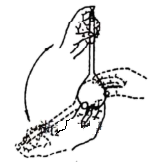
(5)纯净的碘化钾为白色颗粒状固体,所得产品略带黄色,请分析原因:
____________。