17. 三草酸合铁(III)酸钾K
3[Fe(C
2O
4)
3]·3H
2O是光化学研究中一种常见物质,为翠绿色单斜晶体。实验室利用硫酸亚铁铵[化学式为(FeSO
4·(NH
4)
2SO
4·6H
2O]、草酸等原料制备三草酸合铁(III)酸钾的流程如下:
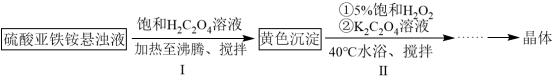
已知:K
3[Fe(C
2O
4)
3]·3H
2O可溶于水,在水中的溶解度随温度升高而增大(0℃时,溶解度为4.7 g;100℃时,溶解度为117.7 g)。
I.三草酸合铁(III)酸钾的制备
(1)写出步骤I生成黄色沉淀FeC
2O
4·2H
2O的化学方程式
_______。
(2)分析步骤II需要维持40℃水浴的原因
_______。
II.三草酸合铁(III)酸钾的组成分析

含量的测定
在电子分析天平上称取少量样品,加入适量2mol·L
−1H
2SO
4和去离子水微热溶解,并配成100mL溶液。取出10.00mL,用0.0200mol·L
−1KMnO
4标准溶液滴定,发生反应的离子方程式为:5

+2

+16H
+=10CO
2↑+2Mn
2++8H
2O,达滴定终点时,消耗KMnO
4标准溶液14.00mL(保留溶液待下一步分析使用)。
Fe
3+含量的测量
在上述保留的溶液中加入一小匙锌粉,加热近沸,直到黄色消失,使Fe
3+完全转化为Fe
2+,趁热过滤除去多余的锌粉,滤液收集到另一锥形瓶中。继续用0.0200 mol·L
−1KMnO
4标准溶液进行滴定,达到滴定终点时,消耗 KMnO
4溶液的体积为2.00 mL。
(3)测定

含量的实验中,滴定达到终点时的现象是
_______。
(4)通过计算确定

与Fe
3+粒子数目的比值:n(

)/n(Fe
3+)=
_______ (写出计算过程)。
(5)结果分析:假设测定结果 n(

)/n(Fe
3+)大于3﹕1,请分析原因(假设测定过程中各项操作规范)
_______。