名校
解题方法
1 . X、Y、Z三种元素基态原子的价电子排布式分别为 、
、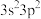 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是
 、
、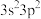 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是A. | B.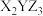 | C.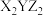 | D. |
您最近一年使用:0次
2024-04-04更新
|
151次组卷
|
10卷引用:吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题
吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题2014-2015河南省实验中学高二下学期期中考试化学试卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题湖南省汨罗市楚雄中学2021-2022学年高二12月月考化学试题四川省广元中学2021-2022学年高二下学期第一次段考化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题甘肃省武山县第一高级中学2023-2024学年高二下学期第一次月考化学试卷
2 . 化合物H是一种抗艾滋病药物,某课题组设计的合成路线如下:
(1)写出有机物A的名称___________ 。
(2)过程A→B的作用是___________ 。
(3)写出在一定条件下,B与足量NaOH溶液反应的化学方程式___________ 。
(4)化合物D的结构简式是___________ 。
(5)下列说法错误的是___________ (填标号)。
a.E分子中碳原子的杂化方式有3种
b.合成H过程中涉及的反应类型均为取代反应
c.F与足量H2加成后,产物分子中含有4个手性碳原子
d.化合物G可以与水形成分子间氢键,易溶于水
(6)化合物N(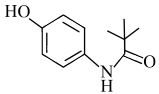 )是另一种合成路线的中间体,化合物N符合下列条件的同分异构体有
)是另一种合成路线的中间体,化合物N符合下列条件的同分异构体有___________ 种,写出其中一种结构简式___________ 。
①含有苯环;②H-NMR谱显示有6种不同化学环境的氢原子;③能发生水解反应,产物之一是甘氨酸。

(1)写出有机物A的名称
(2)过程A→B的作用是
(3)写出在一定条件下,B与足量NaOH溶液反应的化学方程式
(4)化合物D的结构简式是
(5)下列说法错误的是
a.E分子中碳原子的杂化方式有3种
b.合成H过程中涉及的反应类型均为取代反应
c.F与足量H2加成后,产物分子中含有4个手性碳原子
d.化合物G可以与水形成分子间氢键,易溶于水
(6)化合物N(
 )是另一种合成路线的中间体,化合物N符合下列条件的同分异构体有
)是另一种合成路线的中间体,化合物N符合下列条件的同分异构体有①含有苯环;②H-NMR谱显示有6种不同化学环境的氢原子;③能发生水解反应,产物之一是甘氨酸。
您最近一年使用:0次
名校
解题方法
3 . 由Li、Al、Si构成的某三元化合物固态晶胞结构如图所示:

| A.晶体中Li、Al、Si三种微粒的比例为1:1:1 |
B.图中所指Si原子的坐标为( , , , , ) ) |
| C.晶体中与每个Al紧邻的Li为6个,与每个Si紧邻的Si为12个 |
| D.晶体中Al和Li构成CsCl型晶体结构,晶体中Al和Si构成金刚石型晶体结构 |
您最近一年使用:0次
2024-04-04更新
|
393次组卷
|
3卷引用:吉林省吉林地区普通高中2024届高三三模考试化学试卷
吉林省吉林地区普通高中2024届高三三模考试化学试卷2024届河北省雄安新区部分高中高三下学期三模化学试题(已下线)压轴题10?晶体结构及相关计算(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
4 . 空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成视觉障碍的叫霾。科研人员提出了雾霾微颗粒中硫酸盐(含SO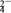 、HSO
、HSO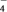 )生成的三个阶段的转化机理,其主要过程示意图如图,下列说法错误的是
)生成的三个阶段的转化机理,其主要过程示意图如图,下列说法错误的是
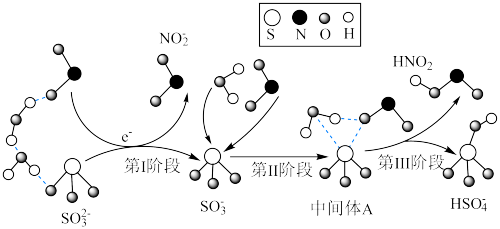
A.SO 和NO 和NO 的中心原子的杂化轨道类型分别是:sp3、sp2 的中心原子的杂化轨道类型分别是:sp3、sp2 |
| B.整个过程中有H2O参加反应,而且包含了硫氧键的断裂与形成 |
C.1molSO 在第Ⅱ、Ⅲ两个阶段共失去电子数目为NA 在第Ⅱ、Ⅲ两个阶段共失去电子数目为NA |
D.硫酸盐转化过程中发生的总反应方程式为:SO +2NO2+H2O=HSO +2NO2+H2O=HSO +NO +NO +HNO2 +HNO2 |
您最近一年使用:0次
2024-04-04更新
|
423次组卷
|
3卷引用:吉林省吉林地区普通高中2024届高三三模考试化学试卷
吉林省吉林地区普通高中2024届高三三模考试化学试卷河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题(已下线)压轴题04?化学反应机理、历程、能垒图分析(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
5 . A、B、C、D、E是五种原子序数依次递增的短周期元素。已知:A的一种同位素可以用于测定文物的年代;基态C原子含3对成对电子;D在同周期金属元素中第一电离能最大;基态E原子的3p轨道中含有自旋方向不同且数目之比为3:1的电子。下列说法正确的是
| A.简单离子的离子半径:B<C<D<E |
| B.简单氢化物的沸点:A<B<C<E |
| C.D的单质可以在A和C形成的某种化合物中燃烧 |
| D.Xe(氙)是目前最易形成化合物的稀有气体,XeC3为非极性分子 |
您最近一年使用:0次
2024-04-04更新
|
1269次组卷
|
5卷引用:吉林省吉林地区普通高中2024届高三三模考试化学试卷
吉林省吉林地区普通高中2024届高三三模考试化学试卷(已下线)题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)化学(新七省高考“15+4”)-2024年高考押题预测卷湖南省衡阳市衡阳县第一中学2023-2024学年高三下学期4月月考化学试题2024届河南省信阳市光山县第二高级中学高三下学期模拟预测理综试题-高中化学
名校
6 . 设NA为阿伏加德罗常数的值。下列叙述中正确的是
| A.28gC5H10的烃分子中含有C-C σ键的数目一定为1.6NA |
| B.在标准状况下,22.4L由SO2和SO3组成的混合物中含有硫原子的数目为NA |
| C.有2.00L0.5mol·L−1的稀硫酸和足量金属钠反应,消耗钠原子的数目为2NA |
| D.在2CuH+2HCl==Cu+CuCl2+2H2↑反应中,每生成4.48L(标准状况)H2,反应转移的电子数目为0.3NA |
您最近一年使用:0次
2024-04-04更新
|
812次组卷
|
3卷引用:吉林省吉林地区普通高中2024届高三三模考试化学试卷
吉林省吉林地区普通高中2024届高三三模考试化学试卷(已下线)题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)河北省张家口市尚义县第一中学等校2023-2024学年高三下学期模拟演练化学试题
名校
解题方法
7 . 某锂离子电池电解液中溶质的结构如图所示,X、Y、Z、W为原子序数依次增大的短周期元素,W原子的最外层电子数是内层电子数的一半。下列说法正确的是
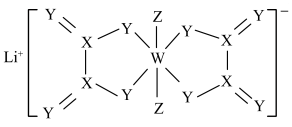
| A.原子半径:W>Z>Y |
| B.含X、Y元素的盐溶液可能呈碱性 |
| C.W的最高价氧化物对应水化合物是强酸 |
| D.Y和Z分别形成的最简单氢化物的稳定性:Y>Z |
您最近一年使用:0次
2024-04-01更新
|
535次组卷
|
5卷引用:2024届吉林省吉林市第一中学高三下学期适应性训练化学试题
名校
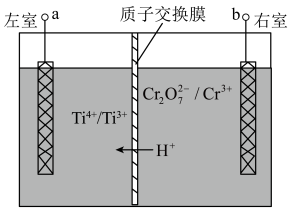
8 . 一种电解装置如图所示,电解时 从右室移向左室。通过电解获得的电解液可实现
从右室移向左室。通过电解获得的电解液可实现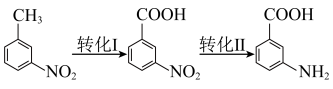 。下列说法正确的是
。下列说法正确的是
| A.左室电解获得的电解液可用于实现“转化Ⅰ” |
B.右室发生的电极反应为 |
C.“转化Ⅱ”发生的反应为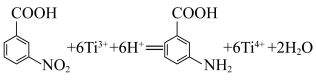 |
D.“转化Ⅰ”生成1 mol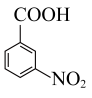 ,理论上电路中通过:3 mol ,理论上电路中通过:3 mol  |
您最近一年使用:0次
2024-03-31更新
|
638次组卷
|
5卷引用:吉林省吉林市第一中学2024届高三下学期适应性训练化学试题
吉林省吉林市第一中学2024届高三下学期适应性训练化学试题江苏省南通市2024届高三下学期第二次调研测试化学试题(已下线)通关练09 重温“两池”原理及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2024届河北省雄安新区部分高中高三下学期三模化学试题江苏省宿迁地区2023-2024学年高二下学期期中调研测试化学试题
9 . 常温下,向0.02mol·L-1 FeCl3溶液(用少量盐酸酸化)中匀速逐滴加入0.1mol·L-1 NaOH溶液,得到pH-t曲线如图。下列说法正确的是
已知:25℃时,Fe(OH)3的Ksp=2.8×10-39
已知:25℃时,Fe(OH)3的Ksp=2.8×10-39
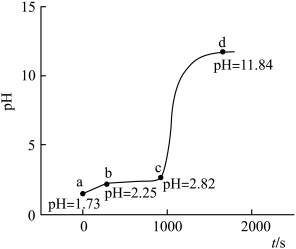
| A.已知a点为滴定起始点,pH=1.73是因为FeCl3溶于水发生了水解反应 |
| B.由a点到b点的过程中,滴加的NaOH溶液与FeCl3发生反应 |
| C.该条件下,Fe3+的沉淀pH范围约为2.25~2.82 |
| D.d点的溶液中,由水电离出的c(OH—)约为10-2.16mol·L-1 |
您最近一年使用:0次
2024-03-26更新
|
664次组卷
|
5卷引用:2024届吉林省吉林市第一中学高三下学期适应性训练化学试题
2024届吉林省吉林市第一中学高三下学期适应性训练化学试题北京市顺义区2023-2024学年高三上学期第一次统练化学试题 (已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)北京交通大学附属中学2023-2024学年高三下学期3月月考化学试题福建省福州市八县市一中2024届高三下学期模拟联考化学试题
名校
10 . 1922年范斯莱克(Vanslyke)提出用缓冲容量β来描述缓冲溶液缓冲能力大小,β越大,缓冲能力越大。下图是常温下,CH3COOH和CH3COONa组成缓冲溶液的β-pH关系图,其中A、B两条曲线分别对应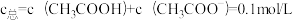 和
和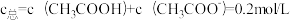 。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
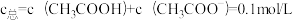 和
和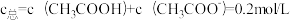 。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是
。已知常温下,Ka(CH3COOH)=10-4.76,下列说法不正确的是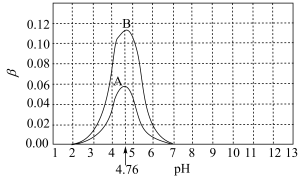
| A.向pH=4.76的上述缓冲溶液中加入少量NaOH溶液,水的电离程度会增大 |
B.A曲线上任意一点的溶液中均存在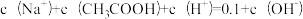 |
| C.B曲线代表的溶液缓冲能力最大时,溶液中c(Na+)>c(CH3COOH) |
D.pH=4时,A、B曲线所代表的溶液中 相等 相等 |
您最近一年使用:0次
2024-03-16更新
|
364次组卷
|
4卷引用:吉林省吉林市第一中学2024届高三下学期适应性训练化学试题



