1 . 某些资料表明:NO、NO2不能与Na2O2反应。某小组学生提出质疑,他们从理论上分析Na2O2和NO2都有氧化性,根据化合价升降原则提出如下假设:
假设Ⅰ. Na2O2氧化NO2; 假设Ⅱ. NO2氧化Na2O2。
请回答下列问题:
(1)甲同学设计如图1所示实验装置:
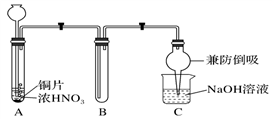
①试管A中反应的离子方程式是___________________________________________________ 。
②待试管B中收集满气体,向试管B中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。甲同学据此认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,应在A、B之间增加一个装置,该装置的作用是__________________________________________________________________ 。
③乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的化学方程式是_____________________ 。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化,查阅资料知:
ⅰ) 2NO+Na2O2===2NaNO2;
ⅱ) 6NaNO2+3H2SO4===3Na2SO4+2HNO3+4NO↑+2H2O;
ⅲ)酸性条件下,NO或NO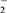 都能与MnO
都能与MnO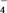 反应生成NO
反应生成NO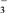 和Mn2+。
和Mn2+。
丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应:
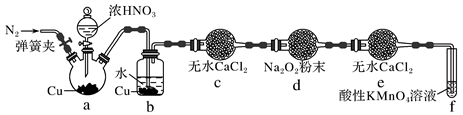
①b装置中观察到的主要现象是__________________________________________________ ,f装置的作用是_________________________________________________________________ 。
②在反应前,先打开弹簧夹,通入一段时间N2,其目的是____________________________
③充分反应后,检验d装置中发生反应的实验是___________________________ 。
假设Ⅰ. Na2O2氧化NO2; 假设Ⅱ. NO2氧化Na2O2。
请回答下列问题:
(1)甲同学设计如图1所示实验装置:

图1
①试管A中反应的离子方程式是
②待试管B中收集满气体,向试管B中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。甲同学据此认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,应在A、B之间增加一个装置,该装置的作用是
③乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的化学方程式是
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化,查阅资料知:
ⅰ) 2NO+Na2O2===2NaNO2;
ⅱ) 6NaNO2+3H2SO4===3Na2SO4+2HNO3+4NO↑+2H2O;
ⅲ)酸性条件下,NO或NO
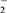 都能与MnO
都能与MnO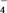 反应生成NO
反应生成NO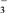 和Mn2+。
和Mn2+。丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应:

图2
①b装置中观察到的主要现象是
②在反应前,先打开弹簧夹,通入一段时间N2,其目的是
③充分反应后,检验d装置中发生反应的实验是
您最近一年使用:0次
2018-05-01更新
|
183次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——氮及其氧化物的性质(提升练)
名校
解题方法
2 . 为探究Na2SO3溶液和铬(VI)盐溶液的反应规律,某小组同学进行实验如下:已知: (橙色)+ H2O⇌
(橙色)+ H2O⇌ (黄色)+ 2H+
(黄色)+ 2H+
(1)配制溶液
①用化学用语表示饱和Na2SO3溶液pH约为9的原因:__ 。
(2)进行实验iii和iv:
②用离子方程式解释iii中现象:__ 。
(3)继续进行实验v:
③实验vi的目的是__ 。
④用化学平衡移动原理解释v中现象:__ 。
⑤根据实验iii~v,可推测:Na2SO3溶液和铬(VI)盐溶液的反应与溶液酸碱性有关,__ 。
⑥向实验v所得黄色溶液中滴加__ ,产生的现象证实了上述推测。
(4)继续探究溶液酸性增强对铬(VI)盐溶液氧化性的影响,该同学利用如图装置继续实验(已知电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,电压为a。
b.向U形管左侧溶液中滴加3滴浓硫酸后,电压增大了b。
⑦上述实验说明:__ 。
⑧有同学认为:随溶液酸性增强,溶液中O2的氧化性增强也会使电压增大。利用如图装置选择合适试剂进行实验,结果表明O2的存在不影响上述结论。该实验方案是__ ,测得电压增大了d(d < b)。
 (橙色)+ H2O⇌
(橙色)+ H2O⇌ (黄色)+ 2H+
(黄色)+ 2H+(1)配制溶液
| 序号 | 操作 | 现象 |
| i | 配制饱和Na2SO3溶液,测溶液的pH | pH约为9 |
| ii | 配制0.05 mol·L−1的K2Cr2O7溶液,把溶液平均分成两份,向两份溶液中分别滴加浓硫酸和浓KOH溶液,得到pH=2的溶液A和pH=8的溶液B | pH=2的溶液A呈橙色;pH=8的溶液B呈黄色 |
①用化学用语表示饱和Na2SO3溶液pH约为9的原因:
(2)进行实验iii和iv:
| 序号 | 操作 | 现象 |
| iii | 向2 mL溶液A中滴加3滴饱和Na2SO3溶液 | 溶液变绿色(含Cr3+) |
| iv | 向2 mL溶液B中滴加3滴饱和Na2SO3溶液 | 溶液没有明显变化 |
②用离子方程式解释iii中现象:
(3)继续进行实验v:
| 序号 | 操作 | 现象 |
| v | 向2 mL饱和Na2SO3溶液中滴加3滴溶液A | 溶液变黄色 |
| vi | 向2 mL蒸馏水中滴加3滴溶液A | 溶液变浅橙色 |
③实验vi的目的是
④用化学平衡移动原理解释v中现象:
⑤根据实验iii~v,可推测:Na2SO3溶液和铬(VI)盐溶液的反应与溶液酸碱性有关,
⑥向实验v所得黄色溶液中滴加
(4)继续探究溶液酸性增强对铬(VI)盐溶液氧化性的影响,该同学利用如图装置继续实验(已知电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,电压为a。
b.向U形管左侧溶液中滴加3滴浓硫酸后,电压增大了b。
⑦上述实验说明:
⑧有同学认为:随溶液酸性增强,溶液中O2的氧化性增强也会使电压增大。利用如图装置选择合适试剂进行实验,结果表明O2的存在不影响上述结论。该实验方案是
您最近一年使用:0次
3 . 在学习氧化还原反应时,某同学提出Ag+具有较强氧化性,I-具有较强还原性,二者也可发生氧化还原反应。为验证这个问题,该学生设计了系列实验。
(1)研究AgNO3溶液与KI溶液反应产物
向盛有1mL1mol/LAgNO3溶液的试管中加入1mL1mol/LKI溶液,振荡试管,向其中加入___ ,溶液无明显变化。(提示:若发生氧化还原反应,I-应被氧化为单质)
(实验结论)二者混合只发生沉淀反应,无明显氧化还原反应。
(2)验证Ag+的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中铁的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用试剂:①KSCN溶液②NaOH溶液③酸性KMnO4溶液。请完成下表:
(实验结论)铁的氧化产物为Fe2+和Fe3+,则Ag+氧化性强于Fe3+。
另一同学用pH计测得常温该硝酸银溶液的pH为5.50,于是该同学对实验结论提出质疑。你认为他提出质疑的理由可能是____ 。
(3)电池原理探究Ag+与I-之间的氧化还原反应
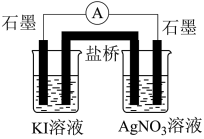
按图设计原电池。电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。读懂文中划线部分内容,请回答以下问题:
根据下表数据,盐桥中应选择_____ 作为电解质。
(4)已知Cl2能氧化+4价的硫为+6价的硫。请写出Na2SO3溶液和Cl2反应反应的离子方程式____ 。
(5)硫酸亚铁受热可按下式分解:aFeSO4=bFeO+cFe2O3+dSO3+eSO2+fO2,a、b、c、d、e、f为待定系数,若d:e:f=3:4:1,则b:c=_____ 。
(1)研究AgNO3溶液与KI溶液反应产物
向盛有1mL1mol/LAgNO3溶液的试管中加入1mL1mol/LKI溶液,振荡试管,向其中加入
(实验结论)二者混合只发生沉淀反应,无明显氧化还原反应。
(2)验证Ag+的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中铁的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用试剂:①KSCN溶液②NaOH溶液③酸性KMnO4溶液。请完成下表:
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 存在Fe3+ | |
| 取少量除尽Ag+后的溶液于试管中,加入1~2滴 | 存在Fe2+ |
另一同学用pH计测得常温该硝酸银溶液的pH为5.50,于是该同学对实验结论提出质疑。你认为他提出质疑的理由可能是
(3)电池原理探究Ag+与I-之间的氧化还原反应

按图设计原电池。电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。读懂文中划线部分内容,请回答以下问题:
根据下表数据,盐桥中应选择
| 阳离子 | u∞×108(m2∙s-1∙V-1) | 阴离子 | u∞×108(m2∙s-1∙V-1) |
| Li+ | 4.07 |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 |  | 8.27 |
(5)硫酸亚铁受热可按下式分解:aFeSO4=bFeO+cFe2O3+dSO3+eSO2+fO2,a、b、c、d、e、f为待定系数,若d:e:f=3:4:1,则b:c=
您最近一年使用:0次
4 . 三氧化砷,俗称砒霜,分子式As2O3,是最具商业价值的砷化合物及主要的砷化学开始物料。它也是最古老的毒物之一,无臭无味,外观为白色霜状粉末,故称砒霜。
(1)完成并配平下列化学方程式:___ As2O3+___ Zn+___ H2SO4→___ AsH3+___ ZnSO4+___
(2)As2O3在上述反应中显示出来的性质是___ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3,则转移电子的物质的量为___ mol。
(4)砷化氢AsH3是一种很强的还原性,在室温下它能在空气中自然,其氧化产物是砒霜,写出该反应的化学方程式___ 。
(1)完成并配平下列化学方程式:
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3,则转移电子的物质的量为
(4)砷化氢AsH3是一种很强的还原性,在室温下它能在空气中自然,其氧化产物是砒霜,写出该反应的化学方程式
您最近一年使用:0次
2020-03-21更新
|
338次组卷
|
4卷引用:专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
(已下线)专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)2015届陕西省渭南市高三教学质量检测(一模)化学试卷上海市六校联考2015-2016学年高三上学期期中考试化学试题沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题
5 . IBr、ICl等称之为卤素互化物,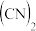 、
、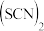 、
、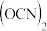 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
 氯化碘
氯化碘 能与水发生反应:
能与水发生反应: ,该反应
,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应。
氧化还原反应。
 溴化碘
溴化碘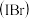 具有强氧化性,能与
具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为___ 。
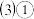 已知某些离子的还原性强弱顺序为
已知某些离子的还原性强弱顺序为 。现将几滴KSCN溶液滴入到含少量
。现将几滴KSCN溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________ 。
 下列物质中,也可以使该溶液红色褪去的是
下列物质中,也可以使该溶液红色褪去的是 _________ 。
A.新制氯水 碘水
碘水 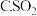
 盐酸
盐酸
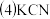 为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为_______________ 。
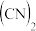 、
、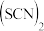 、
、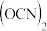 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。 氯化碘
氯化碘 能与水发生反应:
能与水发生反应: ,该反应
,该反应 填“是”或“不是”
填“是”或“不是” 氧化还原反应。
氧化还原反应。 溴化碘
溴化碘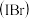 具有强氧化性,能与
具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为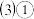 已知某些离子的还原性强弱顺序为
已知某些离子的还原性强弱顺序为 。现将几滴KSCN溶液滴入到含少量
。现将几滴KSCN溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象 下列物质中,也可以使该溶液红色褪去的是
下列物质中,也可以使该溶液红色褪去的是 A.新制氯水
 碘水
碘水 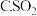
 盐酸
盐酸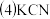 为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为
您最近一年使用:0次
2020-01-30更新
|
274次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——氯及其化合物
6 . 已知HNO2在低温下较稳定,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表,且酸性: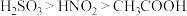 。下列有关说法
。下列有关说法错误 的是

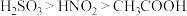 。下列有关说法
。下列有关说法

| pH范围 |  |  |
| 产物 |  | NO、 、 、 中的一种 中的一种 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为 |
| B.向冷的NaNO2溶液中通入H2S气体,有淡黄色沉淀产生 |
| C.低温时不用其它试剂即可区分HNO2溶液与Na2CO3溶液 |
| D.向冷的NaNO2溶液中通入SO2可得到HNO2 |
您最近一年使用:0次
名校
解题方法
7 . 某化学兴趣小组为制取NH3并探究其性质,按下图装置进行实验。【制取氨气的反应原理:2NH4Cl+Ca(OH)2 CaCl2+2NH3+2H2O,部分夹持仪器已略去】
CaCl2+2NH3+2H2O,部分夹持仪器已略去】
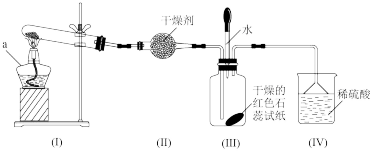
【实验探究】(1)装置(I)中仪器a的名称是_____ 。
(2)装置(Ⅱ)中可用_________ (填“碱石灰”或“食盐”)作干燥剂。
(3)实验进行一段时间后,装置(Ⅲ)中干燥的红色石蕊试纸不变色,然后滴加水,观察到试纸颜色变为___ (填“白色”或“蓝色”)原因是氨水呈____ (填“碱性”或“酸性”)。
(4)装置(Ⅲ)中胶头滴管若改装浓盐酸,实验进行一段时间后,滴加浓盐酸,观察到瓶内充满_______ (填“白烟”或“白雾”),写出NH3与HCl反应生成NH4Cl的化学方程式:_________ 。
(5)装置(IV)中稀硫酸的作用是___________ 。
(6)用0.1 mol NH4Cl与足量Ca(OH)2反应,理论上可生成NH3的物质的量是____ mol。
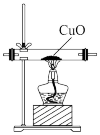
【实验拓展】(7)已知:2NH3+3CuO 3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为
3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为____ (填“白色”或“红色”),在这过程中NH3表现出__ (填“还原性”或“氧化性”)。
【知识应用】(8)氨气是一种重要的化工原料。写出它的一种用途:__________ 。
 CaCl2+2NH3+2H2O,部分夹持仪器已略去】
CaCl2+2NH3+2H2O,部分夹持仪器已略去】
【实验探究】(1)装置(I)中仪器a的名称是
(2)装置(Ⅱ)中可用
(3)实验进行一段时间后,装置(Ⅲ)中干燥的红色石蕊试纸不变色,然后滴加水,观察到试纸颜色变为
(4)装置(Ⅲ)中胶头滴管若改装浓盐酸,实验进行一段时间后,滴加浓盐酸,观察到瓶内充满
(5)装置(IV)中稀硫酸的作用是
(6)用0.1 mol NH4Cl与足量Ca(OH)2反应,理论上可生成NH3的物质的量是
【实验拓展】(7)已知:2NH3+3CuO
 3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为
3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为
【知识应用】(8)氨气是一种重要的化工原料。写出它的一种用途:
您最近一年使用:0次
2020-07-17更新
|
433次组卷
|
4卷引用:专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编
(已下线)专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编2020年6月福建省普通高中学业水平合格性考试化学试题福建省泉州市第七中学 2020--2021 学年高二上学期期末化学学业水平合格性测试二福建省莆田第七中学2021-2022学年高一下学期期中考试化学试题
名校
8 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
Ⅰ.制备N2H4
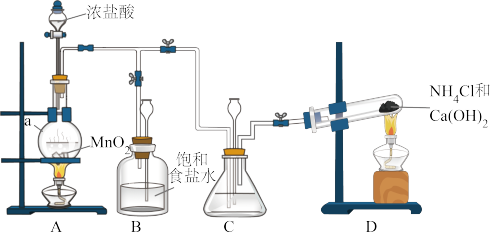
(1)仪器a的名称是___________ 。
(2)装置C中盛放的试剂是___________ 。装置B的作用是___________ 。
(3)制备N2H4的离子方程式为___________ 。
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
①滴定到达终点的现象是___________ 。
②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为___________ 。
Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(5)请完成表中的空白部分:①___________ ;②___________ 。
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:___________ 。
Ⅰ.制备N2H4

(1)仪器a的名称是
(2)装置C中盛放的试剂是
(3)制备N2H4的离子方程式为
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
①滴定到达终点的现象是
②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为
Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入适量①_________ | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 | ②_________ | 黑色固体是Ag和Ag2O |
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:
您最近一年使用:0次
2022-03-29更新
|
833次组卷
|
6卷引用:专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)
(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题四川省绵阳市高中2022-2023学年高二下学期理科突击班6月月考化学试题
2020高三·全国·专题练习
9 . IBr、ICl、BrF3等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称为拟卤素,它们的化学性质均与卤素单质相似,请回答下列问题。
(1)氯化碘(ICl)中碘元素的化合价为________ ;它与水反应的化学方程式为ICl+H2O=HIO+HCl,该反应的反应类型为________ (填中学常见的无机反应类型)。
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液反应,发生反应的离子方程式为__________________ 。
(3)①已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。现将几滴KSCN溶液滴入到含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象:________________________ 。
②下列物质中,也可以使该溶液红色褪去的是________ (填字母)。
A.新制氯水 B.碘水
C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法:在碱性条件下用NaClO溶液将CN-氧化为CO32-和一种单质气体,该反应的离子方程式为_____________________ 。
(5)已知HCN的电离常数K=6.2×10-10,H2CO3的电离常数K1=4.5×10-7,K2=4.7×10-11,则下列离子方程式能发生的是________ (填字母)。
A.CN-+CO2+H2O=HCN+
B.2HCN+ =2CN-+CO2↑+H2O
=2CN-+CO2↑+H2O
C.2CN-+CO2+H2O=2HCN+
D.HCN+ =CN-+
=CN-+
(1)氯化碘(ICl)中碘元素的化合价为
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液反应,发生反应的离子方程式为
(3)①已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。现将几滴KSCN溶液滴入到含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象:
②下列物质中,也可以使该溶液红色褪去的是
A.新制氯水 B.碘水
C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法:在碱性条件下用NaClO溶液将CN-氧化为CO32-和一种单质气体,该反应的离子方程式为
(5)已知HCN的电离常数K=6.2×10-10,H2CO3的电离常数K1=4.5×10-7,K2=4.7×10-11,则下列离子方程式能发生的是
A.CN-+CO2+H2O=HCN+

B.2HCN+
 =2CN-+CO2↑+H2O
=2CN-+CO2↑+H2OC.2CN-+CO2+H2O=2HCN+

D.HCN+
 =CN-+
=CN-+
您最近一年使用:0次
2014高三·全国·专题练习
10 . 一位学生对铁与氧化铁反应后的产物进行探究。
(1)提出假设
假设1:产物为FeO;
假设2: 。
(2)查阅资料
该学生通过查阅资料得知:在铁的三种氧化物中,四氧化三铁最稳定,氧化亚铁最不稳定,常温下极易被氧气氧化成氧化铁(颜色由黑色变成红色)。
通过查阅资料可以得出的初步结论为 。
(3)进行实验
该学生设计了如下装置进行铁与氧化铁反应的实验。请你帮助他将实验步骤补充完整。
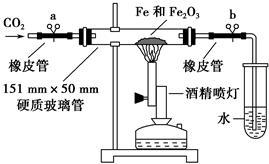
①按如图装置连接好仪器(暂不装入药品), 。
②称取1 g还原性铁粉和5 g氧化铁粉末,混合均匀后平摊在玻璃管中部。
③松开两个弹簧夹, ,即可夹上弹簧夹a,并开始加热药品
(4)现提供如下药品,验证实验得到的黑色粉末的成分。磁铁、稀盐酸、KSCN溶液、酸性KMnO4溶液、试管、胶头滴管。
(5)实验结论:铁与氧化铁反应的化学方程式为 。
(1)提出假设
假设1:产物为FeO;
假设2: 。
(2)查阅资料
该学生通过查阅资料得知:在铁的三种氧化物中,四氧化三铁最稳定,氧化亚铁最不稳定,常温下极易被氧气氧化成氧化铁(颜色由黑色变成红色)。
通过查阅资料可以得出的初步结论为 。
(3)进行实验
该学生设计了如下装置进行铁与氧化铁反应的实验。请你帮助他将实验步骤补充完整。

①按如图装置连接好仪器(暂不装入药品), 。
②称取1 g还原性铁粉和5 g氧化铁粉末,混合均匀后平摊在玻璃管中部。
③松开两个弹簧夹, ,即可夹上弹簧夹a,并开始加热药品
(4)现提供如下药品,验证实验得到的黑色粉末的成分。磁铁、稀盐酸、KSCN溶液、酸性KMnO4溶液、试管、胶头滴管。
| 实验步骤 | 预期现象和结论 |
(5)实验结论:铁与氧化铁反应的化学方程式为 。
您最近一年使用:0次



