1 . 钛(Ti)的性质稳定,有良好的耐高温、抗酸碱、高强度、低密度等特性,工业上常用钛铁矿(主要含) 和少量
和少量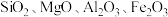 等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。
等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。 易水解,只能存在于强酸性溶液中;
易水解,只能存在于强酸性溶液中;
②常温下,相关金属离子开始沉淀和沉淀完全的pH如表所示。
(1) 中钛元素的化合价为
中钛元素的化合价为___________ ;“酸溶”时,常将钛铁矿粉碎的目的是___________ ;滤渣的成分是___________ (填化学式)。
(2)“酸溶”后,钛主要以 形式存在,写出相应反应的离子方程式:
形式存在,写出相应反应的离子方程式:___________ 。
(3)“分步沉淀”中当 沉淀完全时,“母液”中
沉淀完全时,“母液”中 的浓度为
的浓度为___________  。
。
(4)“水浸”后,过滤、洗涤得水浸渣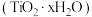 检验
检验 已洗涤干净的方法为
已洗涤干净的方法为___________ 。
(5)已知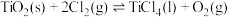
 ,该反应极难进行,从化学平衡的角度解释“氯化”时需向反应体系中加入焦炭的原因是
,该反应极难进行,从化学平衡的角度解释“氯化”时需向反应体系中加入焦炭的原因是___________ 。
(6)研究发现,可以用石墨、钛网作电极、熔融 作电解质,利用如图装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。若由
作电解质,利用如图装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。若由 制得
制得 金属
金属 ,则理论上产生的
,则理论上产生的 的体积换算成标准状况时为
的体积换算成标准状况时为___________ L。
 和少量
和少量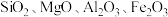 等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。
等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。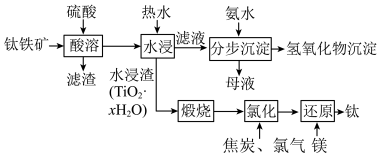
 易水解,只能存在于强酸性溶液中;
易水解,只能存在于强酸性溶液中;②常温下,相关金属离子开始沉淀和沉淀完全的pH如表所示。
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 2.2 | 6.5 | 3.5 | 9.5 |
沉淀完全(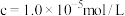 )的pH )的pH | 3.2 | 9.7 | 4.7 | 11.0 |
(1)
 中钛元素的化合价为
中钛元素的化合价为(2)“酸溶”后,钛主要以
 形式存在,写出相应反应的离子方程式:
形式存在,写出相应反应的离子方程式:(3)“分步沉淀”中当
 沉淀完全时,“母液”中
沉淀完全时,“母液”中 的浓度为
的浓度为 。
。(4)“水浸”后,过滤、洗涤得水浸渣
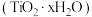 检验
检验 已洗涤干净的方法为
已洗涤干净的方法为(5)已知
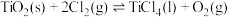
 ,该反应极难进行,从化学平衡的角度解释“氯化”时需向反应体系中加入焦炭的原因是
,该反应极难进行,从化学平衡的角度解释“氯化”时需向反应体系中加入焦炭的原因是(6)研究发现,可以用石墨、钛网作电极、熔融
 作电解质,利用如图装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。若由
作电解质,利用如图装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。若由 制得
制得 金属
金属 ,则理论上产生的
,则理论上产生的 的体积换算成标准状况时为
的体积换算成标准状况时为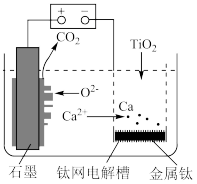
您最近一年使用:0次
解题方法
2 . 二氧化碳的资源化利用有利于碳中和目标实现。请回答下列问题:
(1) 加氢合成甲醇以及甲醇脱水生成二甲醚的热化学方程式如下:
加氢合成甲醇以及甲醇脱水生成二甲醚的热化学方程式如下:
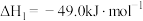 ,
,
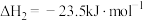 ,则
,则 的
的
___________  。该反应
。该反应___________ (填“自发进行”或“非自发进行”或“高温自发”或“低温自发”)
(2)向一容积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,一定温度下发生反应
,一定温度下发生反应 。
。 时达到化学平衡状态,测得
时达到化学平衡状态,测得 的物质的量分数为
的物质的量分数为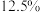 。
。
①达到化学平衡状态的标志是___________ (填标号)。
A.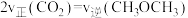
B.容器内混合气体的密度不再改变
C.容器内混合气体压强下再发生改变
D.容器内混合气体的平均相对分子质量不再改变
E.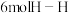 键断裂的同时生成
键断裂的同时生成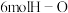 键
键
② 内,用
内,用 表示的平均反应速率
表示的平均反应速率
___________ ,平衡时 的转化率为
的转化率为___________ 。该温度下,反应的平衡常数K为___________ 。
(3) 可以被
可以被 捕获。若所得溶液中,
捕获。若所得溶液中,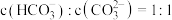 ,则溶液的pH为
,则溶液的pH为___________ 。若所得溶液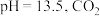 主要转化为
主要转化为___________ (填离子符号)。(已知:室温下 的
的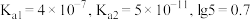 )
)
(1)
 加氢合成甲醇以及甲醇脱水生成二甲醚的热化学方程式如下:
加氢合成甲醇以及甲醇脱水生成二甲醚的热化学方程式如下:
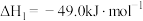 ,
,
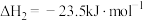 ,则
,则 的
的
 。该反应
。该反应(2)向一容积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,一定温度下发生反应
,一定温度下发生反应 。
。 时达到化学平衡状态,测得
时达到化学平衡状态,测得 的物质的量分数为
的物质的量分数为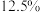 。
。①达到化学平衡状态的标志是
A.
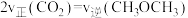
B.容器内混合气体的密度不再改变
C.容器内混合气体压强下再发生改变
D.容器内混合气体的平均相对分子质量不再改变
E.
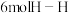 键断裂的同时生成
键断裂的同时生成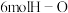 键
键②
 内,用
内,用 表示的平均反应速率
表示的平均反应速率
 的转化率为
的转化率为(3)
 可以被
可以被 捕获。若所得溶液中,
捕获。若所得溶液中,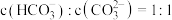 ,则溶液的pH为
,则溶液的pH为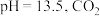 主要转化为
主要转化为 的
的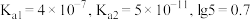 )
)
您最近一年使用:0次
解题方法
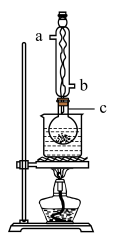
3 . 硫代硫酸钠( )又名大苏打、海波,是重要的化工原料,易溶于水,难溶于乙醇,在酸性条件下不稳定。某课外活动小组利用如图所示的实验装置制备
)又名大苏打、海波,是重要的化工原料,易溶于水,难溶于乙醇,在酸性条件下不稳定。某课外活动小组利用如图所示的实验装置制备 并测定产品纯度。已知,制备
并测定产品纯度。已知,制备 反应原理及
反应原理及 。
。___________ ,球形冷凝管中冷凝水的流向应从___________ (填“a”或“b”)口进。
(2)水浴加热一段时间后,将装置c中所得溶液趁热过滤,将滤液经蒸发浓缩、___________ 、过滤、洗涤、___________ ,得到 样品,洗涤时为尽可能避免产品损失应选用的试剂是
样品,洗涤时为尽可能避免产品损失应选用的试剂是___________ 。
(3)该实验一般控制在中性或碱性环境下进行,用离子反应方程式表示其可能的原因:___________ 。
(4)测定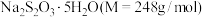 样品的纯度(杂质不参与反应)时,准确称取
样品的纯度(杂质不参与反应)时,准确称取 产品,溶于蒸馏水配成
产品,溶于蒸馏水配成 溶液,取
溶液,取 注入锥形瓶,以淀粉作指示剂,用
注入锥形瓶,以淀粉作指示剂,用 标准碘溶液滴定。已知:
标准碘溶液滴定。已知: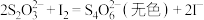
①滴定终点的现象为___________ 。
②重复上述操作,记录数据如下,则产品中 的质量分数为
的质量分数为___________ 。(列出算式即可)
③下列操作测得 的质量分数偏小的是
的质量分数偏小的是___________
a.读取标准碘溶液体积刻度时,滴定前仰视,滴定后平视
b.滴定前滴定管内有气泡,滴定后气泡消失
c.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
d.滴定管用蒸馏水洗净后,直接加入标准碘溶液
(5)市售硫代硫酸钠中常含有硫酸根离子,可用 溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度
溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度 认为完全除尽)溶液中
认为完全除尽)溶液中 的浓度至多为
的浓度至多为___________  。(已知:该温度下,
。(已知:该温度下,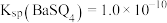 ,
,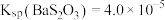 )。
)。
 )又名大苏打、海波,是重要的化工原料,易溶于水,难溶于乙醇,在酸性条件下不稳定。某课外活动小组利用如图所示的实验装置制备
)又名大苏打、海波,是重要的化工原料,易溶于水,难溶于乙醇,在酸性条件下不稳定。某课外活动小组利用如图所示的实验装置制备 并测定产品纯度。已知,制备
并测定产品纯度。已知,制备 反应原理及
反应原理及 。
。
(2)水浴加热一段时间后,将装置c中所得溶液趁热过滤,将滤液经蒸发浓缩、
 样品,洗涤时为尽可能避免产品损失应选用的试剂是
样品,洗涤时为尽可能避免产品损失应选用的试剂是(3)该实验一般控制在中性或碱性环境下进行,用离子反应方程式表示其可能的原因:
(4)测定
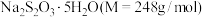 样品的纯度(杂质不参与反应)时,准确称取
样品的纯度(杂质不参与反应)时,准确称取 产品,溶于蒸馏水配成
产品,溶于蒸馏水配成 溶液,取
溶液,取 注入锥形瓶,以淀粉作指示剂,用
注入锥形瓶,以淀粉作指示剂,用 标准碘溶液滴定。已知:
标准碘溶液滴定。已知: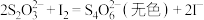
①滴定终点的现象为
②重复上述操作,记录数据如下,则产品中
 的质量分数为
的质量分数为| 滴定次数 | 滴定前/ | 滴定后/ |
| 第一次 | 0.00 | 28.11 |
| 第二次 | 0.30 | 30.30 |
| 第三次 | 0.22 | 28.35 |
 的质量分数偏小的是
的质量分数偏小的是a.读取标准碘溶液体积刻度时,滴定前仰视,滴定后平视
b.滴定前滴定管内有气泡,滴定后气泡消失
c.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
d.滴定管用蒸馏水洗净后,直接加入标准碘溶液
(5)市售硫代硫酸钠中常含有硫酸根离子,可用
 溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度
溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度 认为完全除尽)溶液中
认为完全除尽)溶液中 的浓度至多为
的浓度至多为 。(已知:该温度下,
。(已知:该温度下,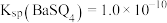 ,
,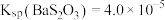 )。
)。
您最近一年使用:0次
4 . 回答下列问题。
(1)已知相关化学键的键能数据如下表:
则

___________  。
。
(2)利用污泥燃烧产生的还原性气体( 、CO等)可还原烟气中的
、CO等)可还原烟气中的 。CO还原NO的反应历程中相对能量变化如图1所示:
。CO还原NO的反应历程中相对能量变化如图1所示:
___________  ,该步骤的化学方程式是
,该步骤的化学方程式是___________ 。
(3)多晶Cu可高效催化 甲烷化,电解
甲烷化,电解 制备
制备 的原理示意图如图2所示。电解过程中温度控制在10℃左右,持续通入
的原理示意图如图2所示。电解过程中温度控制在10℃左右,持续通入 。阴、阳极室的
。阴、阳极室的 溶液的浓度基本保持不变。
溶液的浓度基本保持不变。___________ (填“阴”或“阳”)极,阳极上发生的电极反应式是___________ 。
②阴离子交换膜中传导的离子是___________ ,移动方向是___________ (填“从左向右”或“从右向左”)。
(1)已知相关化学键的键能数据如下表:
| 化学键 |  |  |  |  |  |
E/ | 436 | 414 | 464 | 326 | 803 |


 。
。(2)利用污泥燃烧产生的还原性气体(
 、CO等)可还原烟气中的
、CO等)可还原烟气中的 。CO还原NO的反应历程中相对能量变化如图1所示:
。CO还原NO的反应历程中相对能量变化如图1所示: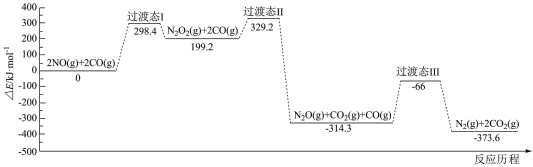
图1
该历程中最大能垒(活化能)
 ,该步骤的化学方程式是
,该步骤的化学方程式是(3)多晶Cu可高效催化
 甲烷化,电解
甲烷化,电解 制备
制备 的原理示意图如图2所示。电解过程中温度控制在10℃左右,持续通入
的原理示意图如图2所示。电解过程中温度控制在10℃左右,持续通入 。阴、阳极室的
。阴、阳极室的 溶液的浓度基本保持不变。
溶液的浓度基本保持不变。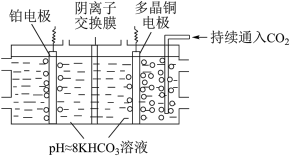
图2
①多晶Cu作②阴离子交换膜中传导的离子是
您最近一年使用:0次
5 . 近年来,化学界广泛开展研究二氧化碳与氢气的反应原理。回答下列问题:
(1)工业上可利用CO或 来生产燃料甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
来生产燃料甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
①据反应 与
与 可推导出
可推导出 、
、 与
与 之间的关系,则
之间的关系,则
___________ (用 、
、 表示)。
表示)。
②500℃时测得反应 在某时刻
在某时刻 、
、 、
、 、
、 的浓度(
的浓度( )分别为0.8、0.1、0.3、0.15,则此时
)分别为0.8、0.1、0.3、0.15,则此时
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(2)某装置中充入一定量 与
与 ,在673K、10.0kPa条件下发生反应:
,在673K、10.0kPa条件下发生反应: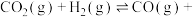
 ,得到部分气体的分压随时间的变化关系如图3所示:
,得到部分气体的分压随时间的变化关系如图3所示: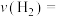
___________ kPa/min(保留两位有效数字)。
②已知反应在80min达到平衡状态,则在673K时,反应 的平衡常数
的平衡常数
___________ (保留两位有效数字)。
(3)在一装有某催化剂的恒容密闭装置中,充入10mol 和23mol
和23mol  ,在一定温度下发生反应:
,在一定温度下发生反应:
 .
. 和
和 .
. ,反应进行到
,反应进行到 时刻,各物质的物质的量不再改变,部分物质的物质的量与时间的关系如图4所示:
时刻,各物质的物质的量不再改变,部分物质的物质的量与时间的关系如图4所示: 时刻反应
时刻反应 的浓度熵
的浓度熵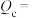
___________ (计算结果保留两位有效数字),b点时
___________ (填“是”或“否”)达到平衡状态。
② 时刻后,若升高装置温度,则重新达到平衡时,
时刻后,若升高装置温度,则重新达到平衡时,
___________ (填序号,下同),若将装置的体积缩小一倍,则重新达到平衡时,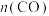
___________ 。
A.增大 B.减小 C.不变 D.无法确定
(1)工业上可利用CO或
 来生产燃料甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
来生产燃料甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:| 化学反应 | 平衡常数 | 温度/℃ | |
| 500 | 800 | ||
 . .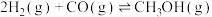 |  | 2.5 | 0.15 |
 . .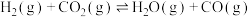 |  | 1.0 | 2.50 |
 . . |  | ||
 与
与 可推导出
可推导出 、
、 与
与 之间的关系,则
之间的关系,则
 、
、 表示)。
表示)。②500℃时测得反应
 在某时刻
在某时刻 、
、 、
、 、
、 的浓度(
的浓度( )分别为0.8、0.1、0.3、0.15,则此时
)分别为0.8、0.1、0.3、0.15,则此时
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(2)某装置中充入一定量
 与
与 ,在673K、10.0kPa条件下发生反应:
,在673K、10.0kPa条件下发生反应: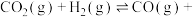
 ,得到部分气体的分压随时间的变化关系如图3所示:
,得到部分气体的分压随时间的变化关系如图3所示: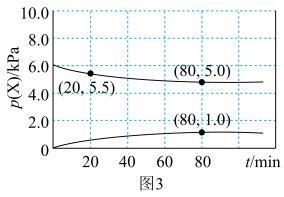
②已知反应在80min达到平衡状态,则在673K时,反应
 的平衡常数
的平衡常数
(3)在一装有某催化剂的恒容密闭装置中,充入10mol
 和23mol
和23mol  ,在一定温度下发生反应:
,在一定温度下发生反应: .
. 和
和 .
. ,反应进行到
,反应进行到 时刻,各物质的物质的量不再改变,部分物质的物质的量与时间的关系如图4所示:
时刻,各物质的物质的量不再改变,部分物质的物质的量与时间的关系如图4所示: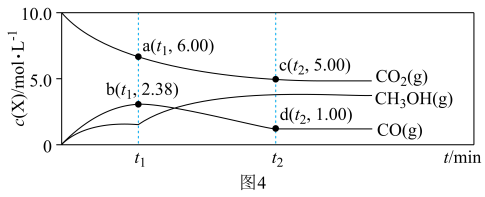
 时刻反应
时刻反应 的浓度熵
的浓度熵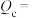

②
 时刻后,若升高装置温度,则重新达到平衡时,
时刻后,若升高装置温度,则重新达到平衡时,
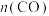
A.增大 B.减小 C.不变 D.无法确定
您最近一年使用:0次
6 . 锂在新能源等领域应用广泛。从粉煤灰(含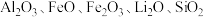 等)中回收提取铝、锂元素化合物的流程如下图所示:
等)中回收提取铝、锂元素化合物的流程如下图所示: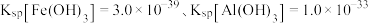 。
。
②当离子浓度≤ 时表示该离子沉淀完全
时表示该离子沉淀完全
回答下列问题
(1)除了“粉碎”粉煤灰,还可以通过___________ 来提高“酸浸”的速率(任写两条)。
(2)滤渣1的成分主要是___________ (填化学式)。
(3)“反应1”中加入 溶液的目的是
溶液的目的是___________ 。
(4)“滤渣2”的主要成分为 和
和 ,“调
,“调 ”中
”中 的最小值为
的最小值为___________ (保留一位小数)。
(5)从“滤渣2”中分离出 的方法如下:
的方法如下:___________ ;试剂 的最好选择是
的最好选择是___________ 。
a.稀 b.
b. c.
c. 溶液
溶液
(6)催化剂TAPP-Mn(Ⅱ)的应用,使 电池的研究取得了新的进展。电池结构和该催化剂作用下正极反应可能的历程如下图所示:
电池的研究取得了新的进展。电池结构和该催化剂作用下正极反应可能的历程如下图所示: 电极接电源
电极接电源___________ 极。
②放电时,正极反应式为___________ 。
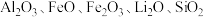 等)中回收提取铝、锂元素化合物的流程如下图所示:
等)中回收提取铝、锂元素化合物的流程如下图所示: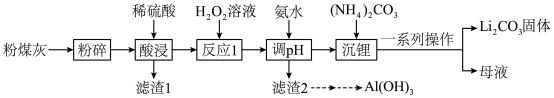
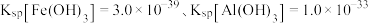 。
。②当离子浓度≤
 时表示该离子沉淀完全
时表示该离子沉淀完全回答下列问题
(1)除了“粉碎”粉煤灰,还可以通过
(2)滤渣1的成分主要是
(3)“反应1”中加入
 溶液的目的是
溶液的目的是(4)“滤渣2”的主要成分为
 和
和 ,“调
,“调 ”中
”中 的最小值为
的最小值为(5)从“滤渣2”中分离出
 的方法如下:
的方法如下: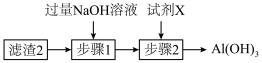
 的最好选择是
的最好选择是a.稀
 b.
b. c.
c. 溶液
溶液(6)催化剂TAPP-Mn(Ⅱ)的应用,使
 电池的研究取得了新的进展。电池结构和该催化剂作用下正极反应可能的历程如下图所示:
电池的研究取得了新的进展。电池结构和该催化剂作用下正极反应可能的历程如下图所示: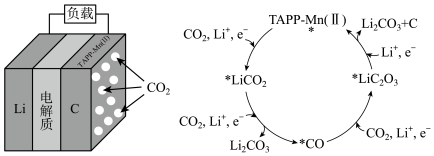
 电极接电源
电极接电源②放电时,正极反应式为
您最近一年使用:0次
解题方法
7 . 硫酸是一种重要的工业原料,常用于肥料、药物、染料等工业。接触法制硫酸生产中的关键工序是 的催化氧化。
的催化氧化。
已知: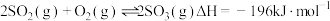
回答下列问题:
(1) 在催化剂
在催化剂 表面反应生成
表面反应生成 的历程为:
的历程为:
ⅰ.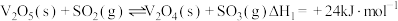
ⅱ.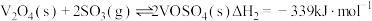
ⅲ.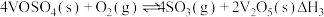

___________  ,反应ⅲ在
,反应ⅲ在___________ (填“高温”“低温”或“任意温度”)下能自发进行。
(2)工业生产中, 在接触室中被氧气氧化成
在接触室中被氧气氧化成 ,在密闭容器中,原料气按体积分数为
,在密闭容器中,原料气按体积分数为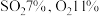 、
、 进料,分别在
进料,分别在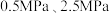 和
和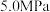 压强下发生反应,
压强下发生反应, 平衡转化率随温度变化关系如图所示:
平衡转化率随温度变化关系如图所示:
___________  (填“>”“<”或“=”);
(填“>”“<”或“=”);
②反应在0.5MPa、550℃时的
___________ ,判断的依据是___________ 。
(3)一定温度,将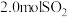 和
和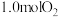 置于
置于 密闭容器中,发生反应
密闭容器中,发生反应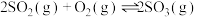 ,经
,经 达平衡,
达平衡, 的转化率为
的转化率为 ,体系总压强为
,体系总压强为 。
。
①此过程中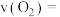
___________ mol/(L·min)。
②该反应的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4) 在吸收塔中转化为
在吸收塔中转化为 ,工业上不用水或稀硫酸,一般用
,工业上不用水或稀硫酸,一般用 的浓硫酸,主要原因是
的浓硫酸,主要原因是___________ 。
 的催化氧化。
的催化氧化。已知:
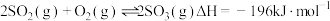
回答下列问题:
(1)
 在催化剂
在催化剂 表面反应生成
表面反应生成 的历程为:
的历程为:ⅰ.
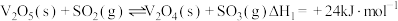
ⅱ.
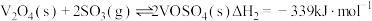
ⅲ.
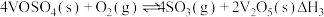

 ,反应ⅲ在
,反应ⅲ在(2)工业生产中,
 在接触室中被氧气氧化成
在接触室中被氧气氧化成 ,在密闭容器中,原料气按体积分数为
,在密闭容器中,原料气按体积分数为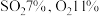 、
、 进料,分别在
进料,分别在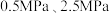 和
和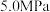 压强下发生反应,
压强下发生反应, 平衡转化率随温度变化关系如图所示:
平衡转化率随温度变化关系如图所示: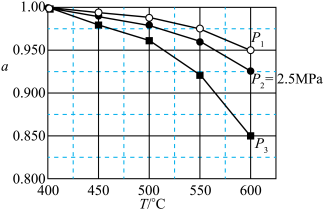

 (填“>”“<”或“=”);
(填“>”“<”或“=”);②反应在0.5MPa、550℃时的

(3)一定温度,将
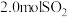 和
和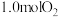 置于
置于 密闭容器中,发生反应
密闭容器中,发生反应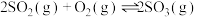 ,经
,经 达平衡,
达平衡, 的转化率为
的转化率为 ,体系总压强为
,体系总压强为 。
。①此过程中
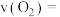
②该反应的平衡常数

 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)
 在吸收塔中转化为
在吸收塔中转化为 ,工业上不用水或稀硫酸,一般用
,工业上不用水或稀硫酸,一般用 的浓硫酸,主要原因是
的浓硫酸,主要原因是
您最近一年使用:0次
解题方法
8 .  作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用
作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用 氧化
氧化 制备
制备 的装置如图(部分夹持装置略):
的装置如图(部分夹持装置略):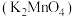 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 。
。
回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置B中的试剂为___________ ,缺少此装置对实验的影响为___________ 。
(3)装置C中生成高锰酸钾的化学方程式为___________ 。
(4)装置D中的试剂为___________ ,其作用为___________ 。
(5)利用 测定草酸亚铁晶体
测定草酸亚铁晶体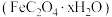 中
中 的值,实验步骤如下:
的值,实验步骤如下:
Ⅰ.准确称取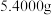 草酸亚铁晶体溶于一定浓度的硫酸中,配制成
草酸亚铁晶体溶于一定浓度的硫酸中,配制成 溶液;量取
溶液;量取 加入到锥形瓶中;
加入到锥形瓶中;
Ⅱ.用 标准溶液滴定至终点,平行测定三次,消耗
标准溶液滴定至终点,平行测定三次,消耗 标准溶液的体积平均值为
标准溶液的体积平均值为 。
。
已知:滴定过程中铁、碳元素分别被氧化为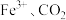 ,锰元素被还原为
,锰元素被还原为
①滴定时应将 溶液装入
溶液装入___________ (填“酸式”或“碱式”)滴定管中;
②滴定终点的现象是___________ ;
③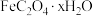 中
中
___________ 。[提示: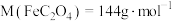 ]
]
 作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用
作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用 氧化
氧化 制备
制备 的装置如图(部分夹持装置略):
的装置如图(部分夹持装置略):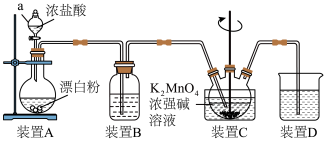
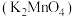 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 。
。回答下列问题:
(1)仪器a的名称是
(2)装置B中的试剂为
(3)装置C中生成高锰酸钾的化学方程式为
(4)装置D中的试剂为
(5)利用
 测定草酸亚铁晶体
测定草酸亚铁晶体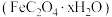 中
中 的值,实验步骤如下:
的值,实验步骤如下:Ⅰ.准确称取
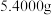 草酸亚铁晶体溶于一定浓度的硫酸中,配制成
草酸亚铁晶体溶于一定浓度的硫酸中,配制成 溶液;量取
溶液;量取 加入到锥形瓶中;
加入到锥形瓶中;Ⅱ.用
 标准溶液滴定至终点,平行测定三次,消耗
标准溶液滴定至终点,平行测定三次,消耗 标准溶液的体积平均值为
标准溶液的体积平均值为 。
。已知:滴定过程中铁、碳元素分别被氧化为
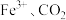 ,锰元素被还原为
,锰元素被还原为
①滴定时应将
 溶液装入
溶液装入②滴定终点的现象是
③
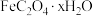 中
中
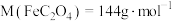 ]
]
您最近一年使用:0次
解题方法
9 . 汽车尾气是城市的主要空气污染物,尾气里含有的NO是由内燃机燃烧时产生的高温引起氮气和氧气反应所致: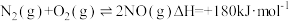
(1)该反应的平衡常数表达式为_______ 。
(2)用化学原理对氮氧化物进行处理可实现废物利用。已知H2的燃烧热为 ,在催化剂存在下,H2还原NO生成液态水和氮气的热化学方程式为
,在催化剂存在下,H2还原NO生成液态水和氮气的热化学方程式为_______ 。
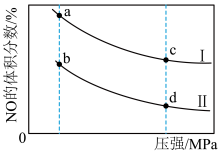
(3)利用反应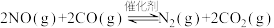 可实现汽车尾气的无害化处理。向甲、乙两个容积都为1L的恒容密闭容器中分别充入1.0molNO和1.0molCO,分别在T1、T2温度下发生上述反应。反应过程中n(CO2)随时间(t)的变化情况见下表,平衡时NO的体积分数与温度、压强的关系如下图:
可实现汽车尾气的无害化处理。向甲、乙两个容积都为1L的恒容密闭容器中分别充入1.0molNO和1.0molCO,分别在T1、T2温度下发生上述反应。反应过程中n(CO2)随时间(t)的变化情况见下表,平衡时NO的体积分数与温度、压强的关系如下图:

_______  (填“>”、“<”或“=”,下同),该反应的
(填“>”、“<”或“=”,下同),该反应的
_______ 0.温度、压强图中,曲线Ⅰ代表_______ (填“甲”或“乙”)容器。
②甲容器中NO的平衡转化率为_____ ,乙容器中,2~4s内N2的平均反应速率
_____ 。
③该反应达到平衡后,下列说法正确的是_______ 。
a.该反应在任意温度下均可自发
b.平衡常数:
c.该反应正反应活化能小于逆反应的活化能
d.升高温度可同时提高反应速率和NO的平衡转化率
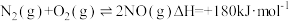
(1)该反应的平衡常数表达式为
(2)用化学原理对氮氧化物进行处理可实现废物利用。已知H2的燃烧热为
 ,在催化剂存在下,H2还原NO生成液态水和氮气的热化学方程式为
,在催化剂存在下,H2还原NO生成液态水和氮气的热化学方程式为(3)利用反应
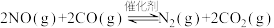 可实现汽车尾气的无害化处理。向甲、乙两个容积都为1L的恒容密闭容器中分别充入1.0molNO和1.0molCO,分别在T1、T2温度下发生上述反应。反应过程中n(CO2)随时间(t)的变化情况见下表,平衡时NO的体积分数与温度、压强的关系如下图:
可实现汽车尾气的无害化处理。向甲、乙两个容积都为1L的恒容密闭容器中分别充入1.0molNO和1.0molCO,分别在T1、T2温度下发生上述反应。反应过程中n(CO2)随时间(t)的变化情况见下表,平衡时NO的体积分数与温度、压强的关系如下图:| 时间(t)/s | 0 | 2 | 4 | 6 | 8 | 10 |
| 甲容器(T1)n(CO2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 | 0.80 |
| 乙容器(T2)n(CO2)/mol | 0 | 0.30 | 0.50 | 0.70 | 0.85 | 0.85 |

 (填“>”、“<”或“=”,下同),该反应的
(填“>”、“<”或“=”,下同),该反应的
②甲容器中NO的平衡转化率为

③该反应达到平衡后,下列说法正确的是
a.该反应在任意温度下均可自发
b.平衡常数:

c.该反应正反应活化能小于逆反应的活化能
d.升高温度可同时提高反应速率和NO的平衡转化率
您最近一年使用:0次
解题方法
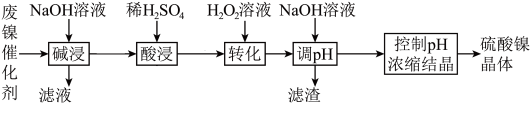
10 . 某油脂厂废弃的油脂加氢镍催化剂主要含有NiO、Al2O3、FeO、Fe2O3,还有少量油脂。采用如下工艺流程回收其中的镍并制备硫酸镍晶体(NiSO4⋅7H2O);
回答下列问题:
(1)写出一种可以提高“碱浸”速率的措施_______ 。
(2)“碱浸”中NaOH的作用是除去油脂和_______ 。为回收金属,向“滤液”中通入过量CO2,生成沉淀,该反应的离子方程式为_______ 。
(3)“转化”时反应的离子方程式是_______ ,“转化”过程中可替代 的物质是
的物质是_______ 。
(4)利用上述表格数据,计算Ni(OH)2的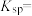
_____ ,如果“转化”后的溶液中Ni2+浓度为 ,则“调pH”应控制的范围是
,则“调pH”应控制的范围是_____ 。
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是_______ 。
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀时(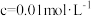 )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)写出一种可以提高“碱浸”速率的措施
(2)“碱浸”中NaOH的作用是除去油脂和
(3)“转化”时反应的离子方程式是
 的物质是
的物质是(4)利用上述表格数据,计算Ni(OH)2的
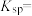
 ,则“调pH”应控制的范围是
,则“调pH”应控制的范围是(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次



