名校
1 .  有高毒性,在溶液中以
有高毒性,在溶液中以 或
或 的形式存在,不同
的形式存在,不同 条件下两者可相互转化(
条件下两者可相互转化( )。常用还原法、微生物电化学法、沉淀法处理含
)。常用还原法、微生物电化学法、沉淀法处理含 的废水。
的废水。
(1)向废水中加入 或
或 等还原剂可将
等还原剂可将 还原为低毒性
还原为低毒性 ,再调节溶液
,再调节溶液 使
使 转化为
转化为 沉淀除去。
沉淀除去。
①酸性废水中 将
将 还原为
还原为 的离子方程式为
的离子方程式为___________ 。
②其他条件相同,在不改变所加铁屑总量的情况下,加入烟道灰(细小的活性炭),可增大 的去除率,其原因是
的去除率,其原因是___________ 。
(2)利用微生物电化学法可有效处理含有机物和 的酸性废水,其工作原理如图所示。
的酸性废水,其工作原理如图所示。
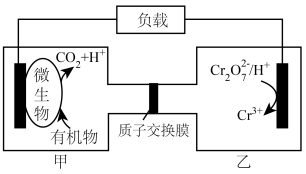
①若废水中的有机物是 ,则甲池中电极反应式为
,则甲池中电极反应式为___________ 。
②甲池产生 (标准状况)
(标准状况) 时,理论上乙池中
时,理论上乙池中 的物质的量减少
的物质的量减少___________ 。
(3)已知 易溶于水,
易溶于水, 难溶于水。利用沉淀法有效去除酸性废水中
难溶于水。利用沉淀法有效去除酸性废水中 的实验操作为
的实验操作为___________ 。
 有高毒性,在溶液中以
有高毒性,在溶液中以 或
或 的形式存在,不同
的形式存在,不同 条件下两者可相互转化(
条件下两者可相互转化( )。常用还原法、微生物电化学法、沉淀法处理含
)。常用还原法、微生物电化学法、沉淀法处理含 的废水。
的废水。(1)向废水中加入
 或
或 等还原剂可将
等还原剂可将 还原为低毒性
还原为低毒性 ,再调节溶液
,再调节溶液 使
使 转化为
转化为 沉淀除去。
沉淀除去。①酸性废水中
 将
将 还原为
还原为 的离子方程式为
的离子方程式为②其他条件相同,在不改变所加铁屑总量的情况下,加入烟道灰(细小的活性炭),可增大
 的去除率,其原因是
的去除率,其原因是(2)利用微生物电化学法可有效处理含有机物和
 的酸性废水,其工作原理如图所示。
的酸性废水,其工作原理如图所示。
①若废水中的有机物是
 ,则甲池中电极反应式为
,则甲池中电极反应式为②甲池产生
 (标准状况)
(标准状况) 时,理论上乙池中
时,理论上乙池中 的物质的量减少
的物质的量减少(3)已知
 易溶于水,
易溶于水, 难溶于水。利用沉淀法有效去除酸性废水中
难溶于水。利用沉淀法有效去除酸性废水中 的实验操作为
的实验操作为
您最近一年使用:0次
2023-11-19更新
|
319次组卷
|
3卷引用:山西省晋城市第一中学校2023-2024学年高二上学期第五次调研考试化学试题
名校
2 . 以甲烷为燃料、含铜氧化物为载体的化学链燃烧过程如图所示,下列说法不正确的是

| A.该流程中无需补充CuO |
B.空气反应器中的反应为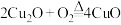 |
C.理论上燃料反应器中每产生22.0g ,空气反应器中要消耗标况下11.2L ,空气反应器中要消耗标况下11.2L |
D.该流程比传统燃烧更有利于捕集 |
您最近一年使用:0次
2023-11-16更新
|
133次组卷
|
2卷引用:山西省朔州市怀仁市2023-2024学年高一上学期1月期末化学试题
解题方法
3 . 8月1日起,为了国家信息安全,我国禁止镓和锗的出口,锗是一种重要的半导体材料,工业上用精硫锗矿(主要成分为 )制取高纯度锗的工艺流程如图所示:
)制取高纯度锗的工艺流程如图所示: 分子中各原子均达到8电子稳定结构,其结构式为
分子中各原子均达到8电子稳定结构,其结构式为___________ 。
(2)800℃升华时通入 的目的是:
的目的是:___________ 、___________ 。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:___________ ,酸浸时温度不能过高的原因是___________ 。
(4) 易水解生成
易水解生成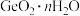 ,证明
,证明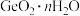 沉淀洗涤干净的方法是
沉淀洗涤干净的方法是___________ 。
(5)测定错的含量:称取0.5500g锗样品,加入双氧水溶解,再加入盐酸生成 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下
的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下 ,能将
,能将 氧化为
氧化为 ,①在滴定过程中依次发生的离子方程式为:
,①在滴定过程中依次发生的离子方程式为:___________ 、___________ ,②该样品中储的质量分数是___________ %(精确到0.01%)。
 )制取高纯度锗的工艺流程如图所示:
)制取高纯度锗的工艺流程如图所示: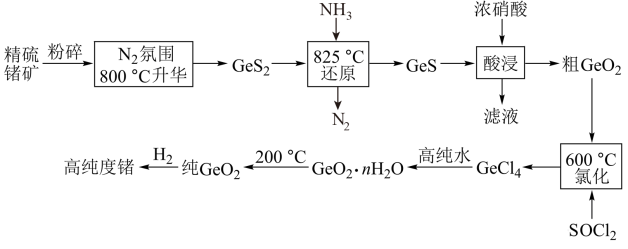
 分子中各原子均达到8电子稳定结构,其结构式为
分子中各原子均达到8电子稳定结构,其结构式为(2)800℃升华时通入
 的目的是:
的目的是:(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
(4)
 易水解生成
易水解生成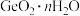 ,证明
,证明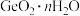 沉淀洗涤干净的方法是
沉淀洗涤干净的方法是(5)测定错的含量:称取0.5500g锗样品,加入双氧水溶解,再加入盐酸生成
 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下
的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下 ,能将
,能将 氧化为
氧化为 ,①在滴定过程中依次发生的离子方程式为:
,①在滴定过程中依次发生的离子方程式为:
您最近一年使用:0次
名校
解题方法
4 . 下列说法中正确的个数为
①在氧化还原反应中,金属单质在反应中只能作还原剂
②在氧化还原反应中,非金属单质在反应中只能作氧化剂
③某元素从游离志变为化合态,则该元素一定被还原
④有单质参加或生成的化学反应不一定是氧化还原反应
⑤氧化还原反应中的反应物不是氧化剂就是还原剂
⑥氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
⑦阳离子只有氧化性,阴离子只有还原性
⑧在 中只有1种粒子不具有还原性
中只有1种粒子不具有还原性
⑨氧化剂与还原剂混合一定能发生氧化还原反应
⑩金属原子失电子数越多,金属的还原性越强
①在氧化还原反应中,金属单质在反应中只能作还原剂
②在氧化还原反应中,非金属单质在反应中只能作氧化剂
③某元素从游离志变为化合态,则该元素一定被还原
④有单质参加或生成的化学反应不一定是氧化还原反应
⑤氧化还原反应中的反应物不是氧化剂就是还原剂
⑥氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
⑦阳离子只有氧化性,阴离子只有还原性
⑧在
 中只有1种粒子不具有还原性
中只有1种粒子不具有还原性⑨氧化剂与还原剂混合一定能发生氧化还原反应
⑩金属原子失电子数越多,金属的还原性越强
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
名校
5 . 氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中。下列变化涉及到氧化还原反应的有几个
①用石灰乳脱除烟气中的
②用盐酸去除铁锈(主要成分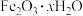 )
)
③用84消毒液(有效成分 )杀灭细菌
)杀灭细菌
④铜铸数像上出现铜绿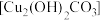
⑤用浸泡过高锰酸钾溶液的硅藻土保鲜水果
⑥谷物发酵酿造食醋
⑦大气中 参与酸雨形成
参与酸雨形成
⑧用赤铁矿石炼铁
⑨打磨磁石制指南针
①用石灰乳脱除烟气中的

②用盐酸去除铁锈(主要成分
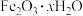 )
)③用84消毒液(有效成分
 )杀灭细菌
)杀灭细菌 ④铜铸数像上出现铜绿
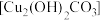
⑤用浸泡过高锰酸钾溶液的硅藻土保鲜水果
⑥谷物发酵酿造食醋
⑦大气中
 参与酸雨形成
参与酸雨形成 ⑧用赤铁矿石炼铁
⑨打磨磁石制指南针
| A.7个 | B.6个 | C.5个 | D.4个 |
您最近一年使用:0次
解题方法
6 . 某透明溶液中可能只存在Na+、Fe2+、Ba2+、NO 、CO
、CO 、HCO
、HCO 、SO
、SO 中的几种离子,现进行如下实验:
中的几种离子,现进行如下实验:
Ⅰ.取适量原溶液,向其中加入BaCl2溶液,无沉淀产生,继续滴加盐酸,严生无色的气体;
Ⅱ.另取适量原溶液,向其中逐滴滴入NaOH溶液,有沉淀a生成。
已知:①NO是一种无色气体;
②不考虑水电离出的H+和OH-;
③Fe2++NO +H+→Fe3++NO↑+H2O;
+H+→Fe3++NO↑+H2O;
④Fe2+与CO (或HCO
(或HCO )在同一溶液中不能大量共存;
)在同一溶液中不能大量共存;
⑤不考虑空气对反应的影响。
回答下列问题:
(1)仅由“取适量原溶液,向其中加入BaCl2溶液,无沉淀产生”可知,该溶液中一定不存在_______ (填离子符号),判断的理由为_______ (用离子方程式表示,写1个即可)。
(2)仅由“继续滴加盐酸,产生无色的气体”可知:
①原溶液中可能存在的离子有_______ (填标号)。
A.NO 、Fe2+ B.HCO
、Fe2+ B.HCO 、Fe2+ C.HCO
、Fe2+ C.HCO 、Na+、Ba2+ D.CO
、Na+、Ba2+ D.CO 、Fe2+、Na+、Ba2+
、Fe2+、Na+、Ba2+
②无色的气体可能是______ 。
③请配平离子方程式Fe2++NO +H+→Fe3++NO↑+H2O:
+H+→Fe3++NO↑+H2O:_______ 。
(3)若原溶液为绿色,则原溶液中一定存在的离子为________ (填离子符号)。
(4)往生成的沉淀a中加入稀盐酸,若有无色气体产生,此时发生反应的离子方程式为________ 。
 、CO
、CO 、HCO
、HCO 、SO
、SO 中的几种离子,现进行如下实验:
中的几种离子,现进行如下实验:Ⅰ.取适量原溶液,向其中加入BaCl2溶液,无沉淀产生,继续滴加盐酸,严生无色的气体;
Ⅱ.另取适量原溶液,向其中逐滴滴入NaOH溶液,有沉淀a生成。
已知:①NO是一种无色气体;
②不考虑水电离出的H+和OH-;
③Fe2++NO
 +H+→Fe3++NO↑+H2O;
+H+→Fe3++NO↑+H2O;④Fe2+与CO
 (或HCO
(或HCO )在同一溶液中不能大量共存;
)在同一溶液中不能大量共存;⑤不考虑空气对反应的影响。
回答下列问题:
(1)仅由“取适量原溶液,向其中加入BaCl2溶液,无沉淀产生”可知,该溶液中一定不存在
(2)仅由“继续滴加盐酸,产生无色的气体”可知:
①原溶液中可能存在的离子有
A.NO
 、Fe2+ B.HCO
、Fe2+ B.HCO 、Fe2+ C.HCO
、Fe2+ C.HCO 、Na+、Ba2+ D.CO
、Na+、Ba2+ D.CO 、Fe2+、Na+、Ba2+
、Fe2+、Na+、Ba2+②无色的气体可能是
③请配平离子方程式Fe2++NO
 +H+→Fe3++NO↑+H2O:
+H+→Fe3++NO↑+H2O:(3)若原溶液为绿色,则原溶液中一定存在的离子为
(4)往生成的沉淀a中加入稀盐酸,若有无色气体产生,此时发生反应的离子方程式为
您最近一年使用:0次
2023-11-04更新
|
93次组卷
|
2卷引用:山西省临汾市尧都区尧庙镇尧庙中学等2023-2024学年高一上学期10月月考化学试题
7 . 某小组在验证反应“ ”,实验探究过程如下。结合探究过程回答下列问题。
”,实验探究过程如下。结合探究过程回答下列问题。
向硝酸酸化的 硝酸银溶液中(忽略
硝酸银溶液中(忽略 的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
(1)检测到滤液中含有 ,可以选用的试剂为
,可以选用的试剂为___________ (填化学式)溶液。 产生的原因可能有以下几种。
产生的原因可能有以下几种。
假设a:可能是铁粉表面有氧化层,能产生 。
。
假设b:空气中存在 ,
, 被氧化为
被氧化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
假设c:酸性溶液中的 具有氧化性,可产生
具有氧化性,可产生 。
。
(2)某同学证明上面假设c不成立,向硝酸酸化的___________ 硝酸钠溶液中加入过量铁粉,搅拌后静置,一段时间后,上层清液未变黄色,经检验无 。
。
(3)取过滤后的黑色固体,洗涤后,___________ (填操作和现象),证明黑色固体中含有Ag。
(4)某同学利用原电池证明 可以将
可以将 氧化为
氧化为 ,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除
,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除 )。甲溶液中的溶质为
)。甲溶液中的溶质为___________ 。写出石墨电极上发生的电极反应式:___________ 。电流表指针不再偏转后,向左侧烧杯中加入 固体,发现电流表指针反向偏转,此时石墨电极为
固体,发现电流表指针反向偏转,此时石墨电极为___________ (填“正极”或“负极”),银电极的电极反应式为___________ 。
 ”,实验探究过程如下。结合探究过程回答下列问题。
”,实验探究过程如下。结合探究过程回答下列问题。向硝酸酸化的
 硝酸银溶液中(忽略
硝酸银溶液中(忽略 的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。(1)检测到滤液中含有
 ,可以选用的试剂为
,可以选用的试剂为 产生的原因可能有以下几种。
产生的原因可能有以下几种。假设a:可能是铁粉表面有氧化层,能产生
 。
。假设b:空气中存在
 ,
, 被氧化为
被氧化为 ,写出反应的离子方程式:
,写出反应的离子方程式:假设c:酸性溶液中的
 具有氧化性,可产生
具有氧化性,可产生 。
。(2)某同学证明上面假设c不成立,向硝酸酸化的
 。
。(3)取过滤后的黑色固体,洗涤后,
(4)某同学利用原电池证明
 可以将
可以将 氧化为
氧化为 ,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除
,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除 )。甲溶液中的溶质为
)。甲溶液中的溶质为 固体,发现电流表指针反向偏转,此时石墨电极为
固体,发现电流表指针反向偏转,此时石墨电极为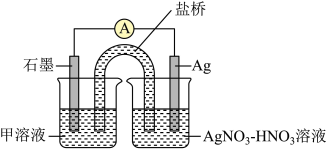
您最近一年使用:0次
2023-10-26更新
|
639次组卷
|
7卷引用:山西省部分学校2023-2024学年高三上学期10月月考(一轮复习联考(二))化学试题
名校
8 . 我国学者制备了一种介孔二氧化锰负载的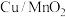 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是

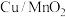 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
| A.BZA中既含有极性键又含有非极性键 |
B.反应中氧化剂为 ,氧化产物为 ,氧化产物为 和 和 |
C.直接降解BZA的活性氧物种的化学式为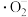 和 和 |
D.据机理图可知氧化性: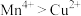 |
您最近一年使用:0次
2023-10-25更新
|
145次组卷
|
2卷引用:山西太原市成成中学校2023-2024学年高三上学期12月月考化学试题
解题方法
9 . 以辉铜矿(主要成分是 Cu2S。含少量 FeS2、FeS、SiO2等)为原料制备胆矾、硫代硫酸钠(Na2S2O3·5H2O)。流程如图所示。 回答下列问题:
(1)焙烧时,粉碎矿石的目的是___________ ;滤渣2的主要成分是___________ (填化学式)。
(2)向Na2S和 Na2CO3的混合溶液中通入SO2制备硫代硫酸钠的化学方程式为___________ 。
(3)某小组探究外界条件对 Na2S2O3相关反应的反应速率的影响,实验方案如下:
已知:① (慢),②
(慢),② (快)。
(快)。
上述反应中,活化能较大的反应是___________ (填“①”或“②”)。下列叙述错误的是___________ (填标号)。
A.在KI-淀粉溶液中滴加过量 Na2S2O3溶液,溶液始终不会变蓝
B.上述方案可以探究浓度对反应速率的影响
C.当n(Na2S2O3):n(K2S2O8)的值小于2时会出现蓝色
(4)检验溶液2中含 Fe2+的试剂可能是___________(填标号)。
(5)25.0 g CuSO4·5H2O受热分解。残留固体的质量与温度的关系如图所示。___________ (填化学式)。
②已知580~1000℃之间产生了两种气体和一种固体,写出发生反应的化学方程式:___________ 。
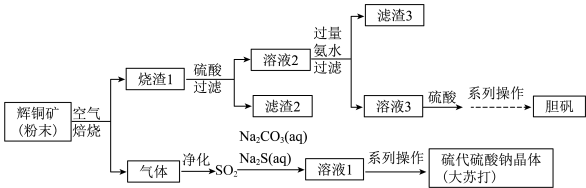
(1)焙烧时,粉碎矿石的目的是
(2)向Na2S和 Na2CO3的混合溶液中通入SO2制备硫代硫酸钠的化学方程式为
(3)某小组探究外界条件对 Na2S2O3相关反应的反应速率的影响,实验方案如下:
已知:①
 (慢),②
(慢),② (快)。
(快)。| 体积/mL | ||||
| 实验序号 | K2S2O8溶液 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 |
| 1 | 10.0 | 4.0 | 5.0 | 2.0 |
| 2 | 5.0 | 4.0 | 5.0 | 2.0 |
A.在KI-淀粉溶液中滴加过量 Na2S2O3溶液,溶液始终不会变蓝
B.上述方案可以探究浓度对反应速率的影响
C.当n(Na2S2O3):n(K2S2O8)的值小于2时会出现蓝色
(4)检验溶液2中含 Fe2+的试剂可能是___________(填标号)。
| A.KSCN溶液 | B.K3Fe(CN)6溶液 | C.酸性 KMnO4溶液 | D.NaOH 溶液 |

②已知580~1000℃之间产生了两种气体和一种固体,写出发生反应的化学方程式:
您最近一年使用:0次
2023-10-17更新
|
428次组卷
|
3卷引用:2024届山西省部分学校高三上学期11月联合考试模拟预测化学试题
2024届山西省部分学校高三上学期11月联合考试模拟预测化学试题云南省部分名校2023-2024学年高三上学期10月联考理科综合化学试题(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
解题方法
10 . 宏观辨识与微观探析是化学学科核心素养之一、根据所学知识,回答下列问题:
(1)拟卤离子主要有 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
①已知还原性;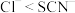 ,写出酸性条件下加热时,
,写出酸性条件下加热时, 和KSCN(aq)反应的离子方程式:
和KSCN(aq)反应的离子方程式:___________ 。
② 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为___________ 。氰化提金工艺在黄金生产领域仍占主导地位,但会产生大量含氰( )废水,含氰废水中加入足量的
)废水,含氰废水中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为 。理论上处理含氰废水(含
。理论上处理含氰废水(含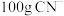 ),需要消耗
),需要消耗___________ g (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:
(保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:___________ 。
(2)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成 。写出该反应的离子方程式:
。写出该反应的离子方程式:___________ ;在该反应中还原剂是___________ (填化学式)。氧化23g乙醇时转移电子的物质的量为___________ 。
(3) 和
和 都属于离子型化合物,前者跟水反应生成
都属于离子型化合物,前者跟水反应生成 和
和 ,写出
,写出 跟水反应的化学方程式:
跟水反应的化学方程式:___________ 。
(1)拟卤离子主要有
 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。①已知还原性;
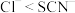 ,写出酸性条件下加热时,
,写出酸性条件下加热时, 和KSCN(aq)反应的离子方程式:
和KSCN(aq)反应的离子方程式:②
 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为 )废水,含氰废水中加入足量的
)废水,含氰废水中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为 。理论上处理含氰废水(含
。理论上处理含氰废水(含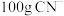 ),需要消耗
),需要消耗 (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:
(保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:(2)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成
 。写出该反应的离子方程式:
。写出该反应的离子方程式:(3)
 和
和 都属于离子型化合物,前者跟水反应生成
都属于离子型化合物,前者跟水反应生成 和
和 ,写出
,写出 跟水反应的化学方程式:
跟水反应的化学方程式:
您最近一年使用:0次
2023-10-08更新
|
152次组卷
|
3卷引用:山西省名校2023-2024学年高三上学期10月联考化学试题



