1 . 以废钒电池负极电解液(主要化学成分是V3+、V2+、H2SO4) 为原料,回收其中的钒制备V2O5的工艺流程如图所示:
回答下列问题:
(1)在“氧化”中低价态钒都转化为 ,其中V3+转化反应的离子方程式为
,其中V3+转化反应的离子方程式为___________ ,实际生产中的氧化剂不选择HClO3的原因是___________ 。
(2)“浓缩”至钒溶液质量浓度(折合V2O5质量浓度)为27.3 g·L-1'时,则溶液中c( )=
)=___________ mol·L-1。(结果保留1位小数)
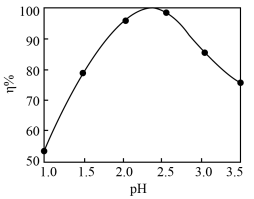
(3)pH对沉钒率(η)的影响如图所示,则沉钒时控制钒液合适的pH范围是___________ ,沉淀产物为2NH4V3O8·H2O,则加(NH4)2SO4沉钒的化学方程式是___________ 。___________ 。检验沉淀已洗涤干净的操作是___________ 。
(5)“煅烧”需要在通风或氧化气氛下进行,其目的是___________ 。
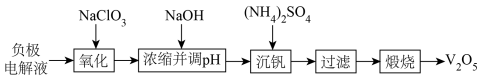
回答下列问题:
(1)在“氧化”中低价态钒都转化为
 ,其中V3+转化反应的离子方程式为
,其中V3+转化反应的离子方程式为(2)“浓缩”至钒溶液质量浓度(折合V2O5质量浓度)为27.3 g·L-1'时,则溶液中c(
 )=
)=(3)pH对沉钒率(η)的影响如图所示,则沉钒时控制钒液合适的pH范围是
(5)“煅烧”需要在通风或氧化气氛下进行,其目的是
您最近一年使用:0次
解题方法
2 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向FeBr2溶液中通入少量的氯气,再滴加少量苯,上层呈橙色 | Fe3+的氧化性比Br2强 |
| B | 室温下,向碳酸氢钠溶液中加入适量盐酸,温度下降 | 碳酸氢钠和盐酸反应吸收热量 |
| C | 将少量BaSO4固体用饱和Na2CO3溶液浸泡,过滤后,向滤渣中加盐酸,滤渣溶解,产生气泡 | 相同温度下,Ksp(BaCO3)<Ksp(BaSO4) |
| D | 向久置的FeSO4溶液加入K3Fe(CN)6溶液,出现蓝色沉淀 | FeSO4没有变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 亚硝酸和硝酸是常见的两种氮的含氧酸,亚硝酸钠(NaNO2)有毒,也有一定氧化性,已知高铁血红蛋白( )无携氧能力。
)无携氧能力。
(1)亚硝酸钠使人体中毒的原因为___________ 。
(2)误食亚硝酸钠可立即服用下列物质中的___________ ,以起到解毒效果。
A.高锰酸钾晶体 B.维生素C C.FeCl3固体
(3)某实验小组模拟用H2O2氧化除去废水中的NO2和NH ,实验数据如下表,消除NH
,实验数据如下表,消除NH 时可能发生的离子反应有
时可能发生的离子反应有___________ 。已知上述反应在该条件下均有较大反应限度,但混合体系中NH 浓度几乎未发生变化的原因是
浓度几乎未发生变化的原因是___________ ,若取1L废水进行实验,则实验2中转移电子的物质的量约为___________ mol。
(4)将6.4g铜片加入100mL9mol/L的硝酸溶液中,铜片完全溶解,并产生标准状况下2.24L气体(气体为NO和NO2的混合气体,不含N2O4),则向反应后的溶液中加入___________ mL浓度为4mol/L的NaOH溶液,可使 恰好完全沉淀。若将产生的气体与足量氧气混合通入水中充分反应,至少需要标准状况下的氧气
恰好完全沉淀。若将产生的气体与足量氧气混合通入水中充分反应,至少需要标准状况下的氧气___________ L。
 )无携氧能力。
)无携氧能力。(1)亚硝酸钠使人体中毒的原因为
(2)误食亚硝酸钠可立即服用下列物质中的
A.高锰酸钾晶体 B.维生素C C.FeCl3固体
(3)某实验小组模拟用H2O2氧化除去废水中的NO2和NH
 ,实验数据如下表,消除NH
,实验数据如下表,消除NH 时可能发生的离子反应有
时可能发生的离子反应有 浓度几乎未发生变化的原因是
浓度几乎未发生变化的原因是| 温度:283K,反应时间:30min | ||||||
| 序号 | 反应前(mg/L) | 反应后(mg/L) | ||||
| [NO2] | [ ] ] | [H2O2] | [NO2] | [ ] ] | 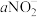 (%) (%) | |
| 1 | 0.000 | 1.00 | 0.66 | 0.000 | 1.00 | 0.0 |
| 2 | 0.100 | 1.00 | 0.66 | 0.048 | 1.00 | 52.0 |
| 3 | 0.100 | 1.00 | 0.00 | 0.100 | 1.00 | 0.0 |
| 4 | 0.500 | 5.00 | 0.00 | 0.498 | 5.00 | 0.4 |
| 5 | 0.500 | 5.00 | 60.0 | 0.200 | 4.98 | 60.0 |
 恰好完全沉淀。若将产生的气体与足量氧气混合通入水中充分反应,至少需要标准状况下的氧气
恰好完全沉淀。若将产生的气体与足量氧气混合通入水中充分反应,至少需要标准状况下的氧气
您最近一年使用:0次
名校
解题方法
4 . 水体中硝酸盐在电催化无害化处理过程中,在催化剂表面,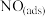 中间体还原为N2的一种反应历程如图(ads指吸附),下列说法错误的是
中间体还原为N2的一种反应历程如图(ads指吸附),下列说法错误的是

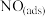 中间体还原为N2的一种反应历程如图(ads指吸附),下列说法错误的是
中间体还原为N2的一种反应历程如图(ads指吸附),下列说法错误的是
A.历程中1molNO还原为N2消耗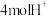 |
| B.历程中4步反应均伴随电子转移 |
C.反应④为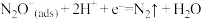 |
| D.该反应历程将化学能转化为电能 |
您最近一年使用:0次
2023-05-27更新
|
561次组卷
|
2卷引用:山西省大同市2022-2023学年高一下学期5月期中考试化学试题
解题方法
5 . 利用NH3吸收液和ClO2可实现煤炭燃烧烟气高效脱硫(SO2)脱硝(NO),吸收处理后得到废液,其成分主要为(NH4)2SO4、NH4NO3、NH4Cl。已知ClO2在碱性条件下会产生 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A.脱除NO的总反应为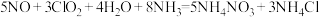 |
| B.标准状况下,脱除含SO2、NO各0.1mol的烟气,至少共需要8.96LNH3 |
| C.每生成1molNH4Cl至少需要1molClO2 |
| D.碱性越强,脱除效率越高 |
您最近一年使用:0次
解题方法
6 . 我国科学家首次实现了CO2直接加氢制取高辛烷值汽油,转化关系如图,下列说法错误的是
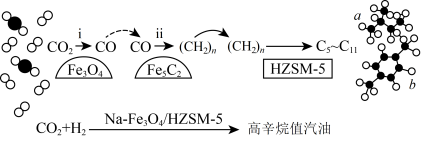

A.反应ⅱ为 |
| B.1molCO2完全转化为 (CH2)n得到4NA个电子 |
| C.a的化学名称为2-甲基丁烷 |
| D.b的一氯取代物有2种结构 |
您最近一年使用:0次
7 . 碲是制作合金添加剂、半导体、制冷元件、光电元件的主体材料,并被广泛应用于冶金、石油、化工、航空航天与电子等领域。铜电解精炼阳极泥碲化铜渣(主要成分为Cu2Te,还含有金、铂等金属)提取碲的工艺流程如图所示,回答下列问题:

已知:TeO2难溶于水;亚碲酸钠易溶于水;高碲酸钠的化学式:Na2TeO4。
(1)酸浸焙烧前要将碲化铜渣粉碎,目的是___________ 。
(2)滤液i的主要成分:___________ (写物质名称)。
(3)焙烧过程中涉及的化学方程式:___________ 。
(4)碱浸的目的是___________ 。
(5)用H2SO3“酸溶还原沉碲”,写出离子方程式:___________ 。
(6)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为_______________ ,设ZnTe的摩尔质量为M,阿伏加德罗常数的值为NA,密度为dg/cm3,则Zn与Te最近距离为___________ nm。
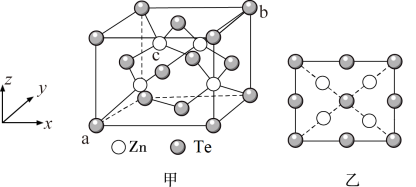

已知:TeO2难溶于水;亚碲酸钠易溶于水;高碲酸钠的化学式:Na2TeO4。
(1)酸浸焙烧前要将碲化铜渣粉碎,目的是
(2)滤液i的主要成分:
(3)焙烧过程中涉及的化学方程式:
(4)碱浸的目的是
(5)用H2SO3“酸溶还原沉碲”,写出离子方程式:
(6)将碲与锌一起加热,然后升华可制得碲化锌。碲化锌是一种重要的半导体材料,图甲为它的一种立方晶胞结构,图乙为该晶胞沿z轴投影图。已知a点的坐标为(0,0,0),b点的坐标为(1,1,1),则c点的坐标为

您最近一年使用:0次
名校
解题方法
8 . 根据下列事实得出的相应结论错误的是
| 选项 | 事实 | 结论 |
| A | 25℃时分别测定浓度均为0.1mol·L-1的NaCl溶液和CH3COONH4溶液的pH,pH都等于7 | 两溶液中水的电离程度相等 |
| B | t ℃时,反应①:Br2(g)+ H2(g)  2HBr(g) K=5. 6×107;反应②:I2(g)+ H2(g) 2HBr(g) K=5. 6×107;反应②:I2(g)+ H2(g)  2HI(g) K=43 2HI(g) K=43 | 相同条件下。平衡体系中卤化氢所占的比例:反应①>反应② |
| C | 向漂白粉溶液中通入足量SO2气体,产生白色沉淀 | 还原性:SO2>Cl- |
| D | 常温下,将50mL苯与50mLCH3COOH混合,所得混合液的体积为101 mL | 混合过程中削弱了CH3COOH分子间的氢键。且苯与CH3COOH分子间的范德华力弱于CH3COOH分子间的氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-22更新
|
92次组卷
|
2卷引用:山西省大同市2023届高三下学期三模理科综合化学试题
9 . 稀土金属元素钪在国防、航天、核能等领域具有重要应用。从某工业废料“赤泥”(含有Fe2O3、Fe3O4、Al2O3、SiO2、Sc2O3、TiO2等)中回收Sc2O3的工艺流程如下:

已知:该条件下,Ksp[Fe(OH)3]=1.0×10−38,Ksp[Al(OH)3]=1.0×10−33,Kw=1.0×10−14。
请回答下列问题:
(1)稀土元素Y为第五周期Sc的同族元素,基态Y原子的d能级和s能级电子个数比为___________ 。
(2)“滤渣”的成分为TiO2和________ (填化学式,下同)。
(3)“氢氧化物沉淀”的成分为________ ;为使杂质离子沉淀完全,“调pH”范围应调节为_______ ~6之间。
(4)“氧化”时反应离子方程式为___________ 。
(5)“沉钪”时,将K2CO3固体加入草酸(H2C2O4)溶液[配料比n(K2CO3):n(H2C2O4)=2:3],制得KHC2O4和K2C2O4混合溶液。K2CO3需分批缓慢加入的原因是_______ ;发生反应的离子方程式为______ 。
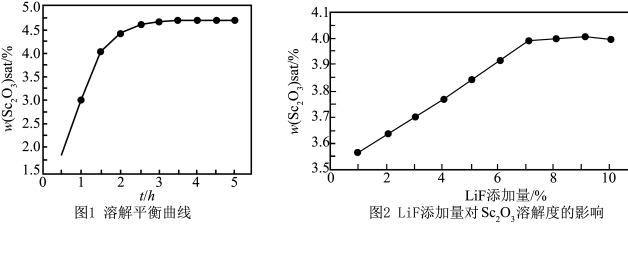
(6)Al-Sc合金是新一代航天结构材料,制备该合金的熔盐电解法涉及原料Sc2O3在熔盐体系中的溶解问题。950℃下部分条件对Sc2O3的溶解影响如图1、图2所示,则应采取的最佳溶解时间和LiF添加量分别为___________ 。

已知:该条件下,Ksp[Fe(OH)3]=1.0×10−38,Ksp[Al(OH)3]=1.0×10−33,Kw=1.0×10−14。
请回答下列问题:
(1)稀土元素Y为第五周期Sc的同族元素,基态Y原子的d能级和s能级电子个数比为
(2)“滤渣”的成分为TiO2和
(3)“氢氧化物沉淀”的成分为
(4)“氧化”时反应离子方程式为
(5)“沉钪”时,将K2CO3固体加入草酸(H2C2O4)溶液[配料比n(K2CO3):n(H2C2O4)=2:3],制得KHC2O4和K2C2O4混合溶液。K2CO3需分批缓慢加入的原因是
(6)Al-Sc合金是新一代航天结构材料,制备该合金的熔盐电解法涉及原料Sc2O3在熔盐体系中的溶解问题。950℃下部分条件对Sc2O3的溶解影响如图1、图2所示,则应采取的最佳溶解时间和LiF添加量分别为

您最近一年使用:0次
10 . 下列各组实验中,可以由操作,现象得出相应结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向KI溶液中滴加硝酸酸化的Fe(NO3)3溶液,再加CCl4振荡静置 | 下层溶液呈紫色 | 氧化性:Fe3+>I2 |
| B | 将乙醇与浓硫酸以体积比1:3混合,迅速加热到170°C,再将产生的气体通过溴水 | 溴水褪色 | 乙醇发生消去反应生成乙烯 |
| C | 在干冰中央挖一个小穴,撒一些镁粉,用红热的铁棒把镁引燃,盖上另一块干冰 | 镁粉在干冰中继续燃烧,发出耀眼的白光 | CO2不能扑灭金属镁引起的火灾 |
| D | 向碳酸钠溶液中加入盐酸,将反应产生的气体通入苯酚钠溶液 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



