名校
1 . 我国学者制备了一种介孔二氧化锰负载的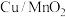 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是

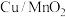 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
| A.BZA中既含有极性键又含有非极性键 |
B.反应中氧化剂为 ,氧化产物为 ,氧化产物为 和 和 |
C.直接降解BZA的活性氧物种的化学式为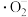 和 和 |
D.据机理图可知氧化性: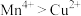 |
您最近一年使用:0次
2023-10-25更新
|
124次组卷
|
2卷引用:山西太原市成成中学校2023-2024学年高三上学期12月月考化学试题
解题方法
2 . 宏观辨识与微观探析是化学学科核心素养之一、根据所学知识,回答下列问题:
(1)拟卤离子主要有 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
①已知还原性;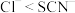 ,写出酸性条件下加热时,
,写出酸性条件下加热时, 和KSCN(aq)反应的离子方程式:
和KSCN(aq)反应的离子方程式:___________ 。
② 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为___________ 。氰化提金工艺在黄金生产领域仍占主导地位,但会产生大量含氰( )废水,含氰废水中加入足量的
)废水,含氰废水中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为 。理论上处理含氰废水(含
。理论上处理含氰废水(含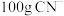 ),需要消耗
),需要消耗___________ g (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:
(保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:___________ 。
(2)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成 。写出该反应的离子方程式:
。写出该反应的离子方程式:___________ ;在该反应中还原剂是___________ (填化学式)。氧化23g乙醇时转移电子的物质的量为___________ 。
(3) 和
和 都属于离子型化合物,前者跟水反应生成
都属于离子型化合物,前者跟水反应生成 和
和 ,写出
,写出 跟水反应的化学方程式:
跟水反应的化学方程式:___________ 。
(1)拟卤离子主要有
 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。①已知还原性;
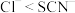 ,写出酸性条件下加热时,
,写出酸性条件下加热时, 和KSCN(aq)反应的离子方程式:
和KSCN(aq)反应的离子方程式:②
 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为 )废水,含氰废水中加入足量的
)废水,含氰废水中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为 。理论上处理含氰废水(含
。理论上处理含氰废水(含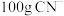 ),需要消耗
),需要消耗 (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:
(保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:(2)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成
 。写出该反应的离子方程式:
。写出该反应的离子方程式:(3)
 和
和 都属于离子型化合物,前者跟水反应生成
都属于离子型化合物,前者跟水反应生成 和
和 ,写出
,写出 跟水反应的化学方程式:
跟水反应的化学方程式:
您最近一年使用:0次
2023-10-08更新
|
145次组卷
|
3卷引用:山西省名校2023-2024学年高三上学期10月联考化学试题
3 . 周期表中第VA族元素的化合物应用广泛。下列化学反应表示错误的是
A.亚硝酸钠可被酸性 溶液氧化: 溶液氧化: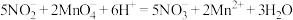 |
B.制备砷化镓晶体: |
C.磷矿石与浓硫酸反应制磷肥[有效成分为 ]: ]: |
D.肼( )—空气碱性燃料电池的负极反应: )—空气碱性燃料电池的负极反应: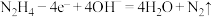 |
您最近一年使用:0次
2023-10-08更新
|
105次组卷
|
2卷引用:山西省名校2023-2024学年高三上学期10月联考化学试题
解题方法
4 . 由硫铁矿烧渣(主要成分为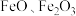 ,还含有少量
,还含有少量 )制备绿矾(
)制备绿矾( ,高温易分解)的工艺流程如图所示。
,高温易分解)的工艺流程如图所示。
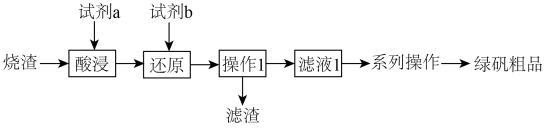
回答下列问题:
(1)“酸浸”时,将烧渣研细的目的为_____ ;试剂 是
是_____ (填“稀盐酸”“稀硫酸”或“稀硝酸”)。
(2)试剂b如果是 ,写出“还原”时发生反应的离子方程式:
,写出“还原”时发生反应的离子方程式:_____ 。
(3)“操作1”中使用的玻璃仪器是漏斗、_____ ;试剂 为
为 时,滤渣的主要成分为
时,滤渣的主要成分为_____ (填化学式)。
(4)“系列操作”的最后一步为减压烘干,其目的是_____ 。
(5)为了测定绿矾粗品的纯度,某实验小组采用以下方案。量取 绿矾粗品,配成
绿矾粗品,配成 溶液,取出
溶液,取出 溶液用
溶液用 的酸性
的酸性 标准液进行滴定,达到滴定终点时消耗
标准液进行滴定,达到滴定终点时消耗 酸性
酸性 标准液(已知滴定过程中
标准液(已知滴定过程中 被还原为
被还原为 )。
)。
①滴定管选择正确且操作规范的是_____ (填字母)。
②滴定到终点时的现象是_____ 。
③绿矾粗品的纯度为_____  (保留三位有效数字)。
(保留三位有效数字)。
A. B.
B.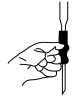 C.
C.
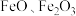 ,还含有少量
,还含有少量 )制备绿矾(
)制备绿矾( ,高温易分解)的工艺流程如图所示。
,高温易分解)的工艺流程如图所示。
回答下列问题:
(1)“酸浸”时,将烧渣研细的目的为
 是
是(2)试剂b如果是
 ,写出“还原”时发生反应的离子方程式:
,写出“还原”时发生反应的离子方程式:(3)“操作1”中使用的玻璃仪器是漏斗、
 为
为 时,滤渣的主要成分为
时,滤渣的主要成分为(4)“系列操作”的最后一步为减压烘干,其目的是
(5)为了测定绿矾粗品的纯度,某实验小组采用以下方案。量取
 绿矾粗品,配成
绿矾粗品,配成 溶液,取出
溶液,取出 溶液用
溶液用 的酸性
的酸性 标准液进行滴定,达到滴定终点时消耗
标准液进行滴定,达到滴定终点时消耗 酸性
酸性 标准液(已知滴定过程中
标准液(已知滴定过程中 被还原为
被还原为 )。
)。①滴定管选择正确且操作规范的是
②滴定到终点时的现象是
③绿矾粗品的纯度为
 (保留三位有效数字)。
(保留三位有效数字)。A.
 B.
B. C.
C.
您最近一年使用:0次
2023-10-02更新
|
93次组卷
|
2卷引用:山西省部分学校2023-2024学年高三第一联考(月考)化学试题
解题方法
5 . 回答下列问题。
(1)用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为10)中SO 将NO2转化为NO
将NO2转化为NO ,其离子方程式为
,其离子方程式为___________ 。
(2)高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:

“平炉”中发生的化学方程式为___________ 。
(3)某地污水中的有机污染物主要成分是三氯乙烯CHCl=CCl2向此污水中加入KMnO4高锰酸钾被还原为MnO2溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式:___________ 。
(4)Na2S2O3还原性较强,在溶液中易被Cl2氧化成 SO ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为___________ 。
(5)+6价铬的化合物毒性较大,常用NaHSO3将废液中的 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为___________ 。
(6)FeO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是___________ 。
(1)用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为10)中SO
 将NO2转化为NO
将NO2转化为NO ,其离子方程式为
,其离子方程式为(2)高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:

“平炉”中发生的化学方程式为
(3)某地污水中的有机污染物主要成分是三氯乙烯CHCl=CCl2向此污水中加入KMnO4高锰酸钾被还原为MnO2溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式:
(4)Na2S2O3还原性较强,在溶液中易被Cl2氧化成 SO
 ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为(5)+6价铬的化合物毒性较大,常用NaHSO3将废液中的
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为(6)FeO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近一年使用:0次
名校
6 . 回答下列问题:
(1)关于甲、乙、丙、丁四套装置的说法正确的是_______ 。

(2)以下物质(或粒子)与其用途之间关联正确的是_______ 。
(3)实验室制取Cl2的化学方程式:_______ 。浓盐酸表现的性质是_______ 。
(4)已知:在稀硫酸中,MnO 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。_______
(1)关于甲、乙、丙、丁四套装置的说法正确的是

| A.用装置甲制取氯气 | B.用丙装置可以较长时间看到白色Fe(OH)2白色沉淀 |
| C.用丁装置证明碳酸氢钠受热易分解 | D.用装置乙除去氢气中的少量氯化氢 |
| A.硬铝——制导线 | B.14C——测定文物年代 |
| C.锗——作半导体材料 | D.Ti-Fe合金——作不锈钢材料 |
(4)已知:在稀硫酸中,MnO
 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
您最近一年使用:0次
2023-09-24更新
|
325次组卷
|
4卷引用:山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)
山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题07 铁及其化合物 金属材料-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)(已下线)专项02 氧化还原反应的概念、规律及综合应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)
解题方法
7 . 硒被誉为“生命的火种”。亚硒酸钙(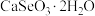 ,难溶于水)常作饲料添加剂,
,难溶于水)常作饲料添加剂, 常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:

已知部分信息如下:
①含硒废料的主要成分是 和
和 ,“焙烧”中固体产物为
,“焙烧”中固体产物为 、
、 和
和 ;
;
② 易溶于水,
易溶于水, 难溶于水。
难溶于水。
(1)“焙烧”时常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部加入,这样操作的目的是___________ 。“焙烧”中被氧化的元素有___________ (填元素符号)。
(2)“浸渣”的主要成分是___________ (填化学式)。
(3)“沉硒”的化学方程式为___________ 。
(4)洗涤产品时,测定洗涤液pH,当pH为7时可认为产品已洗净,其原理是___________ 。
(5)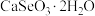 热失重时质量与温度的关系如图所示。
热失重时质量与温度的关系如图所示。

380℃时固体的成分是___________ (填化学式)。
(6)测定 产品纯度。
产品纯度。
称取wg产品溶于水,加入足量 溶液和适量稀硝酸,充分反应后,用
溶液和适量稀硝酸,充分反应后,用 溶液滴定至终点,消耗VmL滴定液。
溶液滴定至终点,消耗VmL滴定液。
发生反应:①
②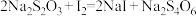
在下列试剂中,宜选择的指示剂为___________ (填标号)。
A. 溶液 B.
溶液 B. 淀粉溶液
淀粉溶液
C. 酚酞溶液 D.
酚酞溶液 D. 甲基橙溶液
甲基橙溶液
该产品中 的质量分数为
的质量分数为___________ %。
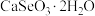 ,难溶于水)常作饲料添加剂,
,难溶于水)常作饲料添加剂, 常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
已知部分信息如下:
①含硒废料的主要成分是
 和
和 ,“焙烧”中固体产物为
,“焙烧”中固体产物为 、
、 和
和 ;
;②
 易溶于水,
易溶于水, 难溶于水。
难溶于水。(1)“焙烧”时常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部加入,这样操作的目的是
(2)“浸渣”的主要成分是
(3)“沉硒”的化学方程式为
(4)洗涤产品时,测定洗涤液pH,当pH为7时可认为产品已洗净,其原理是
(5)
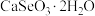 热失重时质量与温度的关系如图所示。
热失重时质量与温度的关系如图所示。
380℃时固体的成分是
(6)测定
 产品纯度。
产品纯度。称取wg产品溶于水,加入足量
 溶液和适量稀硝酸,充分反应后,用
溶液和适量稀硝酸,充分反应后,用 溶液滴定至终点,消耗VmL滴定液。
溶液滴定至终点,消耗VmL滴定液。发生反应:①

②
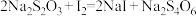
在下列试剂中,宜选择的指示剂为
A.
 溶液 B.
溶液 B. 淀粉溶液
淀粉溶液C.
 酚酞溶液 D.
酚酞溶液 D. 甲基橙溶液
甲基橙溶液该产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
8 . 化学和生活、社会发展息息相关。下列说法正确的组合是
①飞船返回舱表层材料中的玻璃纤维属于天然有机高分子材料
②液化石油气、汽油、煤油、柴油的主要成分都是烃
③工业上通过石油分馏得到大量化工原料苯
④活性炭疏松多孔,可用于除异味和杀菌
⑤维生素C是NaNO2中毒的急救药之一,利用了维生素C的氧化性
⑥“光化学烟雾”“臭氧空洞”“硝酸型酸雨”的形成都与氮氧化物有关
⑦用四氯乙烯干洗剂除去衣服上油污,发生的是物理变化
⑧波尔多液(硫酸铜、石灰和水配成)用作农药,利用Cu2+使病毒蛋白变性
⑨漂白粉与盐酸可混合使用以提高漂白效果
①飞船返回舱表层材料中的玻璃纤维属于天然有机高分子材料
②液化石油气、汽油、煤油、柴油的主要成分都是烃
③工业上通过石油分馏得到大量化工原料苯
④活性炭疏松多孔,可用于除异味和杀菌
⑤维生素C是NaNO2中毒的急救药之一,利用了维生素C的氧化性
⑥“光化学烟雾”“臭氧空洞”“硝酸型酸雨”的形成都与氮氧化物有关
⑦用四氯乙烯干洗剂除去衣服上油污,发生的是物理变化
⑧波尔多液(硫酸铜、石灰和水配成)用作农药,利用Cu2+使病毒蛋白变性
⑨漂白粉与盐酸可混合使用以提高漂白效果
| A.②⑤⑦⑨ | B.②⑥⑦⑧ | C.③④⑥⑧ | D.①③④⑤ |
您最近一年使用:0次
2023-09-10更新
|
260次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三上学期10月月考化学试题
名校
解题方法
9 . 如果用亚硫酸钠溶液恰好能将强氧化剂[RO(OH)2]2+还原到较低价态。若亚硫酸钠和[RO(OH)2]2+的反应比例为3:2,则反应后R的价态为
| A.0价 | B.+1价 | C.+2价 | D.+3价 |
您最近一年使用:0次
2023-08-31更新
|
199次组卷
|
2卷引用:山西省太原市小店区第一中学校2023-2024学年高一上学期10月月考化学试题
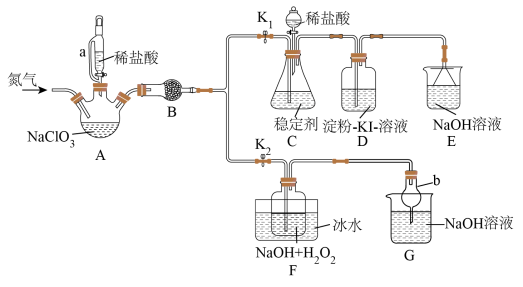
10 . 二氧化氯( )是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放
)是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放 ,并探究其性质。(已知
,并探究其性质。(已知 ,实验室可用稳定剂吸收
,实验室可用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体)。
一种气体)。
已知:① 沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;
沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;
② 饱和溶液低于38℃时析出
饱和溶液低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 ,高于60℃时
,高于60℃时 分解为
分解为 和NaCl。回答下列问题:
和NaCl。回答下列问题:
(1)仪器a的名称是______ ;仪器b的作用是______ 。
(2)按图组装好仪器后,首先应该进行的操作是______ ,实验过程中需持续通入一定量的氮气,其目的是将装置A产生的气体赶入吸收装置被充分吸收,还有______ 。
(3)打开仪器a的活塞,装置A中发生反应,生成 、
、 、NaCl等,写出装置A中发生反应的化学方程式:
、NaCl等,写出装置A中发生反应的化学方程式:_____________ ,关闭仪器a的活塞, 在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是
在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是__________________ 。
(4)向装置C中滴加稀盐酸,反应剧烈,若将稀盐酸换成等pH的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因可能是____________ 。
(5)装置F的目的是制备 ,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为
,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为______ ,从装置F广口瓶内的溶液中获得晶体 的操作步骤是蒸发浓缩、
的操作步骤是蒸发浓缩、______ 、洗涤、干燥。
(6)城市饮用水处理新技术用 替代
替代 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率(
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率( ),那么消毒杀菌剂消毒效率:
),那么消毒杀菌剂消毒效率:
______ 。
 )是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放
)是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放 ,并探究其性质。(已知
,并探究其性质。(已知 ,实验室可用稳定剂吸收
,实验室可用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体)。
一种气体)。
已知:①
 沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;
沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;②
 饱和溶液低于38℃时析出
饱和溶液低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 ,高于60℃时
,高于60℃时 分解为
分解为 和NaCl。回答下列问题:
和NaCl。回答下列问题:(1)仪器a的名称是
(2)按图组装好仪器后,首先应该进行的操作是
(3)打开仪器a的活塞,装置A中发生反应,生成
 、
、 、NaCl等,写出装置A中发生反应的化学方程式:
、NaCl等,写出装置A中发生反应的化学方程式: 在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是
在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是(4)向装置C中滴加稀盐酸,反应剧烈,若将稀盐酸换成等pH的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因可能是
(5)装置F的目的是制备
 ,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为
,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为 的操作步骤是蒸发浓缩、
的操作步骤是蒸发浓缩、(6)城市饮用水处理新技术用
 替代
替代 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率(
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率( ),那么消毒杀菌剂消毒效率:
),那么消毒杀菌剂消毒效率:
您最近一年使用:0次
2023-08-31更新
|
142次组卷
|
3卷引用:山西省大同市2023-2024学年高三上学期开学质量检测化学试题



