解题方法
1 . 中华文明博大精深,源远流长。下列说法错误的是
| A.宣纸是我国传统的书画用纸,用青檀和稻草生产宣纸涉及化学变化 |
| B.《神农本草经》中记载“石硫磺能化金银铜铁”,该过程发生化合反应 |
| C.“千淘万漉虽辛苦,吹尽黄沙始到金”中的淘金原理与化学上的萃取一致 |
| D.“百炼成钢”,反复烧红的生铁在空气中不断锤打可以制得钢,该过程中发生氧化还原反应 |
您最近一年使用:0次
2 . 城市污水中含有一定量的 、
、 ,向污水中加入菌体和
,向污水中加入菌体和 溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现
溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现 、
、 的脱除,其过程如图所示。下列说法正确的是
的脱除,其过程如图所示。下列说法正确的是
 、
、 ,向污水中加入菌体和
,向污水中加入菌体和 溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现
溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现 、
、 的脱除,其过程如图所示。下列说法正确的是
的脱除,其过程如图所示。下列说法正确的是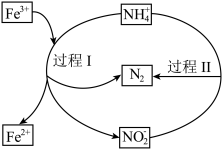
A.“过程Ⅰ”中 为催化剂 为催化剂 |
B. 的氧化性强于 的氧化性强于 |
C.“过程Ⅱ”中氧化产物和还原产物的质量之比为 |
D.“过程Ⅰ”中 和 和 的物质的量之比为 的物质的量之比为 ,则氧化剂与还原剂物质的量之比为 ,则氧化剂与还原剂物质的量之比为 |
您最近一年使用:0次
2023-09-23更新
|
600次组卷
|
10卷引用:黑龙江省双鸭山市第一中学2023-2024学年高三上学期10月月考化学试题
黑龙江省双鸭山市第一中学2023-2024学年高三上学期10月月考化学试题湘豫名校联考2023-2024学年高三上学期一轮诊断化学试题河南省信阳市信阳高级中学2024届高三上学期9月一模化学试题山东省滨州市2023-2024学年高三上学期11月期中考试化学试题(已下线)选择题11-15湖南省湘西州吉首市2024届高三上学期第二届中小学生教师解题大赛化学试题江西省赣州市信丰中学2023-2024学年高一上学期11月月考化学试题河南省南阳市邓州市第一高级中学校2023-2024学年高一上学期期末考试化学试题(已下线)选择题6-10河南省洛阳市宜阳县第一高级中学2023-2024学年高一上学期(研学班)期末考试化学试卷
3 . 随着现代工业发展, 烟气排放量急剧增加。利用气相还原法将
烟气排放量急剧增加。利用气相还原法将 还原为硫黄是目前烟气脱硫研究的热点,原理是在一定温度下(200~300℃)将
还原为硫黄是目前烟气脱硫研究的热点,原理是在一定温度下(200~300℃)将 烟气通过固体还原剂,使
烟气通过固体还原剂,使 中的氧原子转移到固体还原剂上,从而实现
中的氧原子转移到固体还原剂上,从而实现 的还原,其流程如下图所示,下列说法错误的是
的还原,其流程如下图所示,下列说法错误的是

 烟气排放量急剧增加。利用气相还原法将
烟气排放量急剧增加。利用气相还原法将 还原为硫黄是目前烟气脱硫研究的热点,原理是在一定温度下(200~300℃)将
还原为硫黄是目前烟气脱硫研究的热点,原理是在一定温度下(200~300℃)将 烟气通过固体还原剂,使
烟气通过固体还原剂,使 中的氧原子转移到固体还原剂上,从而实现
中的氧原子转移到固体还原剂上,从而实现 的还原,其流程如下图所示,下列说法错误的是
的还原,其流程如下图所示,下列说法错误的是
A.再生塔中,生成的另一种物质的化学式为 |
B.脱硫塔中, 与 与 反应的物质的量之比为 反应的物质的量之比为 |
| C.三个装置中均发生了氧化还原反应 |
D.脱硫过程中,当产生48g单质 时,转移电子的物质的量为3mol 时,转移电子的物质的量为3mol |
您最近一年使用:0次
2023-09-23更新
|
208次组卷
|
3卷引用:黑龙江省双鸭山市第一中学2023-2024学年高三上学期10月月考化学试题
名校
4 . 宏微结合是研究化学的重要方法,从微观的角度了解物质及其变化,有助于更好地认识物质的组成和变化的本质。
I.
(1)下表为部分元素的原子结构示意图:
①表中硫元素的核电荷数x=___________ 。
②R3+离子与氖原子的核外电子排布相同,则R元素为___________ 元素(填元素名称)。
③一个水分子中所含电子总数为___________ 。
④硫元素与氧元素的化学性质相似的原因是___________ 。
(2)甲和乙在一定条件下反应生成丙和丁,反应的微观模型如图所示。

①该反应的生成物中,属于氧化物的是___________ (填化学式)
②每个甲分子是由___________ 构成的。
③参加反应的甲和乙分子个数比为___________ 。
(3)如图是稀硫酸与甲溶液发生复分解反应的微观模型,请写出一种符合图示的a微粒的符号:___________ 。

II.人们在实验研究中总结出常见金属的活动性顺序:

(4)请在表中 内填写对应的元素符号
内填写对应的元素符号___________ 。
(5)Mg、Sn、Pb、Cu、Ag五种金属,能与稀盐酸(或稀硫酸)发生置换反应的金属有___________ 种;写出其中最活泼的金属与稀盐酸反应的化学方程式___________ 。
I.
(1)下表为部分元素的原子结构示意图:
| 元素名称 | 氢 | 氧 | 氟 | 氖 | 钠 | 硫 | 氯 |
| 原子结构示意图 | 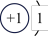 |  | 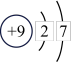 | 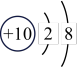 |  | 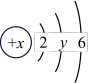 |  |
②R3+离子与氖原子的核外电子排布相同,则R元素为
③一个水分子中所含电子总数为
④硫元素与氧元素的化学性质相似的原因是
(2)甲和乙在一定条件下反应生成丙和丁,反应的微观模型如图所示。

①该反应的生成物中,属于氧化物的是
②每个甲分子是由
③参加反应的甲和乙分子个数比为
(3)如图是稀硫酸与甲溶液发生复分解反应的微观模型,请写出一种符合图示的a微粒的符号:

II.人们在实验研究中总结出常见金属的活动性顺序:

(4)请在表中
 内填写对应的元素符号
内填写对应的元素符号(5)Mg、Sn、Pb、Cu、Ag五种金属,能与稀盐酸(或稀硫酸)发生置换反应的金属有
您最近一年使用:0次
名校
5 . 完成以下离子方程式:
(1)向酸性高锰酸钾溶液中加入草酸溶液_______ 。
(2)向硫酸铝铵溶液中加入过量的氢氧化钡溶液_______ 。
(3)用亚硫酸钠溶液吸收少量氯气_______ 。
(4)泡沫灭火器的工作原理_______ 。
(5)向氯化镁溶液中滴加碳酸钠溶液,生成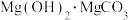
_______ 。
(1)向酸性高锰酸钾溶液中加入草酸溶液
(2)向硫酸铝铵溶液中加入过量的氢氧化钡溶液
(3)用亚硫酸钠溶液吸收少量氯气
(4)泡沫灭火器的工作原理
(5)向氯化镁溶液中滴加碳酸钠溶液,生成
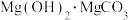
您最近一年使用:0次
2023-09-22更新
|
126次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题
名校
6 . 高铁酸钾(K2FeO4)是一种高效的水处理剂,实验室制备K2FeO4的装置如图所示。(夹持装置略去)
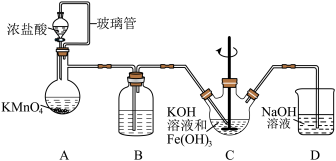
查阅K2FeO4资料如下:①紫色固体,可溶于水、微溶于KOH溶液,不溶于乙醚、醇和氯仿等有机溶剂。②在0~5℃的强碱性溶液中比较稳定。③在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。④KOH溶于醇,微溶于乙醚。
回答下列问题:
(1)装置A为氯气发生装置,KMnO4体现的性质是___________ ,玻璃管的作用是___________ 。
(2)装置B中盛放的试剂是___________ 。
(3)装置C中KOH溶液过量的目的是___________ 。搅拌操作,除了防止因局部溶液碱性减弱,使K2FeO4与水反应产生Fe(OH)3和O2,另外的作用是___________ 。
(4)装置C中生成K2FeO4的离子方程式为___________ 。该反应放热,不利于K2FeO4固体析出,写出一条实验改进措施___________ 。
(5)反应结束后过滤装置C中浊液,得到K2FeO4粗产品,用冷的3 mo·L-1KOH溶液洗涤粗产品后,再用___________ 除水。(填标号)
a.苯 b.浓硫酸 c.异丙醇
(6)装置D的作用是___________ 。

查阅K2FeO4资料如下:①紫色固体,可溶于水、微溶于KOH溶液,不溶于乙醚、醇和氯仿等有机溶剂。②在0~5℃的强碱性溶液中比较稳定。③在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。④KOH溶于醇,微溶于乙醚。
回答下列问题:
(1)装置A为氯气发生装置,KMnO4体现的性质是
(2)装置B中盛放的试剂是
(3)装置C中KOH溶液过量的目的是
(4)装置C中生成K2FeO4的离子方程式为
(5)反应结束后过滤装置C中浊液,得到K2FeO4粗产品,用冷的3 mo·L-1KOH溶液洗涤粗产品后,再用
a.苯 b.浓硫酸 c.异丙醇
(6)装置D的作用是
您最近一年使用:0次
2023-09-07更新
|
583次组卷
|
3卷引用:黑龙江省大庆市2023届高三下学期第二次教学质量检测理科综合化学试题
7 . 工业制备高纯硅的主要过程如下:

下列说法错误的是

下列说法错误的是
| A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
B. 易水解,原料气HCl和 易水解,原料气HCl和 应充分去除水和氧气 应充分去除水和氧气 |
C.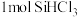 与浓NaOH溶液反应转移电子数为 与浓NaOH溶液反应转移电子数为 |
| D.反应Ⅲ结束,将尾气通入NaOH溶液中,防止空气污染 |
您最近一年使用:0次
2023-09-07更新
|
55次组卷
|
2卷引用:黑龙江省鸡西市密山市2023-2024学年高二上学期9月月考化学试题
名校
8 . 化合物X是一种由三种元素组成的重要化工原料,其相对分子质量小于200,已知B、D含有一种相同的元素且在常温下均为气体化合物,其中气体B可使品红溶液褪色,C可通过单质间的化合反应得到。(部分反应条件省略)请回答:
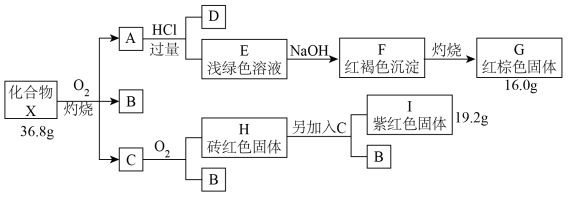
(1)写出X与 反应生成A、B、C的化学方程式
反应生成A、B、C的化学方程式______ 。
(2)检验溶液E中金属阳离子的实验操作是______ 。
(3)B和D两种气体混合发生的反应中,氧化产物与还原产物的质量之比为______ 。
(4)F溶于适量的盐酸中得到J,将5∼6滴J滴入 沸腾的蒸馏水中加热可得到K,区别J和K的方法是
沸腾的蒸馏水中加热可得到K,区别J和K的方法是______ 。
(5)如图中所示,生成 紫红色固体I,吸收
紫红色固体I,吸收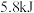 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式______ 。
(6)将固体I溶于 与
与 的混合溶液,向其中滴加
的混合溶液,向其中滴加 的氨水直至沉淀溶解,写出沉淀溶解的离子方程式
的氨水直至沉淀溶解,写出沉淀溶解的离子方程式______ ,再加入 95%的乙醇后得到深蓝色晶体,该晶体的化学式为
95%的乙醇后得到深蓝色晶体,该晶体的化学式为______ 。

(1)写出X与
 反应生成A、B、C的化学方程式
反应生成A、B、C的化学方程式(2)检验溶液E中金属阳离子的实验操作是
(3)B和D两种气体混合发生的反应中,氧化产物与还原产物的质量之比为
(4)F溶于适量的盐酸中得到J,将5∼6滴J滴入
 沸腾的蒸馏水中加热可得到K,区别J和K的方法是
沸腾的蒸馏水中加热可得到K,区别J和K的方法是(5)如图中所示,生成
 紫红色固体I,吸收
紫红色固体I,吸收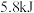 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式(6)将固体I溶于
 与
与 的混合溶液,向其中滴加
的混合溶液,向其中滴加 的氨水直至沉淀溶解,写出沉淀溶解的离子方程式
的氨水直至沉淀溶解,写出沉淀溶解的离子方程式 95%的乙醇后得到深蓝色晶体,该晶体的化学式为
95%的乙醇后得到深蓝色晶体,该晶体的化学式为
您最近一年使用:0次
名校
解题方法
9 . 由 与
与 制备乙醛的反应机理如图所示。下列说法错误的是
制备乙醛的反应机理如图所示。下列说法错误的是
 与
与 制备乙醛的反应机理如图所示。下列说法错误的是
制备乙醛的反应机理如图所示。下列说法错误的是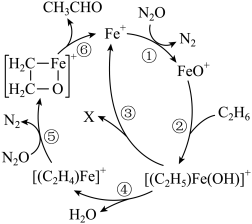
A.每产生1mol  可制得0.5mol 可制得0.5mol  |
B. 为催化剂,X为 为催化剂,X为 |
| C.过程①~⑥中Fe元素呈现的化合价不止一种 |
D.增加 的量,平衡时 的量,平衡时 和 和 的物质的量之比不发生变化 的物质的量之比不发生变化 |
您最近一年使用:0次
2023-07-24更新
|
857次组卷
|
8卷引用:黑龙江省大庆市2023-2024学年高三上学期第一次教学质量检测化学试题
10 . 铝热反应的实验装置如图所示,下列有关说法错误的是


| A.X物质为KClO3 |
| B.镁条燃烧提供引发反应所需的热量 |
| C.若转移0.3 mol电子,被还原的Fe2O3为16 g |
| D.可利用铝热反应冶炼铁 |
您最近一年使用:0次



