名校
解题方法
1 . 物质的氧化性和还原性与溶液 有关,具体可用
有关,具体可用 电势图来表征,电势越大,氧化性越强,铬元素的
电势图来表征,电势越大,氧化性越强,铬元素的 电势图如图所示,下列说法错误的是
电势图如图所示,下列说法错误的是
 有关,具体可用
有关,具体可用 电势图来表征,电势越大,氧化性越强,铬元素的
电势图来表征,电势越大,氧化性越强,铬元素的 电势图如图所示,下列说法错误的是
电势图如图所示,下列说法错误的是
A. 被氧化均生成 被氧化均生成 (Ⅲ) (Ⅲ) |
B. 线的反应为: 线的反应为: |
C. 值越大 值越大 越容易被氧化 越容易被氧化 |
D. 时, 时,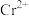 可与 可与 反应生成 反应生成 |
您最近一年使用:0次
名校
解题方法
2 . 以金红石(主要成分为 ,含杂质
,含杂质 等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
 ,含杂质
,含杂质 等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
A.向粉碎后的固体中鼓入 使其“沸腾”有助于充分反应 使其“沸腾”有助于充分反应 |
B.在沸腾氯化炉中, 参加反应转移电子数为 参加反应转移电子数为 |
C.“碳氯化法”得到的 液体中混有杂质 液体中混有杂质 ,可蒸馏分离 ,可蒸馏分离 |
D.可用活泼金属 等在空气中加热还原 等在空气中加热还原 制备 制备 |
您最近一年使用:0次
名校
解题方法
3 . 含SO2和H2S废气的治理可以变废为宝,使硫资源得以利用。
(1)一种处理SO2废气的工艺流程如图所示。_______ ;SO2吸收塔中发生反应化学方程式为_______ 。
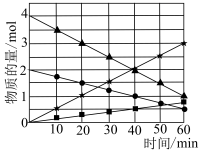
(2)CO与SO2在铝矾土作催化剂、773K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应体系中各组分的物质的量与反应时间的关系如图所示,写出该反应的化学方程式:_______ 。_______ 。
②亚硫酸钠粗品中含有少量Na2SO4,设计实验证明亚硫酸钠粗品中含有少量Na2SO4的方案:_______ 。(必须使用 的试剂有:蒸馏水、稀盐酸、BaCl2溶液)
(4)我国科学家研究在活性炭催化条件下将煤气中的H2S协同脱除,部分反应过程如图所示(·H2S表示H2S气体被吸附在催化剂表面)。_______ 。
②从物质转化与资源综合利用角度分析,该过程初步达到的目的为_______ 。
(1)一种处理SO2废气的工艺流程如图所示。
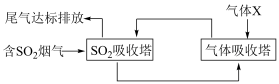
(2)CO与SO2在铝矾土作催化剂、773K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应体系中各组分的物质的量与反应时间的关系如图所示,写出该反应的化学方程式:
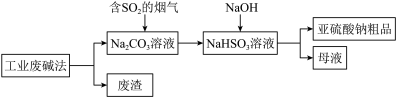
②亚硫酸钠粗品中含有少量Na2SO4,设计实验证明亚硫酸钠粗品中含有少量Na2SO4的方案:
(4)我国科学家研究在活性炭催化条件下将煤气中的H2S协同脱除,部分反应过程如图所示(·H2S表示H2S气体被吸附在催化剂表面)。
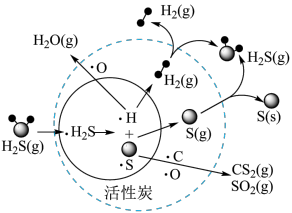
②从物质转化与资源综合利用角度分析,该过程初步达到的目的为
您最近一年使用:0次
2024-02-13更新
|
464次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
4 . 以海带为原料提取碘单质的流程如下:
(1)为提高“水浸”速率,宜采取的措施有:_____________ (任写两种);“氧化1”中 ,不宜过量的原因是
,不宜过量的原因是_____ 。
(2)“过滤”操作需要的玻璃仪器有______ (填仪器名称)。
(3)“吸附”的目的是______ 。
(4)“解吸”中氧化剂、还原剂的物质的量之比为______ 。
(5)“氧化2”中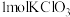 完全反应转移
完全反应转移 电子。与出该反应的离子方程式:
电子。与出该反应的离子方程式:______ 。
(6)利用如图装置提纯碘。
提纯 的原理是
的原理是______ ,棉花防止碘扩散到空气中造成污染。
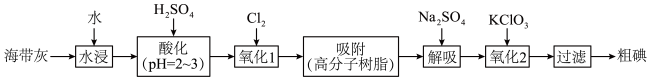
(1)为提高“水浸”速率,宜采取的措施有:
 ,不宜过量的原因是
,不宜过量的原因是(2)“过滤”操作需要的玻璃仪器有
(3)“吸附”的目的是
(4)“解吸”中氧化剂、还原剂的物质的量之比为
(5)“氧化2”中
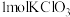 完全反应转移
完全反应转移 电子。与出该反应的离子方程式:
电子。与出该反应的离子方程式:(6)利用如图装置提纯碘。
提纯
 的原理是
的原理是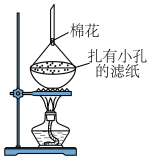
您最近一年使用:0次
2024-01-24更新
|
116次组卷
|
3卷引用:黑龙江省哈尔滨市2023-2024学年高三上学期六校联考化学试题
名校
解题方法
5 . 钼( )及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以
)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
的一种工艺流程如下:
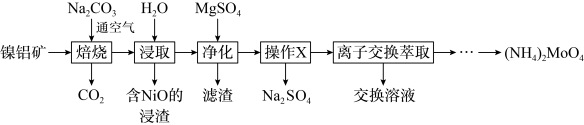
回答下列问题:
(1) 位于元素周期表第
位于元素周期表第_______ 周期第_______ 族。 中钼元素的化合价为
中钼元素的化合价为_______ 。
(2)“焙烧”中生成 的化学方程式为
的化学方程式为_______ 。
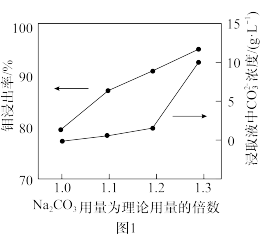
(3) 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中 浓度的影响如图1所示,分析实际生产中选择
浓度的影响如图1所示,分析实际生产中选择 用量为理论用量1.2倍的原因:
用量为理论用量1.2倍的原因:_______ 。
(4) 的溶解度曲线如图2所示,为充分分离
的溶解度曲线如图2所示,为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为_______(填标号)。
”应为_______(填标号)。

(5)为充分利用资源,“离子交换萃取”步骤产生的交换溶液应返回“_______ ”步骤。
(6) 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为
得到金属钼的化学方程式为_______ 。
 )及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以
)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
的一种工艺流程如下:
回答下列问题:
(1)
 位于元素周期表第
位于元素周期表第 中钼元素的化合价为
中钼元素的化合价为(2)“焙烧”中生成
 的化学方程式为
的化学方程式为(3)
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中 浓度的影响如图1所示,分析实际生产中选择
浓度的影响如图1所示,分析实际生产中选择 用量为理论用量1.2倍的原因:
用量为理论用量1.2倍的原因:
(4)
 的溶解度曲线如图2所示,为充分分离
的溶解度曲线如图2所示,为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为_______(填标号)。
”应为_______(填标号)。
| A.蒸发结晶 | B.低温结晶 | C.蒸馏 | D.萃取 |
(5)为充分利用资源,“离子交换萃取”步骤产生的交换溶液应返回“
(6)
 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为
得到金属钼的化学方程式为
您最近一年使用:0次
2024-01-22更新
|
1207次组卷
|
7卷引用:黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题
黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)T16-工业流程题(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)热点23 化学工艺流程综合题(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市丰城市第九中学2023-2024学年高三(复读班)上学期期末考试化学试题
名校
6 . 实验室合成高铁酸钾( )的过程如下图所示。下列说法错误的是
)的过程如下图所示。下列说法错误的是
 )的过程如下图所示。下列说法错误的是
)的过程如下图所示。下列说法错误的是
A.气体a的主要成分为 |
B.沉淀b的主要成分为 |
C. 中 中 的化合价为 的化合价为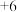 |
D.反应2为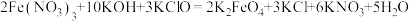 |
您最近一年使用:0次
2024-01-22更新
|
1143次组卷
|
7卷引用:2024年1月“九省联考”黑龙江、吉林卷真题完全解读与考后提升
(已下线)2024年1月“九省联考”黑龙江、吉林卷真题完全解读与考后提升2024年1月吉林、黑龙江普通高等学校招生考试适应性测试化学试题(已下线)选择题11-15河南省信阳高级中学2023-2024学年高一下学期开学化学试题河南省郑州市宇华实验学校2023-2024学年高二下学期开学考试化学试题湖南省长沙市雅礼中学2023-2024学年高三下学期月考(八)化学试题(已下线)专题1 物质及其变化-氧化还原反应方程式的配平与计算
7 . 现有下列物质(括号内为对应物质的主要成分):a.熔融NaOH;b.医用酒精;c.蔗糖晶体;d.加碘盐(NaCl和KIO3);e.“84”消毒液(NaClO);f.小苏打(NaHCO3);g.洁厕灵(HCl),回答下列问题:
(1)上述状态下的物质中,属于电解质且能导电的是_______ (填字母,下同);d和f均为厨房中的常用物质,可用于区分两者的物质是________ 。
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:________ 。
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:___________ ;该反应中被氧化的Ⅰ原子与被还原的Ⅰ原子的个数之比为___________ 。
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:_____ ,__NaClO2+__NaHSO4=___ClO2+___NaCl+__Na2SO4+____H2O;若每片泡腾片中NaClO2的质量分数≥17%为合格品,上述所得ClO2溶液的物质的量浓度为0.002mol/L,则所用泡腾片____ (填“属于”或“不属于”)合格品。
(1)上述状态下的物质中,属于电解质且能导电的是
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:
您最近一年使用:0次
8 . 一氧化二氯( )是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集
)是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集 ,反应的原理如下:
,反应的原理如下: 。
。
已知: 的部分性质如表所示
的部分性质如表所示

请回答下列问题:
(1)装置A中仪器a的名称为___________ ,装置A中发生反应的化学方程式为___________ 。
(2)装置B中盛装的试剂的名称为___________ 。
(3)装置E采用冰水混合物冷却的目的是___________ 。
(4)装置F中无水 的作用是
的作用是___________ 。
(5)装置G中发生反应的离子方程式为___________ 。
(6)与传统消毒剂 比较,
比较, 消毒效率是
消毒效率是 的
的___________ 倍(产物视为 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
 )是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集
)是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集 ,反应的原理如下:
,反应的原理如下: 。
。已知:
 的部分性质如表所示
的部分性质如表所示| 物理性质 | 化学性质 |
常温下, 是棕黄色、有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ 是棕黄色、有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ |  易溶于水,同时与水反应生成 易溶于水,同时与水反应生成 |

请回答下列问题:
(1)装置A中仪器a的名称为
(2)装置B中盛装的试剂的名称为
(3)装置E采用冰水混合物冷却的目的是
(4)装置F中无水
 的作用是
的作用是(5)装置G中发生反应的离子方程式为
(6)与传统消毒剂
 比较,
比较, 消毒效率是
消毒效率是 的
的 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
您最近一年使用:0次
9 . 纪录片《神秘的古文明——三星堆》介绍了大量造型精美的青铜器,震惊世人。刚发掘的青铜器表面有很多铜锈(主要成分是氯化亚铜和碱式碳酸铜),可以用稀硫酸除去,涉及的氧化还原反应是: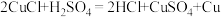 。下列有关该反应的叙述中,正确的是
。下列有关该反应的叙述中,正确的是
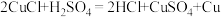 。下列有关该反应的叙述中,正确的是
。下列有关该反应的叙述中,正确的是A. 只作还原剂 只作还原剂 |
B. 只作氧化剂 只作氧化剂 |
C.氧化剂和还原剂的物质的量之比为 |
D.生成 ,转移电子物质的量为 ,转移电子物质的量为 |
您最近一年使用:0次
2024-01-12更新
|
153次组卷
|
2卷引用:黑龙江省哈尔滨市2023-2024学年高一上学期学业质量检测化学试卷
名校
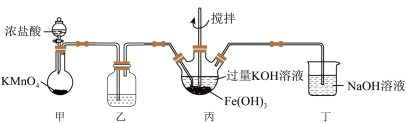
10 . 下图是实验室制备K2FeO4的实验装置图,其中甲为制氯气的装置(资料:K2FeO4为紫色固体,微溶于KOH,具有强氧化性)。回答下列问题:_______ ;乙中所用试剂为______ 。
(2)写出甲中发生反应的化学方程式:___________ 。
(3)丁装置的作用___________ ,写出发生反应的离子方程式:___________ 。
(4)写出丙中发生反应的化学方程式:___________ 。丙中产生紫色固体,说明碱性条件下,___________ 氧化性强于___________ 。若取反应后丙中紫色溶液,加入稀硫酸产生Cl2,是否可以证明K2FeO4具有氧化性:说明原因:___________ 。
(2)写出甲中发生反应的化学方程式:
(3)丁装置的作用
(4)写出丙中发生反应的化学方程式:
您最近一年使用:0次
2023-12-23更新
|
69次组卷
|
2卷引用:黑龙江省实验中学2023-2024学年高一上学期期中测试化学试题



