解题方法
1 . 工业上常用的一种海水中提溴技术叫做“吹出法”,其过程主要包括氧化、吹出、吸收和蒸馏等环节(如下图),下列有关说法错误的是
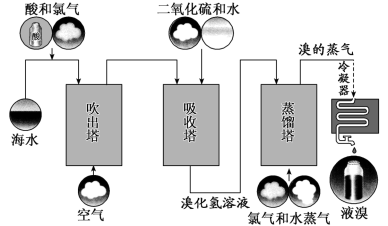
A.过程中酸化海水的目的是抑制 的溶解 的溶解 |
B.吸收塔中发生的主要反应的化学方程式为 |
| C.实验室模拟蒸馏过程,用到的主要仪器包括:蒸馏烧瓶、球形冷凝管、温度计等 |
D.保存液溴的过程中,水封的主要目的是防止或减弱 的挥发 的挥发 |
您最近一年使用:0次
名校
2 . 资料显示银镜用稀硝酸或 溶液清洗均可,某研究小组探究如下。
溶液清洗均可,某研究小组探究如下。
实验所用试剂: 溶液,
溶液, 溶液(向
溶液(向 溶液中加入
溶液中加入 至饱和),饱和碘水,
至饱和),饱和碘水,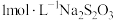 溶液。已知:
溶液。已知: 在水溶液中无色。下列说法错误的是
在水溶液中无色。下列说法错误的是
 溶液清洗均可,某研究小组探究如下。
溶液清洗均可,某研究小组探究如下。实验所用试剂:
 溶液,
溶液, 溶液(向
溶液(向 溶液中加入
溶液中加入 至饱和),饱和碘水,
至饱和),饱和碘水,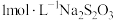 溶液。已知:
溶液。已知: 在水溶液中无色。下列说法错误的是
在水溶液中无色。下列说法错误的是
A.黄色固体为 |
B.①②实验银镜溶解速度对比说明发生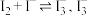 氧化性与 氧化性与 相近但溶解性更好 相近但溶解性更好 |
| C.由实验可知任一氧化剂和碘化钾的混合环境均可溶解银镜 |
D.可向①中试管底部黄色固体加入 溶液验证银镜是否溶解完全,相应的离子方程式为: 溶液验证银镜是否溶解完全,相应的离子方程式为: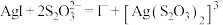 |
您最近一年使用:0次
解题方法
3 . 硫代硫酸钠( ,
,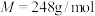 )是重要的化工原料,可用制作定影液等。其易溶于水,酸性条件不稳定。某兴趣小组在实验室开展了硫代硫酸钠制备、纯度检测和结构研究。
)是重要的化工原料,可用制作定影液等。其易溶于水,酸性条件不稳定。某兴趣小组在实验室开展了硫代硫酸钠制备、纯度检测和结构研究。
Ⅰ.制备__________ (填“仪器名称”,下同)和__________ 中的气压,使硫酸顺利流下。
(2)C装置用于观察通气速率和判断是否堵塞,其中可装入的的试剂为__________(填字母)。
(3)制备反应进行时,三通阀应调节为__________(填字母)。
(4)向 溶液通入过量
溶液通入过量 出现淡黄色沉淀,反应的离子方程式
出现淡黄色沉淀,反应的离子方程式_____________ 。
Ⅱ.纯度检测
准确称取6.200g产品,配制成100mL溶液。取20.00mL于锥形瓶中,注入缓冲溶液保证溶液为弱酸性,滴入淀粉溶液作指示剂,用 标准碘水溶液滴定到终点。已知:
标准碘水溶液滴定到终点。已知: 。
。
(5)第一次滴定开始读数为0.00mL,结束时滴定管中的液面如图所示,则第一次消耗碘水标准溶液的体积为__________ mL。重复操作,数据如下表,则产品中 的质量分数为
的质量分数为__________ 。
Ⅲ.结构研究
查阅资料知,可看成 中的一个
中的一个 被
被 代替,结构式如图。
代替,结构式如图。 的空间结构为
的空间结构为__________ 。一定条件下, 中的
中的__________ (填字母)可和金属离子配位。
A.O原子 B.中心S原子 C.端基S原子
 ,
,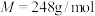 )是重要的化工原料,可用制作定影液等。其易溶于水,酸性条件不稳定。某兴趣小组在实验室开展了硫代硫酸钠制备、纯度检测和结构研究。
)是重要的化工原料,可用制作定影液等。其易溶于水,酸性条件不稳定。某兴趣小组在实验室开展了硫代硫酸钠制备、纯度检测和结构研究。Ⅰ.制备
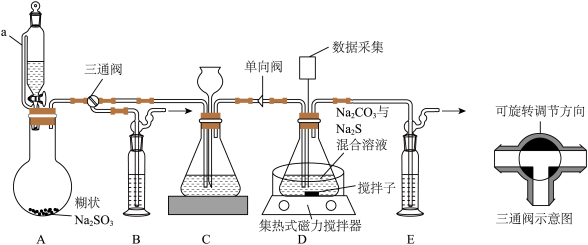
(2)C装置用于观察通气速率和判断是否堵塞,其中可装入的的试剂为__________(填字母)。
| A.浓硫酸 | B.澄清石灰水 |
C.饱和 溶液 溶液 | D.饱和NaCl溶液 |
(3)制备反应进行时,三通阀应调节为__________(填字母)。
A.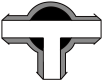 | B.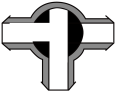 | C.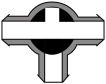 | D.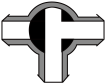 |
(4)向
 溶液通入过量
溶液通入过量 出现淡黄色沉淀,反应的离子方程式
出现淡黄色沉淀,反应的离子方程式Ⅱ.纯度检测
准确称取6.200g产品,配制成100mL溶液。取20.00mL于锥形瓶中,注入缓冲溶液保证溶液为弱酸性,滴入淀粉溶液作指示剂,用
 标准碘水溶液滴定到终点。已知:
标准碘水溶液滴定到终点。已知: 。
。(5)第一次滴定开始读数为0.00mL,结束时滴定管中的液面如图所示,则第一次消耗碘水标准溶液的体积为
 的质量分数为
的质量分数为
滴定次数 | 滴定前刻度/mL | 滴定后刻度/mL |
第二次 | 0.05 | 20.05 |
第三次 | 0.10 | 20.15 |
Ⅲ.结构研究
查阅资料知,可看成
 中的一个
中的一个 被
被 代替,结构式如图。
代替,结构式如图。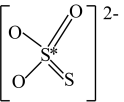
 的空间结构为
的空间结构为 中的
中的A.O原子 B.中心S原子 C.端基S原子
您最近一年使用:0次
名校
解题方法
4 . 2023 年诺贝尔化学奖授予发现量子点的三位科学家,量子点的尺寸一般在1 nm~10 nm之间,是一种纳米级别的半导体。量子点的尺寸不同,则发光颜色不同,吸收光谱波长不同。实验室一种制备CdSe量子点的方法如下:
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为___________ 。
(2)步骤Ⅱ中N2的作用为___________ ,油酸与镉配位的原子为___________ 。
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为___________ ;此方法获得Se单质过程中无需使用的仪器是___________ (填名称)。___________ 现象时,证明CdSe量子点生长基本停止,制备完成。除此方法外,还可利用___________ 物理现象初步鉴定CdSe量子点制备成功。
(5)步骤Ⅳ中加入20 mL乙醇的作用是___________ 。
(6)CdSe洗涤干净的标志是___________ 。
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
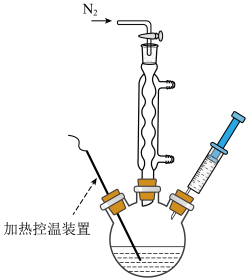
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为
(2)步骤Ⅱ中N2的作用为
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入
 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为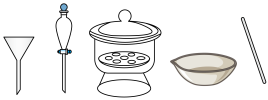
(5)步骤Ⅳ中加入20 mL乙醇的作用是
(6)CdSe洗涤干净的标志是
您最近一年使用:0次
2024-05-11更新
|
265次组卷
|
4卷引用:东北三省四市教研联合体2024届高三下学期高考模拟(二)化学试题
解题方法
5 . 草酸(H2C2O4)、草酸铵[(NH4)2C2O4]是重要的化合物。回答下列问题:
(1)实验表明,加热条件下,H2C2O4可分解生成CO2、CO和H2O。为了验证产物中的CO,设计如下实验装置:_______________ (装置可重复利用)。装置F中发生的化学反应方程式为_______________ 。
②能证明草酸晶体分解产物中有CO的现象是_______________ 。
(2)H2C2O4能与酸性高锰酸钾溶液反应,离子方程式为 。该反应中,还原剂为
。该反应中,还原剂为______________ (填化学式),若称取mg草酸晶体(H2C2O4·2H2O)粗产品,配成100mL溶液于锥形瓶中,加入V mL a mol·L-1KMnO4溶液,恰好完全反应,则该草酸晶体的纯度为______________ %[M(H2C2O4·2H2O)=126g·mol-1]。
(3)(NH4)2C2O4是良好的Co2+的沉淀剂,如下为(NH4)2C2O4加入CoSO4溶液中制备CoO的流程图:______________ (填化学式)。
②称量mg CoC2O4·2H2O[M(CoC2O4·2H2O)=183g·mol-1]“高温分解”,测得固体的失重率( )与温度的关系曲线如图所示:
)与温度的关系曲线如图所示:_______________ ;“高温分解”需控制的最低温度为_______________ (经测定290~890℃过程中产生的气体只有CO2)。
(1)实验表明,加热条件下,H2C2O4可分解生成CO2、CO和H2O。为了验证产物中的CO,设计如下实验装置:
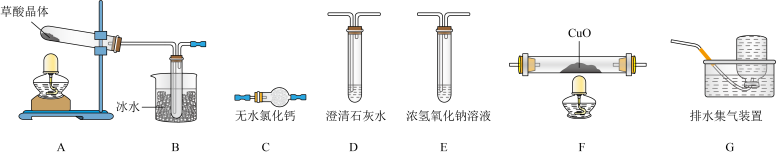
②能证明草酸晶体分解产物中有CO的现象是
(2)H2C2O4能与酸性高锰酸钾溶液反应,离子方程式为
 。该反应中,还原剂为
。该反应中,还原剂为(3)(NH4)2C2O4是良好的Co2+的沉淀剂,如下为(NH4)2C2O4加入CoSO4溶液中制备CoO的流程图:
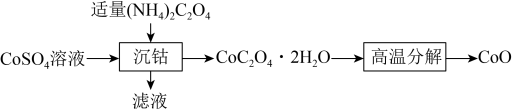
②称量mg CoC2O4·2H2O[M(CoC2O4·2H2O)=183g·mol-1]“高温分解”,测得固体的失重率(
 )与温度的关系曲线如图所示:
)与温度的关系曲线如图所示: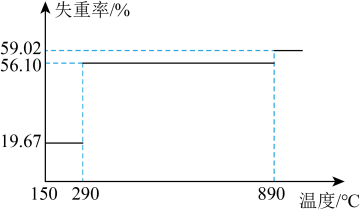
您最近一年使用:0次
名校
解题方法
6 . 铅酸蓄电池由于其技术成熟、安全性高、电压稳定及价格低廉等优势,在电池市场占据主导地位。以方铅可矿(PbS,含少量 )为原料制取
)为原料制取 的流程如图所示:
的流程如图所示:
(1)“酸浸”时温度一般控制在65~90℃,理由是___________ ,酸浸时发生反应的离子方程式为___________ 。
(2)从“酸浸”所得滤渣中回收的 ,可用于
,可用于___________ (任写两种)。
(3)“氧化”时参加反应的氧化剂与还原剂的物质的量之比为___________ 。
(4)若以100kg方铅矿(PbS的质量分数为70%)为原料,最终制得 59.75kg(假设反应过程中Pb无损失),则
59.75kg(假设反应过程中Pb无损失),则 的产率(产率
的产率(产率 )为
)为___________ (保留一位小数)。
(5)铅酸蓄电池为可充电电池,充放电时反应为 。
。
①放电时 电极的电极反应式为
电极的电极反应式为___________ 。
②充电时 电极发生
电极发生___________ (填“氧化”或“还原”)反应。
 )为原料制取
)为原料制取 的流程如图所示:
的流程如图所示: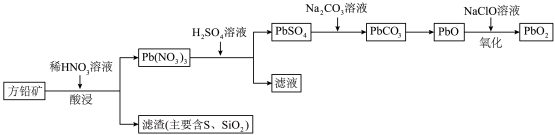
(1)“酸浸”时温度一般控制在65~90℃,理由是
(2)从“酸浸”所得滤渣中回收的
 ,可用于
,可用于(3)“氧化”时参加反应的氧化剂与还原剂的物质的量之比为
(4)若以100kg方铅矿(PbS的质量分数为70%)为原料,最终制得
 59.75kg(假设反应过程中Pb无损失),则
59.75kg(假设反应过程中Pb无损失),则 的产率(产率
的产率(产率 )为
)为(5)铅酸蓄电池为可充电电池,充放电时反应为
 。
。①放电时
 电极的电极反应式为
电极的电极反应式为②充电时
 电极发生
电极发生
您最近一年使用:0次
2024-05-07更新
|
151次组卷
|
4卷引用:黑龙江省双鸭山市第一中学2023-2024学年高一下学期5月期中化学试题
名校
7 . 尿素(分子式 )水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
)水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
 )水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
)水溶液热解产生的NH3可去除尾气中的NOx,流程如下: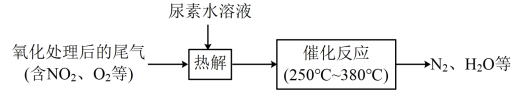
| A.尿素中氮元素的化合价为-3 |
B.“催化反应”过程中NH3还原NO2的化学方程式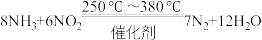 |
| C.若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。硫酸盐的产生是因为SO2被O2、H2O还原成H2SO4,再与NH3反应而得 |
D.“催化反应”过程中需控制温度在 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低 |
您最近一年使用:0次
2024-04-22更新
|
250次组卷
|
2卷引用:黑龙江省鹤岗市萝北县高级中学2023-2024学年高一下学期6月考试化学试卷
名校
8 . 完成下列化学方程式(是离子反应的写离子方程式):
(1)等物质的量二氧化硫和氯气通入水中:___________ 。
(2)二氧化硫通入酸性高锰酸钾溶液中:___________ 。
(3)高温煅烧黄铁矿:___________ 。
(4)炭与浓硫酸加热:___________ 。
(5)硫与浓硫酸加热:___________ 。
(6)铜和浓硫酸加热:___________ 。
(7)铜和浓硝酸(实验室制 ):
):___________ 。
(8)铜和稀硝酸(实验室制 ):
):___________ 。
(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中:___________ 。
(10)二氧化氮通入苛性钠溶液中:___________ 。
(1)等物质的量二氧化硫和氯气通入水中:
(2)二氧化硫通入酸性高锰酸钾溶液中:
(3)高温煅烧黄铁矿:
(4)炭与浓硫酸加热:
(5)硫与浓硫酸加热:
(6)铜和浓硫酸加热:
(7)铜和浓硝酸(实验室制
 ):
):(8)铜和稀硝酸(实验室制
 ):
):(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中:
(10)二氧化氮通入苛性钠溶液中:
您最近一年使用:0次
名校
解题方法
9 . 以Al2O3为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废Pd-Al2O3催化剂(主要含有Pd、Al2O3,还有少量PdO、SiO2、C)为原料制备氯化钯的流程如下:
(1)“焙烧”能有效清除废催化剂表面的积碳,打开Al2O3载体对钯的包裹,提高“氯化浸出”率。依据下图可判断“焙烧”的温度和时间应控制在___________ ,若焙烧时间过长,导致“氯化浸出”率下降可能的原因是___________ 。___________ ,通过该工序可将Pd转化为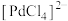 ,
,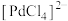 呈平面四边形,则
呈平面四边形,则 的杂化轨道类型为
的杂化轨道类型为___________ (填字母)。
A.sp2杂化 B.sp3杂化 C.dsp2杂化 D.dsp3杂化
(3)滤渣1为___________ ,滤渣2为___________ 。
(4)就“沉钯”中获得的 进行“热分解”,生成的气体可返回
进行“热分解”,生成的气体可返回___________ 工序继续使用。
(5)工业上也可用 还原
还原 制取海绵Pd,且对环境友好,该反应的化学方程式为
制取海绵Pd,且对环境友好,该反应的化学方程式为___________ 。
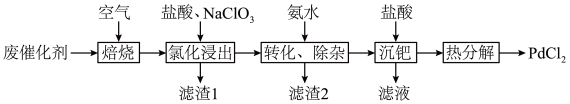
(1)“焙烧”能有效清除废催化剂表面的积碳,打开Al2O3载体对钯的包裹,提高“氯化浸出”率。依据下图可判断“焙烧”的温度和时间应控制在

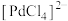 ,
,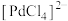 呈平面四边形,则
呈平面四边形,则 的杂化轨道类型为
的杂化轨道类型为A.sp2杂化 B.sp3杂化 C.dsp2杂化 D.dsp3杂化
(3)滤渣1为
(4)就“沉钯”中获得的
 进行“热分解”,生成的气体可返回
进行“热分解”,生成的气体可返回(5)工业上也可用
 还原
还原 制取海绵Pd,且对环境友好,该反应的化学方程式为
制取海绵Pd,且对环境友好,该反应的化学方程式为
您最近一年使用:0次
2024-04-02更新
|
591次组卷
|
4卷引用:东北三省2024届高三下学期三校二模联考化学试题
名校
解题方法
10 . KMnO4是重要氧化剂,广泛用于化工、防腐以及制药等领域。以软锰矿(主要成分为MnO2)为原料,经中间产物K2MnO4制备KMnO4的流程如图。下列说法错误的是
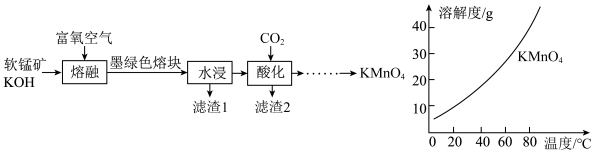
A.“熔融”过程中,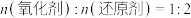 |
| B.滤渣2经处理后可循环回“熔融”过程以提高锰元素的利用率 |
| C.用盐酸替代CO2能加快“酸化”时的速率 |
| D.得到KMnO4晶体的操作为蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥 |
您最近一年使用:0次
2024-04-02更新
|
1062次组卷
|
6卷引用:东北三省2024届高三下学期三校二模联考化学试题
东北三省2024届高三下学期三校二模联考化学试题黑龙江省哈尔滨市三校联考2024届高三二模化学试题(已下线)化学(新七省高考“15+4”)-2024年高考押题预测卷东北三省2024届高三下学期三校二模联考化学试题湖南省衡阳县第四中学2023-2024学年高三下学期4月月考化学试题(已下线)压轴题02 氧化还原反应的概念及规律(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)



