解题方法
1 . 研究人员对Na2SO3和Fe粉去除废水中的硝态氮进行研究。
已知:i.某工厂排放的含氮废水中总氮=10mg·L-1,含有硝态氮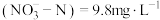 、氨氮
、氨氮 。
。
ii.本实验中Na2SO3在 时,脱除硝态氮(转化为N2)效果较强。
时,脱除硝态氮(转化为N2)效果较强。
iii.Na2SO3和Fe粉均可以脱除硝态氮,本实验中二者均为过量。
(1)Na2SO3和Fe粉在去除废水中硝态氮的过程中表现___________ 性(填“氧化”或“还原”)。
(2)研究Na2SO3在pH=1的含氮废水中发生反应的情况,实验结果如图1。
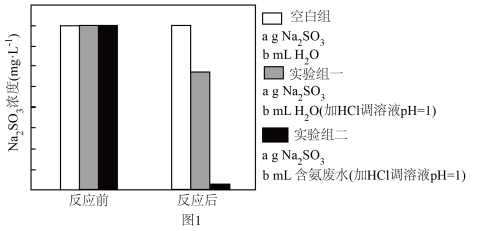
①根据图1,写出“实验组一”中发生反应的离子方程式___________ 。
②进行“实验组二”实验时发现,降低溶液pH更有利于 的去除,可能的原因是
的去除,可能的原因是___________ 。
(3)脱除pH=1的含氮废水中硝态氮,单独加入Na2SO3或同时加入Na2SO3与Fe粉的实验结果如图2和图3。
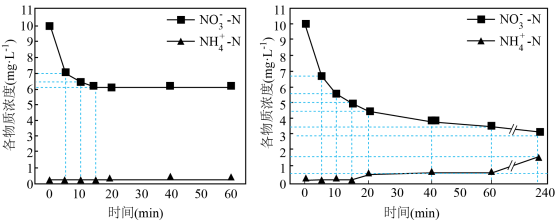
①根据图2,前15min内Na2SO3,脱除NO;主要反应的离子方程式为___________ 。
②根据图2和图3,20~60min内体系中生成 主要反应的离子方程式为
主要反应的离子方程式为___________ 。
③检验处理后的废水中存在 取一定量废水蒸发浓缩,
取一定量废水蒸发浓缩,___________ (补充操作和现象)。
已知:i.某工厂排放的含氮废水中总氮=10mg·L-1,含有硝态氮
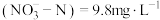 、氨氮
、氨氮 。
。ii.本实验中Na2SO3在
 时,脱除硝态氮(转化为N2)效果较强。
时,脱除硝态氮(转化为N2)效果较强。iii.Na2SO3和Fe粉均可以脱除硝态氮,本实验中二者均为过量。
(1)Na2SO3和Fe粉在去除废水中硝态氮的过程中表现
(2)研究Na2SO3在pH=1的含氮废水中发生反应的情况,实验结果如图1。

①根据图1,写出“实验组一”中发生反应的离子方程式
②进行“实验组二”实验时发现,降低溶液pH更有利于
 的去除,可能的原因是
的去除,可能的原因是(3)脱除pH=1的含氮废水中硝态氮,单独加入Na2SO3或同时加入Na2SO3与Fe粉的实验结果如图2和图3。

①根据图2,前15min内Na2SO3,脱除NO;主要反应的离子方程式为
②根据图2和图3,20~60min内体系中生成
 主要反应的离子方程式为
主要反应的离子方程式为③检验处理后的废水中存在
 取一定量废水蒸发浓缩,
取一定量废水蒸发浓缩,
您最近一年使用:0次
2023-11-15更新
|
214次组卷
|
3卷引用:福建省福清西山学校2023-2024学年高三上学期12月月考化学试题
2 . 某化学小组设计实验探究是否“NO2能与赤热的铜反应生成氧化铜和氮气”。已知:
Ⅰ.NO和FeSO4溶液反应:NO+FeSO4=FeSO4·NO (棕色)
Ⅱ.酸性KMnO4溶液吸收NO生成NO 和Mn2+
和Mn2+
设计实验装置如图所示(各装置中液态试剂均足量)。
(1)该实验装置的连接顺序为:_______ (填装置序号);C装置中盛装试剂是_______ ,其目的是:_______ 。
(2)开始实验时,为排出装置内空气,所要进行的操作是_______ 。
(3)实验过程中,观察到下列现象,请回答:
①B中浅绿色溶液变棕色,得出实验结论是_______ (填代号)。
(a)NO2的还原产物可能有NO
(b)NO2的还原产物一定无NO
(c)NO2的还原产物一定有NO
②E中有紫红色溶液变无色的现象,写出发生反应的离子方程式:_______ 。
(4)当D中铜粉完全反应时停止A中反应,测得反应后D中固体粉末质量为ag。
①当a=_______ (用含 m的代数式表示)时,铜被氧化的产物全部是CuO。
②已知:Cu2O+2H+=Cu+Cu2++H2O,设计下列方案,验证反应后D中固体是否有Cu2O,其中,方案和结论正确的是_______ (填代号)
Ⅰ.NO和FeSO4溶液反应:NO+FeSO4=FeSO4·NO (棕色)
Ⅱ.酸性KMnO4溶液吸收NO生成NO
 和Mn2+
和Mn2+设计实验装置如图所示(各装置中液态试剂均足量)。
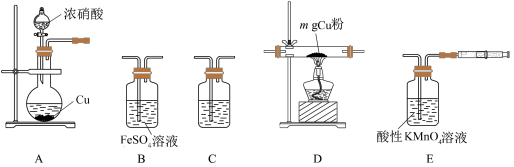
(1)该实验装置的连接顺序为:
(2)开始实验时,为排出装置内空气,所要进行的操作是
(3)实验过程中,观察到下列现象,请回答:
①B中浅绿色溶液变棕色,得出实验结论是
(a)NO2的还原产物可能有NO
(b)NO2的还原产物一定无NO
(c)NO2的还原产物一定有NO
②E中有紫红色溶液变无色的现象,写出发生反应的离子方程式:
(4)当D中铜粉完全反应时停止A中反应,测得反应后D中固体粉末质量为ag。
①当a=
②已知:Cu2O+2H+=Cu+Cu2++H2O,设计下列方案,验证反应后D中固体是否有Cu2O,其中,方案和结论正确的是
| 方案 | 操作 | 现象与结论 |
| A | 取少量固体溶于稀硫酸中 | 溶液中有红色固体,则含Cu2O |
| B | 取少量固体溶于稀硝酸中 | 溶液变蓝色,则含Cu2O |
| C | 取少量固体溶于盐酸中 | 溶液变蓝色(或绿色),则含Cu2O |
| D | 取少量固体加热,通入H2,将气体通入无水硫酸铜粉末中 | 白色硫酸铜粉末变蓝色,则含Cu2O |
您最近一年使用:0次
3 . 下图为各单质与化合物之间的转化关系,单质及化合物的组成元素均为常见的短周期元素。请回答:

(1)若沉淀丁不溶于过量的盐酸,单质A为_______ 。若沉淀丁能溶于过量的盐酸,化合物甲为_______ 。
(2)单质B的化学式为_______ ,丙的电子式为_______ 。
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:_______ 。
(4)KMnO4是重要的氧化剂,在双氧水中滴加少量用稀硫酸酸化的KMnO4溶液,溶液迅速变为无色,同时生成单质B。写出该反应的离子方程式_______ 。
(5)单质B的同素异体与Na2FeO4同是良好的消毒剂,在新冠疫情防控中作用巨大。在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为_______ 。

(1)若沉淀丁不溶于过量的盐酸,单质A为
(2)单质B的化学式为
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:
(4)KMnO4是重要的氧化剂,在双氧水中滴加少量用稀硫酸酸化的KMnO4溶液,溶液迅速变为无色,同时生成单质B。写出该反应的离子方程式
(5)单质B的同素异体与Na2FeO4同是良好的消毒剂,在新冠疫情防控中作用巨大。在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为
您最近一年使用:0次
名校
解题方法
4 . 化学与生产生活密切相关,请根据要求回答下列问题:
(1)纯净的液态硫酸___________ (填“能”或“几乎不能”)导电,在硫酸不断稀释的过程中,溶液导电能力的变化情况为___________ 。
(2)传统蒸馒头常采用酵头发面,再用 调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生
调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
①与等质量的碳酸钠和碳酸氢钠完全反应,消耗酸更多的物质的名称是___________ 。
②若面团发得不好,面团内的气孔少,略有酸味。可不用 而用
而用 ,继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式解释
,继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式解释 的作用
的作用___________ 。
(3)无土栽培需要配制一定组成的植物营养液。已知某植物营养液的配方为: 0.7mol⋅L
0.7mol⋅L ,
, 0.3mol⋅L
0.3mol⋅L 、
、 0.1mol⋅L
0.1mol⋅L 。若以KCl、
。若以KCl、 、
、 和
和 为原料配制1L该营养液,使用托盘天平称量KCl的质量为
为原料配制1L该营养液,使用托盘天平称量KCl的质量为___________ 。
(4)在工业上次磷酸( )常用于化学镀银,发生的反应如下:
)常用于化学镀银,发生的反应如下:
_______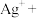 _______
_______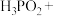 _____
_____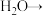 ______
______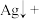 _______
_______ ______
______
① 中,P元素的化合价为
中,P元素的化合价为_______ ;该反应中, 被
被________ (填“氧化”或“还原”)。
②配平该离子方程式:___________ 。
③ 与过量NaOH溶液反应的方程式为
与过量NaOH溶液反应的方程式为 ,则
,则 是
是___________ 元酸(填“一”或“二”或“三”)。
(1)纯净的液态硫酸
(2)传统蒸馒头常采用酵头发面,再用
 调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生
调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。①与等质量的碳酸钠和碳酸氢钠完全反应,消耗酸更多的物质的名称是
②若面团发得不好,面团内的气孔少,略有酸味。可不用
 而用
而用 ,继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式解释
,继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式解释 的作用
的作用(3)无土栽培需要配制一定组成的植物营养液。已知某植物营养液的配方为:
 0.7mol⋅L
0.7mol⋅L ,
, 0.3mol⋅L
0.3mol⋅L 、
、 0.1mol⋅L
0.1mol⋅L 。若以KCl、
。若以KCl、 、
、 和
和 为原料配制1L该营养液,使用托盘天平称量KCl的质量为
为原料配制1L该营养液,使用托盘天平称量KCl的质量为(4)在工业上次磷酸(
 )常用于化学镀银,发生的反应如下:
)常用于化学镀银,发生的反应如下:_______
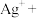 _______
_______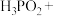 _____
_____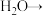 ______
______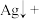 _______
_______ ______
______
①
 中,P元素的化合价为
中,P元素的化合价为 被
被②配平该离子方程式:
③
 与过量NaOH溶液反应的方程式为
与过量NaOH溶液反应的方程式为 ,则
,则 是
是
您最近一年使用:0次
2023-11-11更新
|
168次组卷
|
2卷引用:福建省厦门市第一中学2023-2024学年高一上学期期中考试化学试题
名校
5 . 化学工业为医药行业提供了强有力的物质支撑。请按要求回答下列问题:
(1)研究表明病毒可通过气溶胶传播,气溶胶中粒子的直径大小为___________ ,可以用___________ 来鉴别气溶胶。
(2)常温下, 、乙醇、
、乙醇、 、NaClO溶液都为常用的消毒剂,其中能导电的是
、NaClO溶液都为常用的消毒剂,其中能导电的是___________ ,属于电解质的是___________ 。
(3)熔喷布是一次性医用口罩的关键材料,由熔融态聚丙烯电喷形成的超细纤维经驻极静电处理制成。由丙烯制得聚丙烯的化学方程式是___________ 。
(4)家用制氧机“氧立得”使用的是过碳酸钠( ),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
①写出过碳酸钠在二氧化锰催化下产生氧气的化学方程式:___________ 。
②下列物质不会使过碳酸钠失效的是___________ (填标号)。
A.HCl B. C.
C. D.
D.
(5)消毒能力一般用单位质量的消毒剂所得电子的数量来衡量, 、NaClO等含氯消毒剂进行反应时最终都转化为
、NaClO等含氯消毒剂进行反应时最终都转化为 ,则
,则 与NaClO的消毒能力之比为
与NaClO的消毒能力之比为___________ (写出最简整数比)。
(6)医药行业中测温枪发挥了极大的作用。在测温枪电池制备过程中会生成 (Ti为+4价),1mol
(Ti为+4价),1mol 中过氧键的数目为
中过氧键的数目为___________ 。
(1)研究表明病毒可通过气溶胶传播,气溶胶中粒子的直径大小为
(2)常温下,
 、乙醇、
、乙醇、 、NaClO溶液都为常用的消毒剂,其中能导电的是
、NaClO溶液都为常用的消毒剂,其中能导电的是(3)熔喷布是一次性医用口罩的关键材料,由熔融态聚丙烯电喷形成的超细纤维经驻极静电处理制成。由丙烯制得聚丙烯的化学方程式是
(4)家用制氧机“氧立得”使用的是过碳酸钠(
 ),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
),该药品被称为固体双氧水,兼具碳酸钠和双氧水的双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。①写出过碳酸钠在二氧化锰催化下产生氧气的化学方程式:
②下列物质不会使过碳酸钠失效的是
A.HCl B.
 C.
C. D.
D.
(5)消毒能力一般用单位质量的消毒剂所得电子的数量来衡量,
 、NaClO等含氯消毒剂进行反应时最终都转化为
、NaClO等含氯消毒剂进行反应时最终都转化为 ,则
,则 与NaClO的消毒能力之比为
与NaClO的消毒能力之比为(6)医药行业中测温枪发挥了极大的作用。在测温枪电池制备过程中会生成
 (Ti为+4价),1mol
(Ti为+4价),1mol 中过氧键的数目为
中过氧键的数目为
您最近一年使用:0次
名校
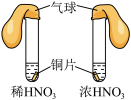
6 . 通过以下实验装置,不能达到实验目的的是
|
|
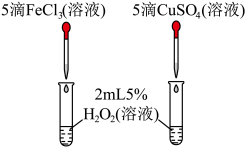
| A.通过气球膨胀速率比较浓硝酸和稀硝酸的氧化性强弱 | B.通过试管中气泡产生速率比较 和 和 的催化效率高低 的催化效率高低 |
|
|
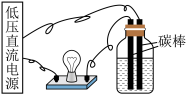
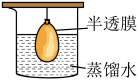
| C.通过小灯泡亮度判断不同浓度NaCl溶液的导电性强弱 | D.通过以上装置分离NaCl溶液和 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-01更新
|
199次组卷
|
3卷引用:福建省福州第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
7 . 高铁酸钾(K2FeO4)是一种新型、高效、无毒的水处理剂。工业上,利用廉价的铁黄(FeOOH)等为原料制备高铁酸钾。工艺流程如图:
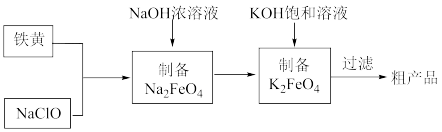
下列说法错误的是

下列说法错误的是
| A.高铁酸钾在水处理过程中涉及氧化还原反应和盐类水解反应 |
| B.制备Na2FeO4反应中氧化剂和还原剂的物质的量之比为2∶3 |
| C.根据流程可以判断相同温度下K2FeO4的溶解度小于Na2FeO4 |
| D.若通过电解法以铁为原料制备高铁酸钾,铁棒应该做阳极 |
您最近一年使用:0次
2023-10-27更新
|
1047次组卷
|
5卷引用:福建省厦门外国语学校2023-2024学年高二上学期期末模拟考试化学试题
福建省厦门外国语学校2023-2024学年高二上学期期末模拟考试化学试题广西部分高中2024届高三第一次摸底测试化学试题广西南宁市2024届高三上学期毕业班摸底测试化学试题(已下线)选择题6-10(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
8 . 物质的分离和鉴别是化学实验中常见的操作。已知某固体混合物可能由 、
、 、
、 、Fe、
、Fe、 、
、 、
、 中的若干种物质组成,某化学兴趣小组设计实验探究该固体混合物的部分组分,实验方案如图(加入的试剂均过量)。请回答下列问题:
中的若干种物质组成,某化学兴趣小组设计实验探究该固体混合物的部分组分,实验方案如图(加入的试剂均过量)。请回答下列问题:

(1)上述实验中需用到480mL 稀硫酸,现用98%的浓硫酸(密度为
稀硫酸,现用98%的浓硫酸(密度为 )配制,则配制时用到的玻璃仪器除烧杯、量筒外,还有
)配制,则配制时用到的玻璃仪器除烧杯、量筒外,还有___________ ,需要量取___________ (保留一位小数)mL98%的浓硫酸。
(2)写出②中酸性高锰酸钾溶液发生氧化还原反应的离子方程式:___________ 。由此可推出原固体混合物中一定含有___________ (填化学式)。
(3)请准确描述白色沉淀B转变成红褐色沉淀C的过程中的现象:___________ 。
(4)根据上述实验,某同学推测原固体混合物中至少有 、Fe中的一种,若仅有
、Fe中的一种,若仅有 时,写出①中生成白色沉淀B中阳离子的离子方程式:
时,写出①中生成白色沉淀B中阳离子的离子方程式:___________ 。
(5)将固体A加入___________ (填试剂名称)中可以判断原固体混合物中是否含有 ;向溶液B中通入足量的
;向溶液B中通入足量的 ,若
,若___________ (填实验现象),则可以确认原固体混合物中含有 。
。
 、
、 、
、 、Fe、
、Fe、 、
、 、
、 中的若干种物质组成,某化学兴趣小组设计实验探究该固体混合物的部分组分,实验方案如图(加入的试剂均过量)。请回答下列问题:
中的若干种物质组成,某化学兴趣小组设计实验探究该固体混合物的部分组分,实验方案如图(加入的试剂均过量)。请回答下列问题:
(1)上述实验中需用到480mL
 稀硫酸,现用98%的浓硫酸(密度为
稀硫酸,现用98%的浓硫酸(密度为 )配制,则配制时用到的玻璃仪器除烧杯、量筒外,还有
)配制,则配制时用到的玻璃仪器除烧杯、量筒外,还有(2)写出②中酸性高锰酸钾溶液发生氧化还原反应的离子方程式:
(3)请准确描述白色沉淀B转变成红褐色沉淀C的过程中的现象:
(4)根据上述实验,某同学推测原固体混合物中至少有
 、Fe中的一种,若仅有
、Fe中的一种,若仅有 时,写出①中生成白色沉淀B中阳离子的离子方程式:
时,写出①中生成白色沉淀B中阳离子的离子方程式:(5)将固体A加入
 ;向溶液B中通入足量的
;向溶液B中通入足量的 ,若
,若 。
。
您最近一年使用:0次
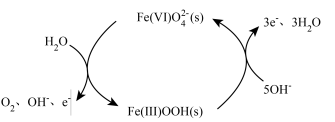
9 . 我国科学家通过简单的光谱电化学直接检测浸出到电解质中的高度氧化的 (VI)中间体。下图为水氧化过程中
(VI)中间体。下图为水氧化过程中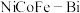 催化剂中
催化剂中 (VI)活性物质形成的机理。下列说法错误的是
(VI)活性物质形成的机理。下列说法错误的是
 (VI)中间体。下图为水氧化过程中
(VI)中间体。下图为水氧化过程中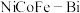 催化剂中
催化剂中 (VI)活性物质形成的机理。下列说法错误的是
(VI)活性物质形成的机理。下列说法错误的是
A.氧化性: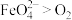 |
B.该过程中电解质溶液的 增大 增大 |
C.该过程中 (VI)活性物质被富集 (VI)活性物质被富集 |
| D.NiCoFe-Bi催化剂加快水氧化的速率 |
您最近一年使用:0次
10 . 完成下列小题
(1)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有:Al2O3、C、N2、AlN、CO,请将AlN之外的反应物与生成物分别填入横线上,并配平_____ 。
_____+_____+_____→AlN+_____
(2)Na2S2O3(其会在稀硫酸中发生歧化反应)还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为_____ 。
(3)对于反应K2Cr2O7+HCl→KCl+CrCl3+Cl2 +H2O(未配平),若有0.1moLK2Cr2O7参加反应,被还原的HCl为
+H2O(未配平),若有0.1moLK2Cr2O7参加反应,被还原的HCl为_____ mol
(1)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有:Al2O3、C、N2、AlN、CO,请将AlN之外的反应物与生成物分别填入横线上,并配平
_____+_____+_____→AlN+_____
(2)Na2S2O3(其会在稀硫酸中发生歧化反应)还原性较强,在溶液中易被Cl2氧化成SO
 ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为(3)对于反应K2Cr2O7+HCl→KCl+CrCl3+Cl2
 +H2O(未配平),若有0.1moLK2Cr2O7参加反应,被还原的HCl为
+H2O(未配平),若有0.1moLK2Cr2O7参加反应,被还原的HCl为
您最近一年使用:0次