名校
1 . 随着科学技术的发展,许多新材料、新技术广泛应用于各个领域。
I.图1是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
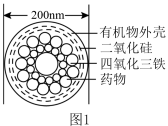
(1)“纳米药物分子车”分散于水中所得的分散系__________ (填“属于”或“不属于”)胶体。
(2)“纳米药物分子车”的外壳属于有机物。①酒精②蔗糖③冰醋酸中这三种有机物中,属于电解质的是__________ (填序号)。
(3)从元素组成的角度分析, 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的__________ 。
Ⅱ.无土栽培技术的成功推广,营养液的准确配制是重要环节。某 营养液中含有
营养液中含有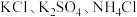 三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中
三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中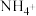 的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
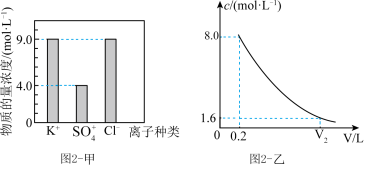
(4)该营养液中 的物质的量浓度为
的物质的量浓度为__________ 。
(5)写出一种与 含相同电子数的分子的化学式
含相同电子数的分子的化学式______________ ;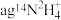 含有的中子的物质的量为
含有的中子的物质的量为__________ 。
Ⅲ.近年来,我国储氢材料的研制取得重大发展。其中电弧法合成储氢碳纳米管时,常伴有大量碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,其反应原理如下:
_____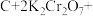 _____
_____ (稀)
(稀) ____
____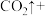 _____
_____ _____
_____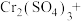 _____
_____
回答下列问题:
(6)完成上述反应的配平_________ 。
(7)某学生欲配制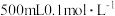 的稀硫酸,用量筒量取需要的浓硫酸,则需量取
的稀硫酸,用量筒量取需要的浓硫酸,则需量取 的浓硫酸
的浓硫酸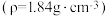 的体积为
的体积为__________ 。
(8)标准状况下,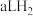 和
和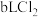 的混合气体,经强光充分照射后,所得气体恰好使含
的混合气体,经强光充分照射后,所得气体恰好使含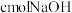 的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是____________________ 。
I.图1是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:

(1)“纳米药物分子车”分散于水中所得的分散系
(2)“纳米药物分子车”的外壳属于有机物。①酒精②蔗糖③冰醋酸中这三种有机物中,属于电解质的是
(3)从元素组成的角度分析,
 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的Ⅱ.无土栽培技术的成功推广,营养液的准确配制是重要环节。某
 营养液中含有
营养液中含有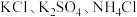 三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中
三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中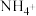 的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
(4)该营养液中
 的物质的量浓度为
的物质的量浓度为(5)写出一种与
 含相同电子数的分子的化学式
含相同电子数的分子的化学式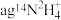 含有的中子的物质的量为
含有的中子的物质的量为Ⅲ.近年来,我国储氢材料的研制取得重大发展。其中电弧法合成储氢碳纳米管时,常伴有大量碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,其反应原理如下:
_____
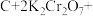 _____
_____ (稀)
(稀) ____
____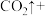 _____
_____ _____
_____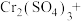 _____
_____
回答下列问题:
(6)完成上述反应的配平
(7)某学生欲配制
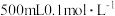 的稀硫酸,用量筒量取需要的浓硫酸,则需量取
的稀硫酸,用量筒量取需要的浓硫酸,则需量取 的浓硫酸
的浓硫酸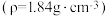 的体积为
的体积为(8)标准状况下,
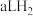 和
和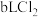 的混合气体,经强光充分照射后,所得气体恰好使含
的混合气体,经强光充分照射后,所得气体恰好使含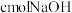 的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
您最近一年使用:0次
名校
解题方法
2 .  是一种大气污染物,但它在化工和食品工业上却有广泛应用.某兴趣小组同学对
是一种大气污染物,但它在化工和食品工业上却有广泛应用.某兴趣小组同学对 的实验室制备(加热装置省略)和性质实验进行研究.
的实验室制备(加热装置省略)和性质实验进行研究.

(1)实验中铜与浓硫酸反应的化学方程式是___________ .在该反应中浓硫酸体现了___________ 性。
(2)从物质类别分析 是酸性氧化物,可以使装置
是酸性氧化物,可以使装置 中的澄清石灰水变浑浊,写出
中的澄清石灰水变浑浊,写出 使澄清石灰水变浑浊的离子方程式
使澄清石灰水变浑浊的离子方程式___________ 。
(3)从化合价角度分析 既有氧化性又有还原性:
既有氧化性又有还原性:
①若C中盛有 溶液,当溶液由黄色变成浅绿色则证明
溶液,当溶液由黄色变成浅绿色则证明 具有还原性,写出该过程的离子方程式
具有还原性,写出该过程的离子方程式___________ 。
②若 中盛有
中盛有 溶液,当溶液有黄色沉淀产生,则证明
溶液,当溶液有黄色沉淀产生,则证明 具有氧化性,写出该过程的化学方程式
具有氧化性,写出该过程的化学方程式___________
(4) 还具有漂白性,则
还具有漂白性,则 中盛放的是
中盛放的是___________ 溶液。
(5)装置 的作用为
的作用为___________ 。
 是一种大气污染物,但它在化工和食品工业上却有广泛应用.某兴趣小组同学对
是一种大气污染物,但它在化工和食品工业上却有广泛应用.某兴趣小组同学对 的实验室制备(加热装置省略)和性质实验进行研究.
的实验室制备(加热装置省略)和性质实验进行研究.
(1)实验中铜与浓硫酸反应的化学方程式是
(2)从物质类别分析
 是酸性氧化物,可以使装置
是酸性氧化物,可以使装置 中的澄清石灰水变浑浊,写出
中的澄清石灰水变浑浊,写出 使澄清石灰水变浑浊的离子方程式
使澄清石灰水变浑浊的离子方程式(3)从化合价角度分析
 既有氧化性又有还原性:
既有氧化性又有还原性:①若C中盛有
 溶液,当溶液由黄色变成浅绿色则证明
溶液,当溶液由黄色变成浅绿色则证明 具有还原性,写出该过程的离子方程式
具有还原性,写出该过程的离子方程式②若
 中盛有
中盛有 溶液,当溶液有黄色沉淀产生,则证明
溶液,当溶液有黄色沉淀产生,则证明 具有氧化性,写出该过程的化学方程式
具有氧化性,写出该过程的化学方程式(4)
 还具有漂白性,则
还具有漂白性,则 中盛放的是
中盛放的是(5)装置
 的作用为
的作用为
您最近一年使用:0次
名校
3 . 下图是自然界中不同价态硫元素之间的转化关系图。回答下列问题:

(1)硫元素在自然界中的存在形态有___________ 和化合态,单质硫矿主要存在于___________ ; 硫单质有多种,正交硫和单斜硫,它们均为硫元素的___________ 。
(2)H2SO4 的电离方程式为___________ 。
(3)硫酸是重要的化工原料,接触法制硫酸主要分三步:
①煅烧黄铁矿(FeS2);_____FeS2 + _____O2 _____Fe2O3 + _____SO2
_____Fe2O3 + _____SO2 ___________ ;
②SO2 的接触氧化;___________ ;
③98.3% H2SO4 吸收:SO3 + H2O=H2SO4。
(4)Fe2O3 可用于焊接钢轨,写出反应的化学方程式___________ 。
(5)写出铜与浓硫酸反应的的化学方程式为___________ ,若反应产生672mL(标准状况)还原性气体,转移电子的数目为___________ 。

(1)硫元素在自然界中的存在形态有
(2)H2SO4 的电离方程式为
(3)硫酸是重要的化工原料,接触法制硫酸主要分三步:
①煅烧黄铁矿(FeS2);_____FeS2 + _____O2
 _____Fe2O3 + _____SO2
_____Fe2O3 + _____SO2 ②SO2 的接触氧化;
③98.3% H2SO4 吸收:SO3 + H2O=H2SO4。
(4)Fe2O3 可用于焊接钢轨,写出反应的化学方程式
(5)写出铜与浓硫酸反应的的化学方程式为
您最近一年使用:0次
名校
4 . 填空
(1)有钠、氢、氧、硫四种元素,用其中的一种或几种元素可以组成多种物质,写出符合下列要求的化学式或化学方程式(各写一个):
①酸式盐________ ②非电解质________ ③置换反应:________ ;
(2)配平反应________  ________
________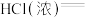 ________
________ ________
________ ________
________ ________
________ 。还原产物为
。还原产物为________ ,若有 参加反应,则参加反应的HCl为
参加反应,则参加反应的HCl为________ mol,其中被氧化的HCl为________ mol,转移电子的物质的量为________ mol
(1)有钠、氢、氧、硫四种元素,用其中的一种或几种元素可以组成多种物质,写出符合下列要求的化学式或化学方程式(各写一个):
①酸式盐
(2)配平反应
 ________
________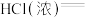 ________
________ ________
________ ________
________ ________
________ 。还原产物为
。还原产物为 参加反应,则参加反应的HCl为
参加反应,则参加反应的HCl为
您最近一年使用:0次
名校
5 . 高锰酸钾在工业中广泛用作氧化剂。以软锰矿(主要成分是 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示: 生成。
生成。
②20℃时各物质的溶解度如下表。
下列说法错误的是
 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示: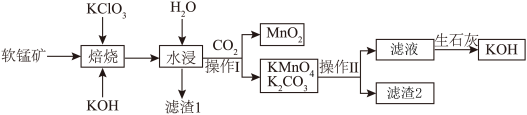
 生成。
生成。 ②20℃时各物质的溶解度如下表。
| 物质 |  |  |  |
| 溶解度/g | 6.38 | 111 | 11.1 |
A.“焙烧”时,主要反应的化学方程式为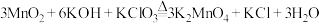 |
B.通入 时,理论上生成的 时,理论上生成的 和 和 的物质的量之比为 的物质的量之比为 |
C.若“焙烧”时加入的 过量,则制得的 过量,则制得的 中混有含 中混有含 元素的杂质 元素的杂质 |
D.操作Ⅱ为蒸发浓缩、冷却结晶、过滤,滤渣2的主要成分为 |
您最近一年使用:0次
2023-12-21更新
|
820次组卷
|
5卷引用:福建省福州第一中学2023-2024学年高三上学期期末考试化学试题
名校
解题方法
6 . 实验室以含锌废液(主要成分为 ,还含有少量的
,还含有少量的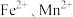 )为原料制备
)为原料制备 的实验流程如下:
的实验流程如下:
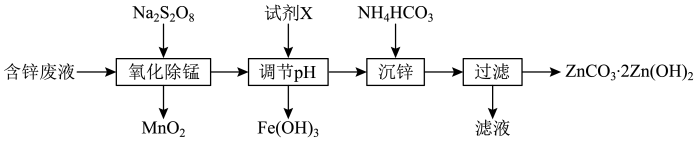
(1)写出基态 原子的电子排布式:
原子的电子排布式:___________ , 中
中 元素的化合价为
元素的化合价为___________ 。
(2)写出“氧化除锰”时反应的离子方程式:___________ 。
(3)常温下“调节 ”时,试剂
”时,试剂 可选用
可选用___________ ;已知溶液中 物质的量浓度为
物质的量浓度为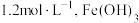 的
的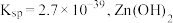 的
的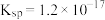 ,则
,则 的调节范围为
的调节范围为___________ 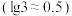 。已知:当溶液中离子浓度小于或等于
。已知:当溶液中离子浓度小于或等于 ,认为该离子已除尽。
,认为该离子已除尽。
(4)写出“沉锌”时反应的离子方程式:___________ 。
(5)“滤液”中的主要成分的用途:___________ 。
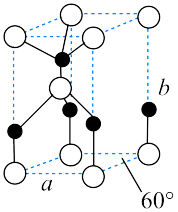
(6) 经焙解得到的活性
经焙解得到的活性 晶胞结构如图所示。该晶胞中
晶胞结构如图所示。该晶胞中 原子的配位数为
原子的配位数为___________ ;已知晶胞参数为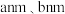 ,则该晶胞的密度为
,则该晶胞的密度为___________  。(写出计算表达式即可)
。(写出计算表达式即可)
 ,还含有少量的
,还含有少量的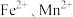 )为原料制备
)为原料制备 的实验流程如下:
的实验流程如下:
(1)写出基态
 原子的电子排布式:
原子的电子排布式: 中
中 元素的化合价为
元素的化合价为(2)写出“氧化除锰”时反应的离子方程式:
(3)常温下“调节
 ”时,试剂
”时,试剂 可选用
可选用 物质的量浓度为
物质的量浓度为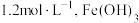 的
的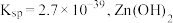 的
的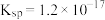 ,则
,则 的调节范围为
的调节范围为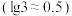 。已知:当溶液中离子浓度小于或等于
。已知:当溶液中离子浓度小于或等于 ,认为该离子已除尽。
,认为该离子已除尽。(4)写出“沉锌”时反应的离子方程式:
(5)“滤液”中的主要成分的用途:
(6)
 经焙解得到的活性
经焙解得到的活性 晶胞结构如图所示。该晶胞中
晶胞结构如图所示。该晶胞中 原子的配位数为
原子的配位数为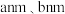 ,则该晶胞的密度为
,则该晶胞的密度为 。(写出计算表达式即可)
。(写出计算表达式即可)
您最近一年使用:0次
2023-12-18更新
|
190次组卷
|
2卷引用:福建省龙岩市一级校联盟2023-2024学年高三上学期半期考联考化学试题
名校
解题方法
7 . 完成下列小题
(1) 溶液含中,含
溶液含中,含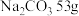 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度_____  。
。
(2)对于反应: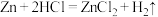 ,现有
,现有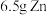 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有_____ 。
(3)对于反应: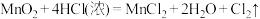 。
。
①用双线桥法表示上述反应电子转移的方向和数目_____ 。
②上述反应中还原剂是_____ ,若该反应有中有 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量_____ g,生成氯在气在STP时体积是_____ L。
③若使用浓盐酸的质量分数0.365、密度 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是_____  。
。
(1)
 溶液含中,含
溶液含中,含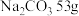 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度 。
。(2)对于反应:
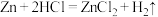 ,现有
,现有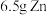 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有(3)对于反应:
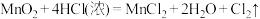 。
。①用双线桥法表示上述反应电子转移的方向和数目
②上述反应中还原剂是
 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量③若使用浓盐酸的质量分数0.365、密度
 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是 。
。
您最近一年使用:0次
名校
8 . 以甲烷为燃料、含铜氧化物为载体的化学链燃烧过程如图所示,下列说法不正确的是


| A.该流程中无需补充CuO |
B.空气反应器中的反应为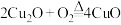 |
C.理论上燃料反应器中每产生22.0g ,空气反应器中要消耗标况下11.2L ,空气反应器中要消耗标况下11.2L |
D.该流程比传统燃烧更有利于捕集 |
您最近一年使用:0次
解题方法
9 . 工业废水中常含有一定量有毒的 和
和 ,需进行处理后再排放。处理含
,需进行处理后再排放。处理含 和
和 的工业废水常用的方法有两种。
的工业废水常用的方法有两种。
方法一:还原沉淀法。
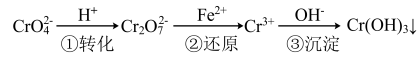
(1)请写出第①步中 与
与 在溶液中存在的平衡:
在溶液中存在的平衡:___________ ,下列能说明该反应达到平衡状态的是___________ (填标号)。
A. 与
与 的物质的量相等
的物质的量相等
B.溶液颜色不变
C.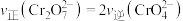
(2)第②步中,每 可还原
可还原___________  ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
方法二:电解法。用石墨和Fe作电极电解含 的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近
的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近 将
将 还原为
还原为 ,最后
,最后 以
以 形式沉淀。
形式沉淀。
(3)在电解除铬的过程中,石墨电极为___________ (填“阴极”或“阳极”),Fe电极的电极反应式为___________ 。
(4)在阴极附近溶液pH升高的原因是___________ (填电极反应式及必要的文字)。
(5)当Fe电极质量减小3.36g时,理论上可处理___________ (填含a的表达式)L含 的酸性废水。
的酸性废水。
 和
和 ,需进行处理后再排放。处理含
,需进行处理后再排放。处理含 和
和 的工业废水常用的方法有两种。
的工业废水常用的方法有两种。方法一:还原沉淀法。

(1)请写出第①步中
 与
与 在溶液中存在的平衡:
在溶液中存在的平衡:A.
 与
与 的物质的量相等
的物质的量相等B.溶液颜色不变
C.
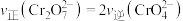
(2)第②步中,每
 可还原
可还原 ,该反应的离子方程式为
,该反应的离子方程式为方法二:电解法。用石墨和Fe作电极电解含
 的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近
的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近 将
将 还原为
还原为 ,最后
,最后 以
以 形式沉淀。
形式沉淀。(3)在电解除铬的过程中,石墨电极为
(4)在阴极附近溶液pH升高的原因是
(5)当Fe电极质量减小3.36g时,理论上可处理
 的酸性废水。
的酸性废水。
您最近一年使用:0次
10 . 乙醛是一种重要的二碳试剂,其某种合成机理如图所示。下列说法错误的是
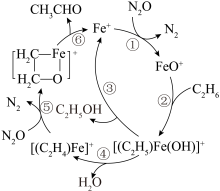
| A.Fe+是该反应的催化剂 |
| B.C2H5OH是合成过程中的副产物 |
C.该合成乙醛的反应为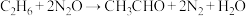 |
| D.及时分离出C2H5OH,有利于提高CH3CHO的产率 |
您最近一年使用:0次
2023-12-04更新
|
150次组卷
|
2卷引用:2024届福建省福州延安中学高三下学期高考第二次模拟化学试题



