1 . 基态锇原子( )的价电子排布式为
)的价电子排布式为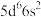 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有
常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有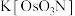 。有关反应如下:
。有关反应如下:
反应I:
反应Ⅱ:
 )的价电子排布式为
)的价电子排布式为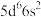 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有
常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有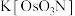 。有关反应如下:
。有关反应如下:反应I:

反应Ⅱ:

反应IⅢ:
A. 的立体异构分子中不存在手性分子 的立体异构分子中不存在手性分子 |
B.反应I中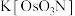 的 的 的化合价为+8 的化合价为+8 |
| C.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶1 |
D.由反应Ⅲ可推测氧化性: 强于酸性 强于酸性 溶液 溶液 |
您最近一年使用:0次
2 . 锰及其化合物在工业生产中具有重要用途。某兴趣小组用软锰矿(主要成分是 ,含少量
,含少量 、
、 )和黄铁矿(主要成分是
)和黄铁矿(主要成分是 ,含少量)为原料制备
,含少量)为原料制备 ,实验流程如下:
,实验流程如下: 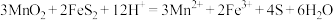
(1)与稀硫酸反应前,将黄铁矿和软锰矿混合研磨的目的是_______ 。
(2)离子反应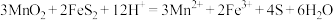 中,被氧化的元素是
中,被氧化的元素是_______ 和_______ 。
(3)步骤(Ⅰ)中分离溶液和沉淀的操作名称是_______ ,所需要的玻璃仪器除烧杯和玻璃棒外,还需要_______ 。
(4)步骤(Ⅱ)中加入NaOH溶液调节pH,是为了完全沉淀 、
、 ,写出生成
,写出生成 沉淀的离子方程式:
沉淀的离子方程式:_______ 。
(5)将步骤(Ⅲ)中发生反应的离子方程式补充完整:______ 。
 _______
_______
 ,含少量
,含少量 、
、 )和黄铁矿(主要成分是
)和黄铁矿(主要成分是 ,含少量)为原料制备
,含少量)为原料制备 ,实验流程如下:
,实验流程如下: 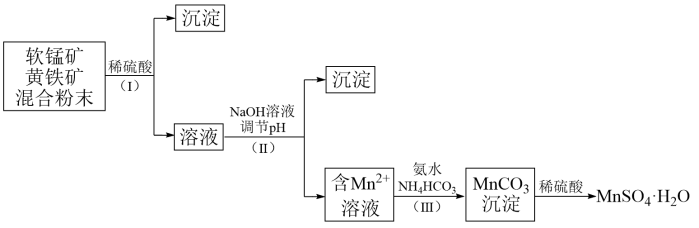
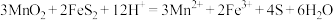
(1)与稀硫酸反应前,将黄铁矿和软锰矿混合研磨的目的是
(2)离子反应
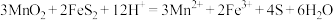 中,被氧化的元素是
中,被氧化的元素是(3)步骤(Ⅰ)中分离溶液和沉淀的操作名称是
(4)步骤(Ⅱ)中加入NaOH溶液调节pH,是为了完全沉淀
 、
、 ,写出生成
,写出生成 沉淀的离子方程式:
沉淀的离子方程式:(5)将步骤(Ⅲ)中发生反应的离子方程式补充完整:
 _______
_______
您最近一年使用:0次
2024-03-29更新
|
153次组卷
|
2卷引用:福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷(学考)
3 . 兴趣小组设计以下实验,探究MnOx氧化甲苯蒸气(还原产物为MnO)生成无污染气体的效果。
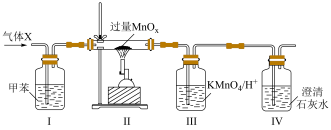
下列说法错误 的是

下列说法
| A.气体X可以是氮气 |
| B.通过Ⅲ、Ⅳ中现象可判断甲苯是否被MnOx完全氧化 |
| C.若n(甲苯):n(MnOx)=1:36发生反应,则x=1.5 |
| D.装置Ⅲ、Ⅳ互换顺序仍可判断甲苯是否被完全氧化 |
您最近一年使用:0次
名校
4 .  是一种光催化材料。工业利用某废催化剂(主要含
是一种光催化材料。工业利用某废催化剂(主要含 、
、 、NiO及少量
、NiO及少量 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下: 、NiO都是不溶于水的碱性氧化物
、NiO都是不溶于水的碱性氧化物
Ⅱ.0.1
 溶液的pH=1.0
溶液的pH=1.0
Ⅲ.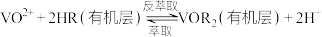
回答下列问题:
(1)滤渣的主要成分是___________ ;酸化时, 完全转化为
完全转化为 的最大pH为
的最大pH为___________ 。(已知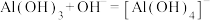
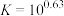 ;离子浓度≤10-5mol/L时沉淀完全)
;离子浓度≤10-5mol/L时沉淀完全)
(2)“酸化”后的溶液中存在 ,则“还原”时发生反应的离子方程式为
,则“还原”时发生反应的离子方程式为___________ 。
(3)反萃取剂应选用___________ (填“酸性”、“中性”或“碱性”)溶液;若“萃取”、“反萃取”的过程中钒的总回收率为90%,则“还原”时加入的 和“氧化”时加入的
和“氧化”时加入的 的物质的量之比为
的物质的量之比为___________ 。
(4)生成 的化学方程式为
的化学方程式为___________ ,实验测得溶液pH、温度和 溶液浓度对生成
溶液浓度对生成 的粒径影响图像如下:
的粒径影响图像如下: 晶体的最佳条件是
晶体的最佳条件是___________ ;制备过程中需加入NaOH维持最佳pH,若 过量,需要增加NaOH的用量,原因是
过量,需要增加NaOH的用量,原因是___________ 。
 是一种光催化材料。工业利用某废催化剂(主要含
是一种光催化材料。工业利用某废催化剂(主要含 、
、 、NiO及少量
、NiO及少量 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下: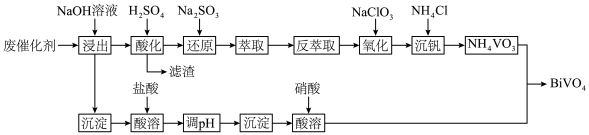
 、NiO都是不溶于水的碱性氧化物
、NiO都是不溶于水的碱性氧化物Ⅱ.0.1

 溶液的pH=1.0
溶液的pH=1.0Ⅲ.
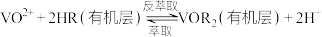
回答下列问题:
(1)滤渣的主要成分是
 完全转化为
完全转化为 的最大pH为
的最大pH为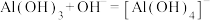
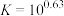 ;离子浓度≤10-5mol/L时沉淀完全)
;离子浓度≤10-5mol/L时沉淀完全)(2)“酸化”后的溶液中存在
 ,则“还原”时发生反应的离子方程式为
,则“还原”时发生反应的离子方程式为(3)反萃取剂应选用
 和“氧化”时加入的
和“氧化”时加入的 的物质的量之比为
的物质的量之比为(4)生成
 的化学方程式为
的化学方程式为 溶液浓度对生成
溶液浓度对生成 的粒径影响图像如下:
的粒径影响图像如下: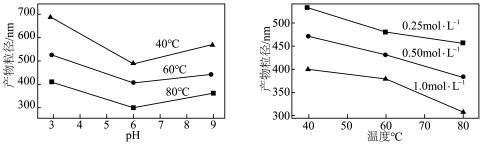
 晶体的最佳条件是
晶体的最佳条件是 过量,需要增加NaOH的用量,原因是
过量,需要增加NaOH的用量,原因是
您最近一年使用:0次
2024-03-14更新
|
1380次组卷
|
7卷引用:2024届福建省福州延安中学高三下学期高考第二次模拟化学试题
2024届福建省福州延安中学高三下学期高考第二次模拟化学试题山东省烟台市2024届高三一模化学试题2024届山东省高三下学期第一次练兵考试一模化学试题山东省德州市2023-2024学年高三下学期一模考试化学试题河北省石家庄市第二中学2023-2024学年高三下3月T8联考化学试题(已下线)化学(山东卷01)-2024年高考押题预测卷(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
5 . 下图为氯元素的“价-类”二维图,下列说法错误的是
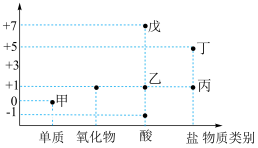

| A.甲可以通过一步反应生成乙 | B.丙的焰色为紫色,则丙为 |
| C.丁可用于实验室制取氧气 | D.戊中氯元素只具有氧化性 |
您最近一年使用:0次
6 . 下列生产生活现象对应的解释错误 的是
选项 | 生产生活现象 | 对应的解释 |
A | 铵态氨肥不能与碱性物质混合施用 | 二者能发生反应 |
B | “卤水”点豆腐 | 电解质与胶体发生化学反应 |
C | 补铁剂与维C共服,促进铁元素的吸收 | 维C具有还原性 |
D | 戴N95口罩防流感病毒 | N95口罩有吸附、过滤等作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。错误 的是

A.过程①: |
B.过程②总反应式: |
C.过程③: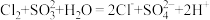 |
D. 溶于水: 溶于水: |
您最近一年使用:0次
2024-03-06更新
|
1112次组卷
|
5卷引用:福建省泉州市2024届高三下学期高中毕业班质量监测(三)化学试卷
福建省泉州市2024届高三下学期高中毕业班质量监测(三)化学试卷云南省云南师范大学实验中学2023-2024学年高一下学期三月月考化学试题(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题(已下线)压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
8 . 甲钴胺是神经元营养药物,由C、H、Co、N、O、P元素组成。下列说法正确的是
A.还原性: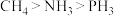 |
| B.基态P原子的最高能级轨道形状为球形 |
| C.同周期中第一电离能小于N的元素有5种 |
D.基态Co原子价层电子轨道表示式为 |
您最近一年使用:0次
2024-02-24更新
|
165次组卷
|
2卷引用:福建省漳州市华安县第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
9 . 酸浸法回收废炉渣中(主要为铜、钴、镍、铁等金属元素的氧化物)的铜、钴、镍的流程如下: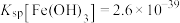 ,
, 。
。
(1)“磨细”过程的目的是_______ 。
(2)酸浸液中大量铁元素以 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为_______ 。
(3)“滤渣2”主要成分为_______ (填化学式)。
(4)“镍钴分离”过程 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)“酸溶1”过程用 替换
替换 ,从绿色化学角度分析其可行性
,从绿色化学角度分析其可行性_______ 。
(6)“焙烧”过程发生反应的化学方程式为_______ 。
(7)已知当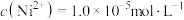 时,认为其沉淀完全。“沉镍”过程的目的是为了将“
时,认为其沉淀完全。“沉镍”过程的目的是为了将“ ”,此时应调节溶液的pH为
”,此时应调节溶液的pH为_______ 。
(8)“操作X”为_______ 。
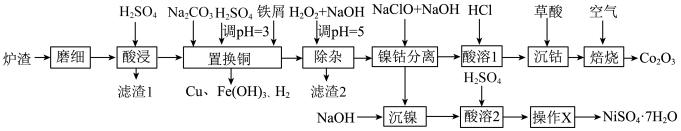
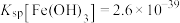 ,
, 。
。(1)“磨细”过程的目的是
(2)酸浸液中大量铁元素以
 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为(3)“滤渣2”主要成分为
(4)“镍钴分离”过程
 发生反应的离子方程式为
发生反应的离子方程式为(5)“酸溶1”过程用
 替换
替换 ,从绿色化学角度分析其可行性
,从绿色化学角度分析其可行性(6)“焙烧”过程发生反应的化学方程式为
(7)已知当
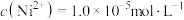 时,认为其沉淀完全。“沉镍”过程的目的是为了将“
时,认为其沉淀完全。“沉镍”过程的目的是为了将“ ”,此时应调节溶液的pH为
”,此时应调节溶液的pH为(8)“操作X”为
您最近一年使用:0次
2024-02-20更新
|
488次组卷
|
2卷引用:福建省2024届名校联盟全国优质校高三大联考化学试题
名校
解题方法
10 . 在无水无氧条件下制备新型锂离子电池电解质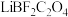 ,其过程可表示为:
,其过程可表示为:
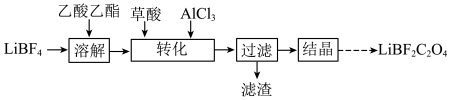
(1)草酸的结构简式为 ,
,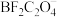 具有五元环结构,
具有五元环结构, 原子的轨道杂化类型是
原子的轨道杂化类型是 ,其结构式可表示为
,其结构式可表示为___________ 。
(2)实验室可以在 用浓硝酸在硝酸汞催化下氧化乙炔(
用浓硝酸在硝酸汞催化下氧化乙炔( )气体来制备草酸,主要装置如图所示。
)气体来制备草酸,主要装置如图所示。
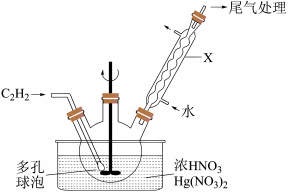
①仪器 的名称为
的名称为___________ ;
②用电石制得的 含有
含有 杂质,通过计算平衡常数说明用
杂质,通过计算平衡常数说明用 溶液除去
溶液除去 气体的可行性
气体的可行性___________ ;(常温下, ,
, 的
的 ,
,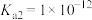 )
)
③装置中浓硝酸的还原产物为 ,生成草酸的化学方程式为
,生成草酸的化学方程式为___________ ,当硝酸的质量分数超过 或温度高于
或温度高于 ,草酸的产率开始下降,其原因分别是
,草酸的产率开始下降,其原因分别是___________ 。
(3) 遇水剧烈水解。
遇水剧烈水解。 和
和 混合加热制取无水
混合加热制取无水 时,
时, 的作用是
的作用是___________ 。
(4)“溶解”和“转化”操作在如图所示装置中进行。“溶解”时的操作依次为:称取一定质量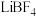 置于三颈瓶中→
置于三颈瓶中→___________ →搅拌直至完全溶解(填字母)。
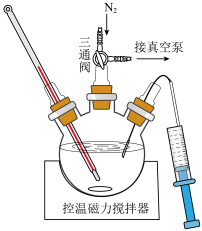
a.注入乙酸乙酯→充入→抽真空
b.抽真空→注入乙酸乙酯→充入
c.抽真空→充入 →注入乙酸乙酯
→注入乙酸乙酯
(5)产品(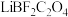 )纯度的测定
)纯度的测定
步骤1:称取 样品(假设只含
样品(假设只含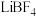 杂质)配制成
杂质)配制成 溶液。(
溶液。(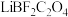 在水中可分解出草酸根,
在水中可分解出草酸根,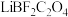 相对分子质量为144)
相对分子质量为144)
步骤2:量取 所配制的溶液于锥形瓶中,用
所配制的溶液于锥形瓶中,用 酸性
酸性 溶液滴定三次,平均消耗体积为
溶液滴定三次,平均消耗体积为 。产品(
。产品(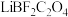 )的质量分数为
)的质量分数为___________ (列式即可,不用化简)。
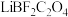 ,其过程可表示为:
,其过程可表示为:
(1)草酸的结构简式为
 ,
,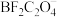 具有五元环结构,
具有五元环结构, 原子的轨道杂化类型是
原子的轨道杂化类型是 ,其结构式可表示为
,其结构式可表示为(2)实验室可以在
 用浓硝酸在硝酸汞催化下氧化乙炔(
用浓硝酸在硝酸汞催化下氧化乙炔( )气体来制备草酸,主要装置如图所示。
)气体来制备草酸,主要装置如图所示。
①仪器
 的名称为
的名称为②用电石制得的
 含有
含有 杂质,通过计算平衡常数说明用
杂质,通过计算平衡常数说明用 溶液除去
溶液除去 气体的可行性
气体的可行性 ,
, 的
的 ,
,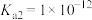 )
)③装置中浓硝酸的还原产物为
 ,生成草酸的化学方程式为
,生成草酸的化学方程式为 或温度高于
或温度高于 ,草酸的产率开始下降,其原因分别是
,草酸的产率开始下降,其原因分别是(3)
 遇水剧烈水解。
遇水剧烈水解。 和
和 混合加热制取无水
混合加热制取无水 时,
时, 的作用是
的作用是(4)“溶解”和“转化”操作在如图所示装置中进行。“溶解”时的操作依次为:称取一定质量
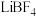 置于三颈瓶中→
置于三颈瓶中→
a.注入乙酸乙酯→充入→抽真空
b.抽真空→注入乙酸乙酯→充入

c.抽真空→充入
 →注入乙酸乙酯
→注入乙酸乙酯(5)产品(
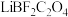 )纯度的测定
)纯度的测定步骤1:称取
 样品(假设只含
样品(假设只含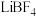 杂质)配制成
杂质)配制成 溶液。(
溶液。(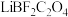 在水中可分解出草酸根,
在水中可分解出草酸根,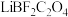 相对分子质量为144)
相对分子质量为144)步骤2:量取
 所配制的溶液于锥形瓶中,用
所配制的溶液于锥形瓶中,用 酸性
酸性 溶液滴定三次,平均消耗体积为
溶液滴定三次,平均消耗体积为 。产品(
。产品(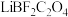 )的质量分数为
)的质量分数为
您最近一年使用:0次



