名校
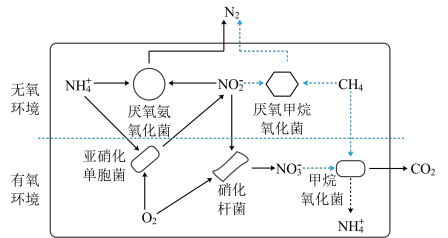
1 . 微生物反应器去除废水中铵盐和甲烷的过程如图。
(1) 的电离方程式为
的电离方程式为_______ 。
(2)Cu和稀硝酸反应的化学方程式为_______ ,反应过程体现了硝酸性质中的________ 。
(3)在厌氧氨氧化菌作用下,转移 电子时产生
电子时产生 的物质的量为
的物质的量为_______ 。
(4)甲烷属于________ (填“电解质”或“非电解质”)。在酸性废水中,甲烷氧化菌催化甲烷转化的离子方程式为_______ 。
(1)
 的电离方程式为
的电离方程式为(2)Cu和稀硝酸反应的化学方程式为
(3)在厌氧氨氧化菌作用下,转移
 电子时产生
电子时产生 的物质的量为
的物质的量为(4)甲烷属于
您最近一年使用:0次
2024-02-02更新
|
66次组卷
|
2卷引用:福建省厦门市2023-2024学年高一上学期期末质量检测化学试题
解题方法
2 . 元素的“价-类”二维图是学习元素及其化合物相关知识的重要模型和工具,下图为硫元素的“价-类”二维图。
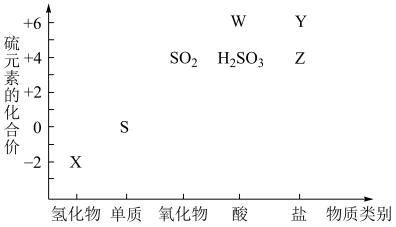
回答下列问题:
(1)X的化学式为___________ 。
(2)将 通入以下溶液均会发生颜色变化,其中体现
通入以下溶液均会发生颜色变化,其中体现 还原性的是___________(填标号)。
还原性的是___________(填标号)。
(3)W的浓溶液与金属铜反应的化学方程式为___________ 。
(4)焦硫酸钠( )在“价-类”二维图中的位置是
)在“价-类”二维图中的位置是___________ (填“Y”或“Z”)。
(5)大苏打( )在电影、纺织、农药等方面均有重要作用。从氧化还原角度分析,实验室制备
)在电影、纺织、农药等方面均有重要作用。从氧化还原角度分析,实验室制备 ,下列药品组合合理的是___________(填标号)。
,下列药品组合合理的是___________(填标号)。
(6)某部门收集的雨水样品在不同时间测得的 如下表,该雨水样品露置于空气中酸性逐渐增强,这一过程发生反应的化学方程式为
如下表,该雨水样品露置于空气中酸性逐渐增强,这一过程发生反应的化学方程式为___________ 。
(7)为了测定某工厂尾气中 的含量,将标准状况下
的含量,将标准状况下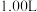 尾气通入足量
尾气通入足量 溶液,再加入足量
溶液,再加入足量 溶液(尾气中其它成分不反应),充分反应后过滤、洗涤、干燥、称量,得到
溶液(尾气中其它成分不反应),充分反应后过滤、洗涤、干燥、称量,得到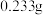 沉淀。则尾气中
沉淀。则尾气中 的体积分数为
的体积分数为___________ 。

回答下列问题:
(1)X的化学式为
(2)将
 通入以下溶液均会发生颜色变化,其中体现
通入以下溶液均会发生颜色变化,其中体现 还原性的是___________(填标号)。
还原性的是___________(填标号)。| A.使溴水褪色 | B.使品红溶液褪色 |
C.使滴有酚酞的 溶液褪色 溶液褪色 | D.使 溶液中出现淡黄色浑浊 溶液中出现淡黄色浑浊 |
(3)W的浓溶液与金属铜反应的化学方程式为
(4)焦硫酸钠(
 )在“价-类”二维图中的位置是
)在“价-类”二维图中的位置是(5)大苏打(
 )在电影、纺织、农药等方面均有重要作用。从氧化还原角度分析,实验室制备
)在电影、纺织、农药等方面均有重要作用。从氧化还原角度分析,实验室制备 ,下列药品组合合理的是___________(填标号)。
,下列药品组合合理的是___________(填标号)。A. | B. |
C. | D. |
(6)某部门收集的雨水样品在不同时间测得的
 如下表,该雨水样品露置于空气中酸性逐渐增强,这一过程发生反应的化学方程式为
如下表,该雨水样品露置于空气中酸性逐渐增强,这一过程发生反应的化学方程式为| 时间/h | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
 | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(7)为了测定某工厂尾气中
 的含量,将标准状况下
的含量,将标准状况下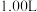 尾气通入足量
尾气通入足量 溶液,再加入足量
溶液,再加入足量 溶液(尾气中其它成分不反应),充分反应后过滤、洗涤、干燥、称量,得到
溶液(尾气中其它成分不反应),充分反应后过滤、洗涤、干燥、称量,得到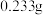 沉淀。则尾气中
沉淀。则尾气中 的体积分数为
的体积分数为
您最近一年使用:0次
3 . 科技工作者提出用铝粉处理含硝酸盐废水的思路,其原理为: ,每生成标准状况下
,每生成标准状况下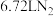 ,至少需要消耗
,至少需要消耗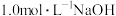 溶液的体积是多少?(写出计算过程)
溶液的体积是多少?(写出计算过程)____________
 ,每生成标准状况下
,每生成标准状况下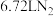 ,至少需要消耗
,至少需要消耗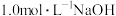 溶液的体积是多少?(写出计算过程)
溶液的体积是多少?(写出计算过程)
您最近一年使用:0次
名校
解题方法
4 . 根据题干信息,按要求回答问题:
(1)钠与氢气在加热条件下反应生成氢化钠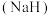 ,
, 在熔融状态下能导电。取少量氢化钠溶于水剧烈反应,生成碱性溶液和一种可燃性气体。写出钠与氢气反应的化学方程式
在熔融状态下能导电。取少量氢化钠溶于水剧烈反应,生成碱性溶液和一种可燃性气体。写出钠与氢气反应的化学方程式__________ 。写出 与
与 的反应的化学方程式
的反应的化学方程式___________ 。反应中 作
作__________ 剂。
(2)从元素化合价角度分析 的性质
的性质
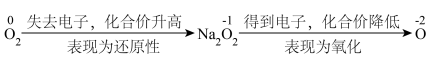
① 吸收
吸收 气体,生成
气体,生成 ,其化学方程式为
,其化学方程式为__________ 。
②在酸性高锰酸钾溶液中加入适量 粉末,溶液褪色,并产生无色气体,
粉末,溶液褪色,并产生无色气体, 表现出
表现出__________ 性,氧化产物是__________ 。
(1)钠与氢气在加热条件下反应生成氢化钠
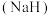 ,
, 在熔融状态下能导电。取少量氢化钠溶于水剧烈反应,生成碱性溶液和一种可燃性气体。写出钠与氢气反应的化学方程式
在熔融状态下能导电。取少量氢化钠溶于水剧烈反应,生成碱性溶液和一种可燃性气体。写出钠与氢气反应的化学方程式 与
与 的反应的化学方程式
的反应的化学方程式 作
作(2)从元素化合价角度分析
 的性质
的性质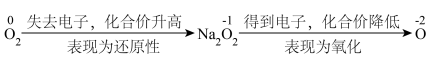
①
 吸收
吸收 气体,生成
气体,生成 ,其化学方程式为
,其化学方程式为②在酸性高锰酸钾溶液中加入适量
 粉末,溶液褪色,并产生无色气体,
粉末,溶液褪色,并产生无色气体, 表现出
表现出
您最近一年使用:0次
5 . 氧化还原反应是一种重要的化学反应类型,回答以下问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加入 和
和 ,即可得到
,即可得到 ,该反应的还原产物是
,该反应的还原产物是__________ 。
(2)高锰酸钾是常见的强氧化剂,若在高锰酸钾溶液中加入适量的稀硫酸可以使其氧化性更强。
①配平以下的离子方程式:______
____ ____
____ ____
____ ____
____ ____
____ ____
____
②能否用盐酸代替硫酸___________ ?(填“能”或“否”)
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加入
 和
和 ,即可得到
,即可得到 ,该反应的还原产物是
,该反应的还原产物是(2)高锰酸钾是常见的强氧化剂,若在高锰酸钾溶液中加入适量的稀硫酸可以使其氧化性更强。
①配平以下的离子方程式:
____
 ____
____ ____
____ ____
____ ____
____ ____
____
②能否用盐酸代替硫酸
您最近一年使用:0次
6 . Ⅰ.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图是硫元素的价类二维图,回答下列问题:

(1) 为
为______ (填物质的类别); 的化学式为
的化学式为______ ;
(2)某同学欲选用如图的部分装置和药品探究: 的性质。
的性质。
上述装置中能体现 具有氧化性的化学反应方程式为
具有氧化性的化学反应方程式为______________________________________ 。
(3)下图是工业上用黄铁矿(主要成分 )为原料制取绿矾(
)为原料制取绿矾(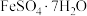 )的工艺流程,已知炉渣的主要成分是
)的工艺流程,已知炉渣的主要成分是 。请写出沸腾炉中发生的化学方程式:
。请写出沸腾炉中发生的化学方程式:______ 以及反应室中发生的化学方程式:______ ;实验小组在实验室模拟该工艺流程,用75g的黄铁矿制备出了139g绿矾,黄铁矿中 的质量分数约为
的质量分数约为______ 。

Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(4)二氧化氯是一种高效消毒剂。工业制备 的反应为:
的反应为:
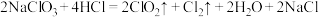
①氧化性:
______ (填“>”或“<”) 。
。
② 和
和 是常见的消毒剂,且还原产物均为
是常见的消毒剂,且还原产物均为 。现将二者的混合气体用足量的
。现将二者的混合气体用足量的 溶液吸收后得到1L的吸收液,并取10mL吸收液检验出
溶液吸收后得到1L的吸收液,并取10mL吸收液检验出 浓度为
浓度为 、
、 的浓度为
的浓度为 ,则原混合气体的物质的量为
,则原混合气体的物质的量为______ 。
(5)将下述氧化还原反应配平___________
______ +______
+______ +______
+______
 ______
______ +______
+______ +______
+______

(1)
 为
为 的化学式为
的化学式为(2)某同学欲选用如图的部分装置和药品探究:
 的性质。
的性质。
|
|
|
|
|
A | B | C | D | E |
 具有氧化性的化学反应方程式为
具有氧化性的化学反应方程式为(3)下图是工业上用黄铁矿(主要成分
 )为原料制取绿矾(
)为原料制取绿矾(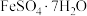 )的工艺流程,已知炉渣的主要成分是
)的工艺流程,已知炉渣的主要成分是 。请写出沸腾炉中发生的化学方程式:
。请写出沸腾炉中发生的化学方程式: 的质量分数约为
的质量分数约为
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(4)二氧化氯是一种高效消毒剂。工业制备
 的反应为:
的反应为: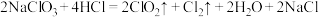
①氧化性:

 。
。②
 和
和 是常见的消毒剂,且还原产物均为
是常见的消毒剂,且还原产物均为 。现将二者的混合气体用足量的
。现将二者的混合气体用足量的 溶液吸收后得到1L的吸收液,并取10mL吸收液检验出
溶液吸收后得到1L的吸收液,并取10mL吸收液检验出 浓度为
浓度为 、
、 的浓度为
的浓度为 ,则原混合气体的物质的量为
,则原混合气体的物质的量为(5)将下述氧化还原反应配平
______
 +______
+______ +______
+______
 ______
______ +______
+______ +______
+______
您最近一年使用:0次
7 .  在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
I. 的性质探究
的性质探究
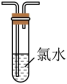
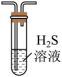
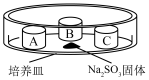
装置如下表(图)所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向 固体上滴加
固体上滴加 硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
(1)70%浓硫酸溶液和 固体反应制备
固体反应制备 的化学方程式为
的化学方程式为________________________________ 。
(2)瓶盖A中发生反应的化学方程式为________________________________ 。
(3)瓶盖A中无明显变化,若要证明A中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是_______ (填字母)。
a. 溶液 b.
溶液 b. 溶液 c.石蕊溶液
溶液 c.石蕊溶液
(4)瓶盖_______ (填字母)中的实验现象能证明 具有还原性,反应的离子方程式为
具有还原性,反应的离子方程式为______________ 。
(5)综合上述实验信息可证明 具有还原性、
具有还原性、___________________________________ 等性质。
(6)增加瓶盖D可验证 具有氧化性,则D中盛装的试剂及现象是
具有氧化性,则D中盛装的试剂及现象是__________________________ 。
II.化石燃料燃烧会产生大量的 ,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
(7)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是 小于
小于_______________ 的降雨。
(8)方法I中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为: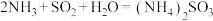 、
、__________ 。
(9)方法II中用 将
将 还原为S时,
还原为S时, 转化为
转化为_______________ (填化学式)。
(10)对方法III吸收 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的___________ 反应。
 在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。I.
 的性质探究
的性质探究装置如下表(图)所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向
 固体上滴加
固体上滴加 硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。实验装置 | 㼛盖 | 物质 | 实验现象 |
| A | 蒸馏水 | 无明显变化 |
B |
| 溶液褪色 | |
C | 蘸有品红溶液的棉花 | 品红溶液褪色 |
(1)70%浓硫酸溶液和
 固体反应制备
固体反应制备 的化学方程式为
的化学方程式为(2)瓶盖A中发生反应的化学方程式为
(3)瓶盖A中无明显变化,若要证明A中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是
a.
 溶液 b.
溶液 b. 溶液 c.石蕊溶液
溶液 c.石蕊溶液(4)瓶盖
 具有还原性,反应的离子方程式为
具有还原性,反应的离子方程式为(5)综合上述实验信息可证明
 具有还原性、
具有还原性、(6)增加瓶盖D可验证
 具有氧化性,则D中盛装的试剂及现象是
具有氧化性,则D中盛装的试剂及现象是II.化石燃料燃烧会产生大量的
 ,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。方法1 | 用氨水将 转化为 转化为 ,再氧化成 ,再氧化成 |
方法2 | 用生物质热解气(主要成分 、 、 、 、 )将 )将 在高温下还原成单质硫,其他生成物均可直接排放 在高温下还原成单质硫,其他生成物均可直接排放 |
方法3 | 用 溶液吸收 溶液吸收 ,再经电解转化为 ,再经电解转化为 |
(7)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是
 小于
小于(8)方法I中氨水吸收燃煤烟气中
 的化学反应为:
的化学反应为: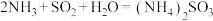 、
、(9)方法II中用
 将
将 还原为S时,
还原为S时, 转化为
转化为(10)对方法III吸收
 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
您最近一年使用:0次
2024-01-17更新
|
125次组卷
|
2卷引用:福建省厦门第一中学2023-2024学年高一上学期12月月考化学试题
名校
8 . 如图是自然界中不同价态硫元索之间的转化关系图,按要求回答问题:

(1)写出图中两种物质混合生成S,且S既是氧化产物又是还原产物的化学方程式____________________ 。
(2)工业生产硫酸的方法之一是:
①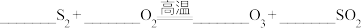 ,配平该反应方程式
,配平该反应方程式____________ ;
②__________________ ,写出该反应的方程式;
③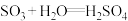 。
。
(3) 可用于焊接钢轨,写出该反应的化学方程式
可用于焊接钢轨,写出该反应的化学方程式___________________ 。
(4)硫酸是重要的化工原料,写出加热时铜和浓硫酸反应的化学方程式:____________________________ ,生成标准状况下 的还原性气体,转移的电子数为
的还原性气体,转移的电子数为_________________ 。

(1)写出图中两种物质混合生成S,且S既是氧化产物又是还原产物的化学方程式
(2)工业生产硫酸的方法之一是:
①
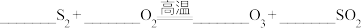 ,配平该反应方程式
,配平该反应方程式②
③
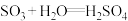 。
。(3)
 可用于焊接钢轨,写出该反应的化学方程式
可用于焊接钢轨,写出该反应的化学方程式(4)硫酸是重要的化工原料,写出加热时铜和浓硫酸反应的化学方程式:
 的还原性气体,转移的电子数为
的还原性气体,转移的电子数为
您最近一年使用:0次
名校
9 . 回答下列问题:
(1)从海水中得到的粗盐中常含 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入_______ 、_______ 、_______ 、稀盐酸来进行提纯。加入适量盐酸的目的是_______ 。
(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。
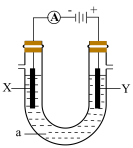
①写出该电解反应的化学方程式_______ 。
②简述检测Y极附近产生的气体的实验方案:_______
(3)下列方法可用于海水淡化的是_______ (填字母)。
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂, 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为_______ 。
②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:_______ 。
(5)目前很多自来水厂使用 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况_______ 。
(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为_______ 。
②软锰矿(主要成分 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为_______ 。
(1)从海水中得到的粗盐中常含
 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。

①写出该电解反应的化学方程式
②简述检测Y极附近产生的气体的实验方案:
(3)下列方法可用于海水淡化的是
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂,
 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:(5)目前很多自来水厂使用
 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和
 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为②软锰矿(主要成分
 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 按要求写出下列反应方程式(1-2书写化学方程式,3-5书写离子方程式)
(1)铝粉和氧化铁粉共热(铝热反应):___________ ;
(2)实验室用铜片和浓硫酸共热制备SO2:___________ ;
(3)FeSO4溶液储存时通常加入少量铁钉的原因:___________ ;
(4)高锰酸钾溶液不能用盐酸酸化的原因:___________ ;
(5)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原氯酸钠,可较安全地生成ClO2气体,反应的离子方程式为___________ 。
(1)铝粉和氧化铁粉共热(铝热反应):
(2)实验室用铜片和浓硫酸共热制备SO2:
(3)FeSO4溶液储存时通常加入少量铁钉的原因:
(4)高锰酸钾溶液不能用盐酸酸化的原因:
(5)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原氯酸钠,可较安全地生成ClO2气体,反应的离子方程式为
您最近一年使用:0次




 酸性溶液
酸性溶液

