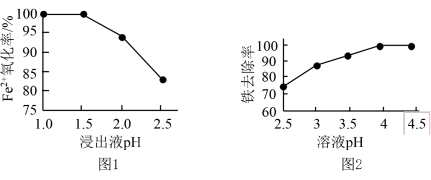
1 . 科研小组用氧化—沉淀法从废电池浸出液中去除铁:用MnO2氧化废电池浸出液中的Fe2+(酸性条件下,MnO2被还原为Mn2+),再加适量Na2CO3溶液调pH使Fe3+转化为Fe(OH)3沉淀。研究发现pH对Fe2+氧化率和铁去除率的影响如图1和图2所示。
下列说法错误的是

下列说法错误的是
| A.由图1可推断MnO2的氧化性随浸出液pH增大而减弱 |
| B.若起始浸出液pH=1,MnO2与Fe2+反应一段时间后,浸出液pH会减小 |
C.Fe3+转变为沉淀的离子方程式为2Fe3++3CO +3H2O=2Fe(OH)3↓+3CO2↑ +3H2O=2Fe(OH)3↓+3CO2↑ |
| D.推测若用NaHCO3溶液调pH也可以使Fe3+转化为Fe(OH)3沉淀 |
您最近一年使用:0次
2023-10-06更新
|
142次组卷
|
3卷引用:山东省部分学校2024届高三上学期10月大联考化学试题
9-10高二·山东·假期作业
2 . 在一定条件下,RO +2R2-+6H+=3R+3H2O,下列关于R元素的叙述中,一定正确的是
+2R2-+6H+=3R+3H2O,下列关于R元素的叙述中,一定正确的是
 +2R2-+6H+=3R+3H2O,下列关于R元素的叙述中,一定正确的是
+2R2-+6H+=3R+3H2O,下列关于R元素的叙述中,一定正确的是| A.R原子的最外层上有4个电子 | B. RO 中的R只能被还原 中的R只能被还原 |
| C.R的单质可能既有氧化性又有还原性 | D.H2RO3一定是强酸 |
您最近一年使用:0次
解题方法
3 . 硫酸氧矾(VOSO4)对高血糖、高血症等具有一定的治疗作用。制备VOSO4的实验流程及实验装置如图(夹持及加热装置已省略)。
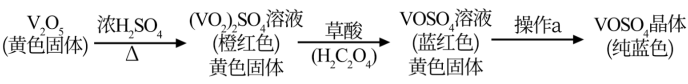
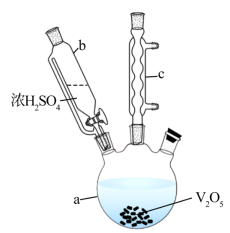
已知:草酸又名乙二酸,是一种二元有机弱酸,易溶于乙醇,可溶于水,不溶于苯,受热易分解,具有还原性。回答下列问题:
(1)仪器c的名称为___________ ,在a中反应生成(VO2)2SO4___________ (填“是”或“不是”)氧化还原反应。
(2)加入草酸前,为防止草酸因反应而减少,需对反应液采取的措施为___________ 、___________ 。
(3)反应液由橙红色变为蓝黑色的反应的化学方程式为___________ 。
(4)硫酸氧钒中钒含量的测定:
Ⅰ.制备VOSO4溶液:称取0. 51 g V2O5,置于上图装置中反应,V2O5全部转化为VOSO4。
Ⅱ.滴定预处理:
①将制得的VOSO4溶液配成250mL溶液;
②取25.00 mL溶液于锥形瓶中,滴加酸性高锰酸钾(可将VO2+转化为VO )溶液至反应完全;
)溶液至反应完全;
③滴加亚硝酸钠溶液反应掉过量的高锰酸钾溶液,加入2mL尿素溶液至溶液不再产生气泡。已知:尿素不直接与亚硝酸盐反应,但可将亚硝酸转化为氮气;亚硝酸可将VO 转化为VO2+。
转化为VO2+。
Ⅲ.滴定过程:加入10mL硫酸-磷酸混酸,调节pH=0,滴入指示剂,用0.05 mol·L−1硫酸亚铁铵标准溶液(将VO 转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
步骤③中加入尿素的目的是___________ ;测得硫酸氧钒中钒的质量分数为___________ (保留三位有效数字)。实验过程中,下列操作会导致所测钒含量偏低的是___________ 。
A.预处理过程中加入尿素的量不足
B.盛装硫酸亚铁铵标准液的滴定管未润洗
C.滴定管读数时,开始时仰视刻度线,结束时平视刻度线
D.滴定前滴定管有气泡,滴定结束后发现滴定管内无气泡


已知:草酸又名乙二酸,是一种二元有机弱酸,易溶于乙醇,可溶于水,不溶于苯,受热易分解,具有还原性。回答下列问题:
(1)仪器c的名称为
(2)加入草酸前,为防止草酸因反应而减少,需对反应液采取的措施为
(3)反应液由橙红色变为蓝黑色的反应的化学方程式为
(4)硫酸氧钒中钒含量的测定:
Ⅰ.制备VOSO4溶液:称取0. 51 g V2O5,置于上图装置中反应,V2O5全部转化为VOSO4。
Ⅱ.滴定预处理:
①将制得的VOSO4溶液配成250mL溶液;
②取25.00 mL溶液于锥形瓶中,滴加酸性高锰酸钾(可将VO2+转化为VO
 )溶液至反应完全;
)溶液至反应完全;③滴加亚硝酸钠溶液反应掉过量的高锰酸钾溶液,加入2mL尿素溶液至溶液不再产生气泡。已知:尿素不直接与亚硝酸盐反应,但可将亚硝酸转化为氮气;亚硝酸可将VO
 转化为VO2+。
转化为VO2+。Ⅲ.滴定过程:加入10mL硫酸-磷酸混酸,调节pH=0,滴入指示剂,用0.05 mol·L−1硫酸亚铁铵标准溶液(将VO
 转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。步骤③中加入尿素的目的是
A.预处理过程中加入尿素的量不足
B.盛装硫酸亚铁铵标准液的滴定管未润洗
C.滴定管读数时,开始时仰视刻度线,结束时平视刻度线
D.滴定前滴定管有气泡,滴定结束后发现滴定管内无气泡
您最近一年使用:0次
2021-12-09更新
|
674次组卷
|
5卷引用:山东省威海市文登区2021-2022学年高三上学期期中考试化学试题
山东省威海市文登区2021-2022学年高三上学期期中考试化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)
12-13高三上·山东泰安·期末
4 . 关于As的反应中,反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
①已知KBrO3在反应中得到电子,则该反应的还原剂是_______ 。
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为_______ 。
③根据上述反应可推知_______ 。(填序号)
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
④在该反应中,氧化剂与还原剂的物质的量之比为_______ 。
①已知KBrO3在反应中得到电子,则该反应的还原剂是
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
③根据上述反应可推知
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
④在该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
2021高三·山东·专题练习
解题方法
5 . 重铬酸钾(K2Cr2O7)是一种强氧化剂,在实验室和工业中都有很广泛的应用。某实验小组以铬铁矿[主要成分为FeO·Cr2O3,还含有少量的MgCO3、Al2O3、SiO2等]为原料,制备K2Cr2O7,流程如图:

已知:①酸化1后的溶液中含有Na2CrO4、Na2CO3等。
②NaNO2具有还原性,当溶液酸性很强时易被强氧化剂氧化。
(1)高温氧化时发生多个反应,其中Al2O3和SiO2分别转化为NaNO2和___________ ;FeO·Cr2O3参与反应的产物中含有Fe2O3、NaNO2等,该反应化学方程式为___________ 。
(2)滤渣1的成分为___________ 。
(3)为使溶液中铝元素尽可能生成沉淀而除去,则需调节溶液中Al3+、AlO 浓度均不超过10-6 mol·L-1.为达此目的酸化1溶液的pH范围是
浓度均不超过10-6 mol·L-1.为达此目的酸化1溶液的pH范围是___________ 。已知:Al(OH)3(s)  H+(aq)+AlO-(aq)+H2O(l) K=1×10-14;Ksp[Al(OH)3]=1×10-33
H+(aq)+AlO-(aq)+H2O(l) K=1×10-14;Ksp[Al(OH)3]=1×10-33
(4)酸化2时,酸化的作用是___________ ,在酸化时溶液酸性不能太强的原因是___________ 。
(5)称取K2Cr2O7,样品2.40 g,配成250 mL溶液,取25.00 mL于碘量瓶中,加入稀硫酸和足量碘化钾,并放于暗处,约6 min后加入适量水和数滴淀粉指示剂,用0.24 mol·L-1 Na2S2O3标准溶液滴定至终点(杂质不参与反应),共用去Na2S2O3标准溶液20.00 mL,所得样品中K2Cr2O7的质量分数为___________ 。
相关反应:(ⅰ)Cr2O +I-+H+-Cr3++I2+H2O (ⅱ)I2+2S2O
+I-+H+-Cr3++I2+H2O (ⅱ)I2+2S2O =2I-+S4O
=2I-+S4O

已知:①酸化1后的溶液中含有Na2CrO4、Na2CO3等。
②NaNO2具有还原性,当溶液酸性很强时易被强氧化剂氧化。
(1)高温氧化时发生多个反应,其中Al2O3和SiO2分别转化为NaNO2和
(2)滤渣1的成分为
(3)为使溶液中铝元素尽可能生成沉淀而除去,则需调节溶液中Al3+、AlO
 浓度均不超过10-6 mol·L-1.为达此目的酸化1溶液的pH范围是
浓度均不超过10-6 mol·L-1.为达此目的酸化1溶液的pH范围是 H+(aq)+AlO-(aq)+H2O(l) K=1×10-14;Ksp[Al(OH)3]=1×10-33
H+(aq)+AlO-(aq)+H2O(l) K=1×10-14;Ksp[Al(OH)3]=1×10-33(4)酸化2时,酸化的作用是
(5)称取K2Cr2O7,样品2.40 g,配成250 mL溶液,取25.00 mL于碘量瓶中,加入稀硫酸和足量碘化钾,并放于暗处,约6 min后加入适量水和数滴淀粉指示剂,用0.24 mol·L-1 Na2S2O3标准溶液滴定至终点(杂质不参与反应),共用去Na2S2O3标准溶液20.00 mL,所得样品中K2Cr2O7的质量分数为
相关反应:(ⅰ)Cr2O
 +I-+H+-Cr3++I2+H2O (ⅱ)I2+2S2O
+I-+H+-Cr3++I2+H2O (ⅱ)I2+2S2O =2I-+S4O
=2I-+S4O
您最近一年使用:0次
名校
解题方法
6 . 三氯化铬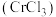 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为
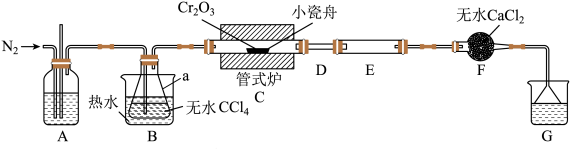
的反应为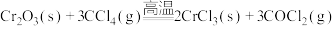 ,其实验装置(夹持仪器省略)如下图所示:
,其实验装置(夹持仪器省略)如下图所示:
已知:① (俗称光气)有毒,遇水发生水解:
(俗称光气)有毒,遇水发生水解: ;
;
②碱性条件下, 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。回答下列问题:
。回答下列问题:
(1)仪器a的名称是_____ ;反应结束后要继续通入一段时间氮气,主要目的是_______ 。
(2)实验过程中若D处出现堵塞,可观察到的现象是_______ ;可通过_______ (填操作)使实验继续进行。
(3)装置G中的液体是足量NaOH溶液,发生反应的离子方程式为_______ 。
(4)测定产品中 质量分数的实验步骤如下:
质量分数的实验步骤如下:
I.取mg 产品,在强碱性条件下,加入过量30%
产品,在强碱性条件下,加入过量30% 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;
II.冷却后,定容于100mL容量瓶中,准确移取上述溶液10.00ml,置于锥形瓶中,加入10ml蒸馏水,2mL浓硫酸和浓磷酸混酸(加浓磷酸的目的是为了防止指示剂提前变色),2滴二苯胺磺酸(指示剂),用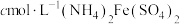 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液VmL(已知
标准溶液VmL(已知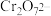 被
被 还原为
还原为 )。
)。
①产品中 质量分数表达式为
质量分数表达式为_______ 。
②下列操作将导致产品中 质量分数测定值偏高的是
质量分数测定值偏高的是_______ (填字母标号)。
a.步骤I中未继续加热一段时间
b.步骤II中未加浓磷酸
c.步骤III中所用 溶液已变质
溶液已变质
d.步骤III中达到滴定终点读数时,滴定管口有半滴悬液没有滴下
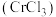 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为
的反应为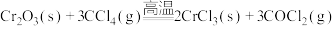 ,其实验装置(夹持仪器省略)如下图所示:
,其实验装置(夹持仪器省略)如下图所示:
已知:①
 (俗称光气)有毒,遇水发生水解:
(俗称光气)有毒,遇水发生水解: ;
;②碱性条件下,
 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。回答下列问题:
。回答下列问题:(1)仪器a的名称是
(2)实验过程中若D处出现堵塞,可观察到的现象是
(3)装置G中的液体是足量NaOH溶液,发生反应的离子方程式为
(4)测定产品中
 质量分数的实验步骤如下:
质量分数的实验步骤如下:I.取mg
 产品,在强碱性条件下,加入过量30%
产品,在强碱性条件下,加入过量30% 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;II.冷却后,定容于100mL容量瓶中,准确移取上述溶液10.00ml,置于锥形瓶中,加入10ml蒸馏水,2mL浓硫酸和浓磷酸混酸(加浓磷酸的目的是为了防止指示剂提前变色),2滴二苯胺磺酸(指示剂),用
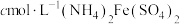 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液VmL(已知
标准溶液VmL(已知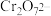 被
被 还原为
还原为 )。
)。①产品中
 质量分数表达式为
质量分数表达式为②下列操作将导致产品中
 质量分数测定值偏高的是
质量分数测定值偏高的是a.步骤I中未继续加热一段时间
b.步骤II中未加浓磷酸
c.步骤III中所用
 溶液已变质
溶液已变质d.步骤III中达到滴定终点读数时,滴定管口有半滴悬液没有滴下
您最近一年使用:0次
2023-01-16更新
|
269次组卷
|
3卷引用:山东省鄄城县第一中学2022-2023学年高三上学期期末考试化学试题
山东省鄄城县第一中学2022-2023学年高三上学期期末考试化学试题山东省菏泽市郓城县实验中学2022-2023学年高三上学期期末考试化学试题(已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(实验综合题)
名校
解题方法
7 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

已知:g为钠盐。
(1)按物质性质分类,c、d均属于___________ 氧化物。
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___________ (填化学式)。
(3)若将a与c混合可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)f的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为___________ 。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________ (填字母)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)c→e→f是硫酸型酸雨的形成途径之一、某地收集的雨水样品在不同时间测得pH如表所示,请用化学方程式解释该雨水样品随时间变化酸性逐渐增强的原因___________ 。

已知:g为钠盐。
(1)按物质性质分类,c、d均属于
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(3)若将a与c混合可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(4)f的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)c→e→f是硫酸型酸雨的形成途径之一、某地收集的雨水样品在不同时间测得pH如表所示,请用化学方程式解释该雨水样品随时间变化酸性逐渐增强的原因
| 时间/h | 0 | 2 | 4 | 6 | 8 | 10 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 |
您最近一年使用:0次
解题方法
8 . 含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。
已知:Cr3+ Cr(OH)3
Cr(OH)3 CrO
CrO
(1)含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O 与FeSO4溶液在酸性条件下反应的离子方程式
与FeSO4溶液在酸性条件下反应的离子方程式_______
②用离子方程式表示溶液pH不能超过10的原因_______
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和CrO 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
①写出阴极的电极反应式_______ 。
②电解法中加入氯化钠的作用是_______ 。
(3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为:_______ 。
②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。则B点时剩余固体的成分是_______ (填化学式)。

已知:Cr3+
 Cr(OH)3
Cr(OH)3 CrO
CrO
(1)含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O
 与FeSO4溶液在酸性条件下反应的离子方程式
与FeSO4溶液在酸性条件下反应的离子方程式②用离子方程式表示溶液pH不能超过10的原因
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和CrO
 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。①写出阴极的电极反应式
②电解法中加入氯化钠的作用是
(3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为:
②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。则B点时剩余固体的成分是

您最近一年使用:0次
9 . 重铬酸钾 是一种强氧化剂,在实验室和工业中都有很广泛的应用.某实验小组以铬铁矿[主要成分为
是一种强氧化剂,在实验室和工业中都有很广泛的应用.某实验小组以铬铁矿[主要成分为 ,还含有少量的
,还含有少量的 、
、 、
、 等]为原料,制备
等]为原料,制备 ,流程如图:
,流程如图:

已知:①酸化1后的溶液中含有 、
、 等。
等。
② 具有还原性,当溶液酸性很强时易被强氧化剂氧化。
具有还原性,当溶液酸性很强时易被强氧化剂氧化。
(1)高温氧化时发生多个反应,其中 和
和 分别转化为
分别转化为 和
和_______ ; 参与反应的产物中含有
参与反应的产物中含有 、
、 等,该反应化学方程式为
等,该反应化学方程式为_______ 。
(2)滤渣1的成分为_______ 。
(3)为使溶液中铝元素尽可能生成沉淀而除去,则需调节溶液中 、
、 浓度均不超过
浓度均不超过 .为达此目的酸化1溶液的
.为达此目的酸化1溶液的 范围是
范围是_______ 。已知: ;
;
(4)酸化2时,酸化的作用是_______ ,在酸化时溶液酸性不能太强的原因是_______ 。
(5)称取 ,样品
,样品 ,配成
,配成 溶液,取
溶液,取 于碘量瓶中,加入稀硫酸和足量碘化钾,并放于暗处,约
于碘量瓶中,加入稀硫酸和足量碘化钾,并放于暗处,约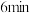 后加入适量水和数滴淀粉指示剂,用
后加入适量水和数滴淀粉指示剂,用 标准溶液滴定至终点(杂质不参与反应),共用去
标准溶液滴定至终点(杂质不参与反应),共用去 标准溶液
标准溶液 ,所得样品中
,所得样品中 的质量分数为
的质量分数为_______ 。相关反应:(ⅰ) (ⅱ)
(ⅱ)
 是一种强氧化剂,在实验室和工业中都有很广泛的应用.某实验小组以铬铁矿[主要成分为
是一种强氧化剂,在实验室和工业中都有很广泛的应用.某实验小组以铬铁矿[主要成分为 ,还含有少量的
,还含有少量的 、
、 、
、 等]为原料,制备
等]为原料,制备 ,流程如图:
,流程如图:
已知:①酸化1后的溶液中含有
 、
、 等。
等。②
 具有还原性,当溶液酸性很强时易被强氧化剂氧化。
具有还原性,当溶液酸性很强时易被强氧化剂氧化。(1)高温氧化时发生多个反应,其中
 和
和 分别转化为
分别转化为 和
和 参与反应的产物中含有
参与反应的产物中含有 、
、 等,该反应化学方程式为
等,该反应化学方程式为(2)滤渣1的成分为
(3)为使溶液中铝元素尽可能生成沉淀而除去,则需调节溶液中
 、
、 浓度均不超过
浓度均不超过 .为达此目的酸化1溶液的
.为达此目的酸化1溶液的 范围是
范围是 ;
;
(4)酸化2时,酸化的作用是
(5)称取
 ,样品
,样品 ,配成
,配成 溶液,取
溶液,取 于碘量瓶中,加入稀硫酸和足量碘化钾,并放于暗处,约
于碘量瓶中,加入稀硫酸和足量碘化钾,并放于暗处,约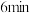 后加入适量水和数滴淀粉指示剂,用
后加入适量水和数滴淀粉指示剂,用 标准溶液滴定至终点(杂质不参与反应),共用去
标准溶液滴定至终点(杂质不参与反应),共用去 标准溶液
标准溶液 ,所得样品中
,所得样品中 的质量分数为
的质量分数为 (ⅱ)
(ⅱ)
您最近一年使用:0次
名校
解题方法
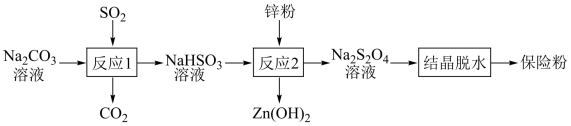
10 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO3还原法制备保险粉的流程如下:
下列说法错误的是

下列说法错误的是
| A.反应1说明酸性:H2SO3>H2CO3 |
| B.反应1结束后,可用盐酸酸化的 BaCl2溶液检验NaHSO3是否被氧化 |
| C.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2 |
| D.反应2最好在无氧条件下进行 |
您最近一年使用:0次
2021-01-25更新
|
2876次组卷
|
28卷引用:山东省聊城市第一中学2021届高三下学期开学模拟考试化学试题
山东省聊城市第一中学2021届高三下学期开学模拟考试化学试题(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)山东省泰安市新泰中学2021-2022学年高一上学期12月月考化学试题重庆市2021年普通高中学业水平选择考适应性测试化学试题天津市第一中学2020-2021学年高一下学期期中考试化学试题广东省广州市广州大学附属中学2020-2021学年高一下学期4月月考试题湖南省衡阳市第八中学2020-2021学年高一下学期期末考试化学试题(已下线)2021年秋季高三开学摸底考化学试卷03(江苏专用)江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期第一次阶段性诊断测试化学试题湖南省天壹名校联盟.宁乡市2021-2022学年高三11月调研考试化学试题湖南师范大学附属中学2021-2022学年高三上学期月考(三)化学试题福建省师范大学附属中学擎云级2021-2022学年高三上学期12月月考化学试题(已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练湖南省长沙市宁乡市2021-2022学年高三11月调研考试化学试题陕西省洋县中学2021-2022学年高一上学期期末考试化学试题(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)辽宁省沈阳市东北育才学校2021-2022高一下学期期中考试化学试题(已下线)第14讲 硫、二氧化硫【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)山西省长治市第二中学校2021-2022学年高一下学期第二次月考化学试题 河南省洛阳市2021-2022学年高一下学期期末质量检测化学试题重庆市璧山来凤中学校2022-2023学年高三10月月考化学试题福建省泉州科技中学2021-2022学年高三上学期期中考试化学试题福建省泉州科技中学2021-2022学年高三上学期期中考试化学试题 天津市实验中学2021-2022学年高三上学期第一次阶段考试化学试题 江西省丰城中学2023-2024学年高三上学期开学考试化学试题河南省南阳镇平一高2023-2024学年高一上学期化学学科训练试题黑龙江省哈尔滨师范大学青冈实验中学校2023-2024学年高三上学期12月份考试化学试题



