真题
解题方法
1 . 精炼铜产生的铜阳极泥富含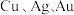 等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
(1) 位于元素周期表第
位于元素周期表第_______ 周期第_______ 族。
(2)“浸出液1”中含有的金属离子主要是_______ 。
(3)“浸取2”步骤中,单质金转化为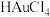 的化学方程式为
的化学方程式为_______ 。
(4)“浸取3”步骤中,“浸渣2”中的_______ (填化学式)转化为 。
。
(5)“电沉积”步骤中阴极的电极反应式为_______ 。“电沉积”步骤完成后,阴极区溶液中可循环利用的物质为_______ (填化学式)。
(6)“还原”步骤中,被氧化的 与产物
与产物 的物质的量之比为
的物质的量之比为_______ 。
(7) 可被
可被 氧化为
氧化为 。从物质结构的角度分析
。从物质结构的角度分析 的结构为(a)而不是(b)的原因:
的结构为(a)而不是(b)的原因:_______ 。
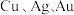 等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。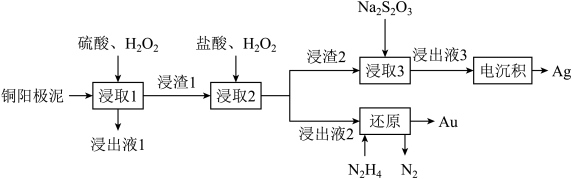
(1)
 位于元素周期表第
位于元素周期表第(2)“浸出液1”中含有的金属离子主要是
(3)“浸取2”步骤中,单质金转化为
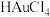 的化学方程式为
的化学方程式为(4)“浸取3”步骤中,“浸渣2”中的
 。
。(5)“电沉积”步骤中阴极的电极反应式为
(6)“还原”步骤中,被氧化的
 与产物
与产物 的物质的量之比为
的物质的量之比为(7)
 可被
可被 氧化为
氧化为 。从物质结构的角度分析
。从物质结构的角度分析 的结构为(a)而不是(b)的原因:
的结构为(a)而不是(b)的原因: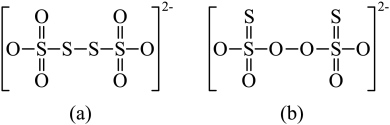
您最近一年使用:0次
名校
2 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。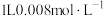 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
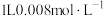 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.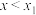 时, 时, 主要被氧化为 主要被氧化为 |
B.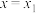 时,生成的 时,生成的 的物质的量为 的物质的量为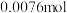 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次
名校
3 . NO、 、CO是常见的空气污染气体。在某分子筛的催化作用下,
、CO是常见的空气污染气体。在某分子筛的催化作用下, 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无害物质,其反应历程如图所示。下列说法不正确的是
,生成两种无害物质,其反应历程如图所示。下列说法不正确的是
 、CO是常见的空气污染气体。在某分子筛的催化作用下,
、CO是常见的空气污染气体。在某分子筛的催化作用下, 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无害物质,其反应历程如图所示。下列说法不正确的是
,生成两种无害物质,其反应历程如图所示。下列说法不正确的是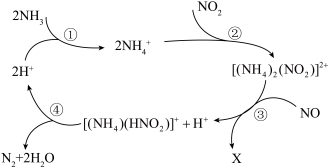
| A.历程中反应①②都是非氧化还原反应 |
B. 中不含有 中不含有 价的N 价的N |
C.X是 和 和 ,其中 ,其中 的电子式是 的电子式是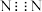 |
D.汽车尾气中的氮氧化合物主要是高温下气缸里的 、 、 反应产生的 反应产生的 |
您最近一年使用:0次
名校
4 . 镉(Cd)可用于制作某些发光电子组件。一种用铜镉废渣(含Cd、Zn、Cu、Fe等单质)为原料制备镉的工艺流程如图。
回答下列问题:
(1)“步骤II”需隔绝氧气的原因是___________ 。
(2)“氧化”时KMnO4的还原产物是MnO2,“步骤IV”中除铁发生的离子方程式___________ ,废渣成分除了MnO2还有___________ 。
(3)“置换”时镉置换率与 的关系如图,其中Zn的理论用量以溶液中Cd2+量为依据。实际生产中
的关系如图,其中Zn的理论用量以溶液中Cd2+量为依据。实际生产中 比值最佳为1.3,不宜超过该比值的原因是
比值最佳为1.3,不宜超过该比值的原因是___________ 。___________ 。(填化学式)
(5)“熔炼”时,海绵镉(含Cd和Zn)与NaOH在反应釜中混合反应,反应的化学方程式是___________ ,当反应釜内无明显气泡产生时停止加热,利用Ca与Na2ZnO2的___________ 不同,将Cd从反应釜下口放出,以达到分离的目的。
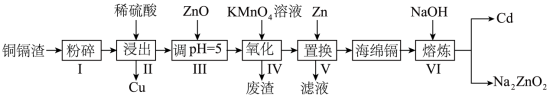
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)“步骤II”需隔绝氧气的原因是
(2)“氧化”时KMnO4的还原产物是MnO2,“步骤IV”中除铁发生的离子方程式
(3)“置换”时镉置换率与
 的关系如图,其中Zn的理论用量以溶液中Cd2+量为依据。实际生产中
的关系如图,其中Zn的理论用量以溶液中Cd2+量为依据。实际生产中 比值最佳为1.3,不宜超过该比值的原因是
比值最佳为1.3,不宜超过该比值的原因是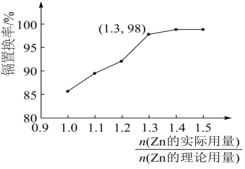
(5)“熔炼”时,海绵镉(含Cd和Zn)与NaOH在反应釜中混合反应,反应的化学方程式是
您最近一年使用:0次
名校
解题方法
5 . 钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题:
① 具有强氧化性。
具有强氧化性。
② ,
, 。
。
(1)为提高含钴废料的浸出效率,可采取的措施是___________ (任写一条)。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ ;浸出渣的主要成分为___________ (填化学式)。
(3)向“浸出液”中加入适量的 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)①“除钙镁”后,滤液中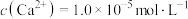 时,
时,
___________  。
。
②若“调pH”时溶液的pH偏低,将会导致 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
(5)将 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: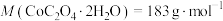 ,曲线中330℃及以上所得固体均为钴氧化物]
,曲线中330℃及以上所得固体均为钴氧化物] ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为___________ 。
 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题: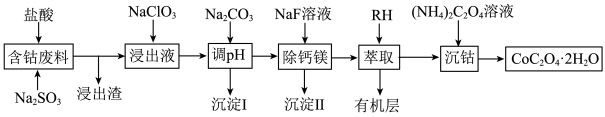
①
 具有强氧化性。
具有强氧化性。②
 ,
, 。
。(1)为提高含钴废料的浸出效率,可采取的措施是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)向“浸出液”中加入适量的
 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为(4)①“除钙镁”后,滤液中
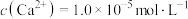 时,
时,
 。
。②若“调pH”时溶液的pH偏低,将会导致
 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是(5)将
 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: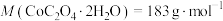 ,曲线中330℃及以上所得固体均为钴氧化物]
,曲线中330℃及以上所得固体均为钴氧化物]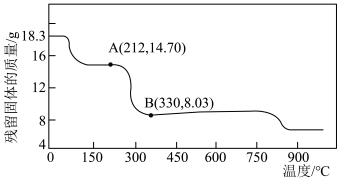
 ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为
您最近一年使用:0次
7日内更新
|
192次组卷
|
5卷引用:2024届河北省保定市十校高三下学期三模化学试题
名校
6 . 以黄铁矿为原料制硫酸会产生大量废渣,合理利用废渣可以减少环境污染,变废为宝。工业上利用废渣(含 、
、 的硫酸盐及少量CaO和MgO)制备高档颜料铁红
的硫酸盐及少量CaO和MgO)制备高档颜料铁红 ,同时回收
,同时回收 ,具体生产流程如图:
,具体生产流程如图:
(2)“过滤”操作所用到的玻璃仪器有___________ 。
(3)为了提高废渣的浸取率,可采取的措施有哪些?___________ (至少写出两点)。
(4)写出一种回收到的滤液的用途:___________ 。
(5)物质A的作用是___________ ,工业上物质A最好选用___________ (填标号)。
A.空气 B. C.
C. D.
D.
写出所选用试剂发生反应的离子方程式:___________ 。
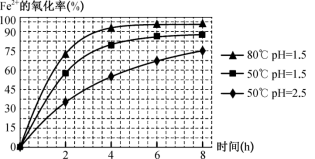
(6)根据如图所示的有关数据,你认为工业上进行“氧化”操作时应控制的条件有___________ (从温度、pH和氧化时间三方面说明)。
 、
、 的硫酸盐及少量CaO和MgO)制备高档颜料铁红
的硫酸盐及少量CaO和MgO)制备高档颜料铁红 ,同时回收
,同时回收 ,具体生产流程如图:
,具体生产流程如图: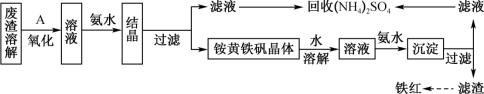
| A.水 | B.氢氧化钠溶液 | C.盐酸 | D.硫酸 |
(3)为了提高废渣的浸取率,可采取的措施有哪些?
(4)写出一种回收到的滤液的用途:
(5)物质A的作用是
A.空气 B.
 C.
C. D.
D.
写出所选用试剂发生反应的离子方程式:
(6)根据如图所示的有关数据,你认为工业上进行“氧化”操作时应控制的条件有
您最近一年使用:0次
名校
7 . 四氢铝钠(NaAlH4)是强还原剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 ,含少量
,含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:___________ (任写一个)。
(2)“转化”中 的具体作用是
的具体作用是___________ ;“分离”的操作是指___________ 。
(3)由 制备
制备 溶液的离子方程式为
溶液的离子方程式为___________ 。
(4)“沉铝”时通入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ ;所得滤液中的溶质有___________ (写化学式)。
(5)“合成”中,发生反应的化学方程式为(乙醚作溶剂,不参与反应)___________ 。
(6) 中氢的化合价为
中氢的化合价为___________ ;“有效氢”指单位质量(1g)含氢还原剂的还原能力相当于多少克氢气的还原能力。则 的“有效氢”为
的“有效氢”为___________ (保留三位有效数字)。
 )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 ,含少量
,含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题: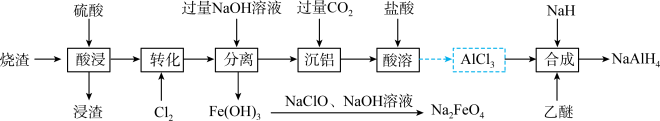
(2)“转化”中
 的具体作用是
的具体作用是(3)由
 制备
制备 溶液的离子方程式为
溶液的离子方程式为(4)“沉铝”时通入过量
 发生反应的离子方程式为
发生反应的离子方程式为(5)“合成”中,发生反应的化学方程式为(乙醚作溶剂,不参与反应)
(6)
 中氢的化合价为
中氢的化合价为 的“有效氢”为
的“有效氢”为
您最近一年使用:0次
8 . 碘化亚铁( )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)___________ ,若无此装置,写出铁粉参与的副反应的化学方程式:___________ 。
(2)硬质玻璃管直接接入收集器而不用导管的原因是___________ ,收集器浸泡在冷水中的原因是___________ 。
(3)试剂a的作用是___________ 。
(4)已知氧化性: 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:___________ 。
 )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)
(2)硬质玻璃管直接接入收集器而不用导管的原因是
(3)试剂a的作用是
(4)已知氧化性:
 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:
您最近一年使用:0次
9 .  在工业上有广泛的用途。以硫铁矿(主要成分为
在工业上有广泛的用途。以硫铁矿(主要成分为 )为原料制备
)为原料制备 的工艺流程如下图:
的工艺流程如下图:_______ (写出一种)。
(2)“操作”在实验室的名称为_______ ,需用到的玻璃仪器是_______ 、玻璃棒和烧杯。
(3)黄铁矿焙烧后得到的主要固体为 ,写出“焙烧”的化学方程式为
,写出“焙烧”的化学方程式为_______ 。
(4)“……”表示的操作为在_______ 气流中蒸发浓缩、_______ 、过滤。
(5)为防治 引起的污染,某工厂设计了新的治污方法,同时可得到化工产品
引起的污染,某工厂设计了新的治污方法,同时可得到化工产品 。该工艺流程如图所示,过程中起催化作用的物质是
。该工艺流程如图所示,过程中起催化作用的物质是_______ ,生成化工产品 的化学方程式为
的化学方程式为_______ 。 生产硫酸。用
生产硫酸。用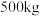 含
含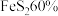 的硫铁矿,生产过程中硫损失
的硫铁矿,生产过程中硫损失 ,则可得
,则可得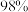 的硫酸
的硫酸_______  。
。
 在工业上有广泛的用途。以硫铁矿(主要成分为
在工业上有广泛的用途。以硫铁矿(主要成分为 )为原料制备
)为原料制备 的工艺流程如下图:
的工艺流程如下图: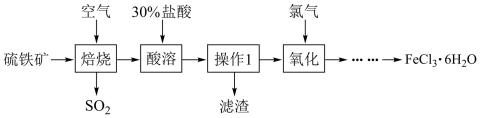
(2)“操作”在实验室的名称为
(3)黄铁矿焙烧后得到的主要固体为
 ,写出“焙烧”的化学方程式为
,写出“焙烧”的化学方程式为(4)“……”表示的操作为在
(5)为防治
 引起的污染,某工厂设计了新的治污方法,同时可得到化工产品
引起的污染,某工厂设计了新的治污方法,同时可得到化工产品 。该工艺流程如图所示,过程中起催化作用的物质是
。该工艺流程如图所示,过程中起催化作用的物质是 的化学方程式为
的化学方程式为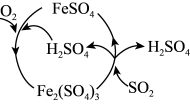
 生产硫酸。用
生产硫酸。用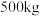 含
含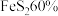 的硫铁矿,生产过程中硫损失
的硫铁矿,生产过程中硫损失 ,则可得
,则可得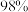 的硫酸
的硫酸 。
。
您最近一年使用:0次
名校
10 . 草酸亚铁晶体( )是常用的分析试剂,可通过
)是常用的分析试剂,可通过 [硫酸亚铁铵晶体,易氧化]与草酸反应制得。制备并测定草酸亚铁晶体组成的实验设计如下,回答下列问题
[硫酸亚铁铵晶体,易氧化]与草酸反应制得。制备并测定草酸亚铁晶体组成的实验设计如下,回答下列问题
实验步骤:(连接好装置后)
(i)……;
(ii)加入试剂;
(iii)打开d、c,加热,通入氨气制得硫酸铵;
(iv)……(a、b止水夹“操作1”),加入稀硫酸,产生 ,赶出装置内的空气,……(a、b止水夹“操作2”),将A中的硫酸亚铁压入到B中;
,赶出装置内的空气,……(a、b止水夹“操作2”),将A中的硫酸亚铁压入到B中;
(v)将B中溶液倒入蒸发皿中,经系列操作得到硫酸亚铁铵。
(1)操作(i)为_______ 。
(2)操作(iv)产生H2,赶出装置内的空气的目的为_______ ;a、b止水夹“操作2”为_______ 。
(3)用离子方程式表示装置B在操作(iii)时发生的反应_______ ;装置B中存在一处缺陷为_______ 。
Ⅱ.制备草酸亚铁晶体并测定其组成。
将制得的硫酸亚铁铵与草酸在一定条件下混合加热,经沉淀,抽滤、洗涤获得草酸亚铁晶体粗品。该草酸亚铁晶体 粗品中可能含有的杂质为
粗品中可能含有的杂质为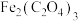 、
、 ,采用
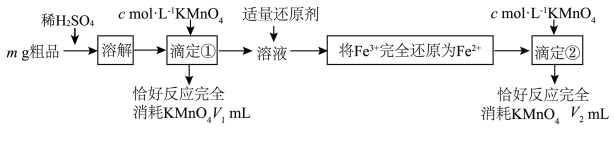
,采用 溶液滴定法测定该粗品的组成,实验过程如下图。
溶液滴定法测定该粗品的组成,实验过程如下图。
已知:草酸为弱酸,可被 溶液氧化为
溶液氧化为 。
。 ,还有
,还有_______ 。
(5)样品中所含 (摩尔质量为
(摩尔质量为 )的质量分数表达式
)的质量分数表达式_______ 。
 )是常用的分析试剂,可通过
)是常用的分析试剂,可通过 [硫酸亚铁铵晶体,易氧化]与草酸反应制得。制备并测定草酸亚铁晶体组成的实验设计如下,回答下列问题
[硫酸亚铁铵晶体,易氧化]与草酸反应制得。制备并测定草酸亚铁晶体组成的实验设计如下,回答下列问题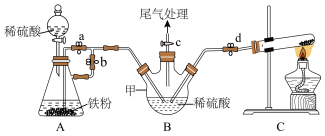
实验步骤:(连接好装置后)
(i)……;
(ii)加入试剂;
(iii)打开d、c,加热,通入氨气制得硫酸铵;
(iv)……(a、b止水夹“操作1”),加入稀硫酸,产生
 ,赶出装置内的空气,……(a、b止水夹“操作2”),将A中的硫酸亚铁压入到B中;
,赶出装置内的空气,……(a、b止水夹“操作2”),将A中的硫酸亚铁压入到B中;(v)将B中溶液倒入蒸发皿中,经系列操作得到硫酸亚铁铵。
(1)操作(i)为
(2)操作(iv)产生H2,赶出装置内的空气的目的为
(3)用离子方程式表示装置B在操作(iii)时发生的反应
Ⅱ.制备草酸亚铁晶体并测定其组成。
将制得的硫酸亚铁铵与草酸在一定条件下混合加热,经沉淀,抽滤、洗涤获得草酸亚铁晶体粗品。该草酸亚铁晶体
 粗品中可能含有的杂质为
粗品中可能含有的杂质为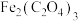 、
、 ,采用
,采用 溶液滴定法测定该粗品的组成,实验过程如下图。
溶液滴定法测定该粗品的组成,实验过程如下图。已知:草酸为弱酸,可被
 溶液氧化为
溶液氧化为 。
。
 ,还有
,还有(5)样品中所含
 (摩尔质量为
(摩尔质量为 )的质量分数表达式
)的质量分数表达式
您最近一年使用:0次



