1 . 室温下,实验测得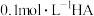 溶液的
溶液的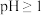 ,下列推理错误的是
,下列推理错误的是
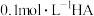 溶液的
溶液的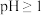 ,下列推理错误的是
,下列推理错误的是| A.NaA可能呈酸性 |
B.HA溶液中 |
C.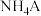 可能呈中性 可能呈中性 |
| D.若稀释HA溶液10倍,pH的数值增大1,则HA是强酸 |
您最近一年使用:0次
2 . Ⅰ.太空很神秘,水的世界也深不可测,从水作溶剂、水分子运动到水的电离、水与活泼金属反应等等。结合书本知识,回答下列问题:
(1)标准状况下,0.01 的NaOH溶液的pH
的NaOH溶液的pH_______ (填“>”“<”或“=”,下同)12,该温度下,水的离子积常数
_______  。
。
(2)T℃下,水的离子积曲线如图所示。_______ (填字母)。
a.T℃小于25℃
b.A点溶液pH=8
c.B点溶液呈碱性
d.保持温度不变,加入少量的酸可以实现从B点到C点的变化
②该温度下,将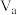 L pH=a NaOH溶液与
L pH=a NaOH溶液与 L
L 硫酸混合。
硫酸混合。
若所得混合溶液呈中性,且a=12,b=1,则
_______ ;若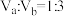 ,且a=11,b=3,则所得混合溶液的pH=
,且a=11,b=3,则所得混合溶液的pH=_______ 。
(3)现有以下五种电解质溶液,回答下列问题:
① ②NaOH ③
②NaOH ③ ④
④ ⑤
⑤
①浓度均为0.1 的五种溶液中导电能力最强的是
的五种溶液中导电能力最强的是_______ (填序号)。
②浓度均为0.1 的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为
的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为_______ (填序号)。
Ⅱ. 、
、 、
、 是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
回答下列问题:
(4)常温下,下列事实能说明 是弱电解质的是
是弱电解质的是_______ (填写序号)
① 与水能以任意比互溶
与水能以任意比互溶
②0.1mol/L 溶液导电能力比0.1mol/L盐酸弱
溶液导电能力比0.1mol/L盐酸弱
③常温下pH=3的 溶液稀释十倍后pH<4
溶液稀释十倍后pH<4
④ 溶液能与
溶液能与 溶液反应放出
溶液反应放出
⑤向 溶液中加入
溶液中加入 固体,溶液pH增大
固体,溶液pH增大
⑥大小相同的锌片与同体积同浓度的盐酸和 反应,产生
反应,产生 的物质的量相同
的物质的量相同
(5)已知 ,则常温下
,则常温下
 溶液的pH=
溶液的pH=_______ 。用水缓慢稀释该氨水的过程中,溶液中随着水量的增加,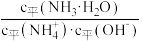
_______ 。(填“增大”“减小”或“不变”)
(1)标准状况下,0.01
 的NaOH溶液的pH
的NaOH溶液的pH
 。
。(2)T℃下,水的离子积曲线如图所示。
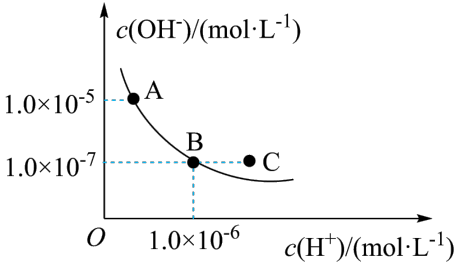
a.T℃小于25℃
b.A点溶液pH=8
c.B点溶液呈碱性
d.保持温度不变,加入少量的酸可以实现从B点到C点的变化
②该温度下,将
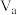 L pH=a NaOH溶液与
L pH=a NaOH溶液与 L
L 硫酸混合。
硫酸混合。若所得混合溶液呈中性,且a=12,b=1,则

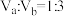 ,且a=11,b=3,则所得混合溶液的pH=
,且a=11,b=3,则所得混合溶液的pH=(3)现有以下五种电解质溶液,回答下列问题:
①
 ②NaOH ③
②NaOH ③ ④
④ ⑤
⑤
①浓度均为0.1
 的五种溶液中导电能力最强的是
的五种溶液中导电能力最强的是②浓度均为0.1
 的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为
的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为Ⅱ.
 、
、 、
、 是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
是中学化学中常见的物质,常温下,有关物质的电离常数如下表:| 物质 |  |  |  |
| 电离常数 | 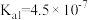 , ,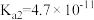 |  | 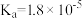 |
(4)常温下,下列事实能说明
 是弱电解质的是
是弱电解质的是①
 与水能以任意比互溶
与水能以任意比互溶②0.1mol/L
 溶液导电能力比0.1mol/L盐酸弱
溶液导电能力比0.1mol/L盐酸弱③常温下pH=3的
 溶液稀释十倍后pH<4
溶液稀释十倍后pH<4④
 溶液能与
溶液能与 溶液反应放出
溶液反应放出
⑤向
 溶液中加入
溶液中加入 固体,溶液pH增大
固体,溶液pH增大⑥大小相同的锌片与同体积同浓度的盐酸和
 反应,产生
反应,产生 的物质的量相同
的物质的量相同(5)已知
 ,则常温下
,则常温下
 溶液的pH=
溶液的pH=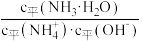
您最近一年使用:0次
3 . 在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,下列判断正确的是

| A.冰醋酸不导电,所以冰醋酸不是电解质 |
B.A、B、 三点对应的溶液中, 三点对应的溶液中, 由小到大的顺序是 由小到大的顺序是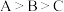 |
C.A、B、C三点对应的溶液中, 电离程度最大的B 电离程度最大的B |
D.若使B点对应的溶液中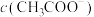 增大、 增大、 增大,可行的方法是加热 增大,可行的方法是加热 |
您最近一年使用:0次
4 . 电离方程式书写正确的是
A. | B.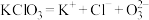 |
C. | D. |
您最近一年使用:0次
5 . 常温下,向某浓度 溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与
溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与 、
、 、
、 变化如图所示。下列说法错误的是
变化如图所示。下列说法错误的是
 溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与
溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与 、
、 、
、 变化如图所示。下列说法错误的是
变化如图所示。下列说法错误的是
| A.a到b的滴定过程中水的电离程度逐渐增大 |
B.常温下, 电离平衡常数 电离平衡常数 为 为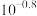 |
C.a点溶液中,存在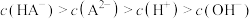 |
D.在NaHA溶液中,存在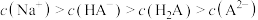 |
您最近一年使用:0次
名校
解题方法
6 . 常温下,下列关于电解质溶液的说法正确的是
| A.pH=12的氨水和氢氧化钠溶液按体积比1∶9混合后,pH值增大 |
B.等体积、等浓度的Na2CO3和NaHCO3溶液混合后,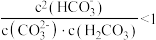 |
C.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后存在: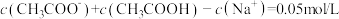 |
D.等浓度的氨水和硫酸按体积比3∶1混合后溶液显碱性,则混合溶液中存在: |
您最近一年使用:0次
2024-05-06更新
|
166次组卷
|
2卷引用:四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷
名校
7 . 亚砷酸(H3AsO3)可用于治疗白血病,亚砷酸在溶液中存在多种微粒形态,向1L0.1mol/LH3AsO3溶液中逐滴加入0.1mol/LKOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示,下列说法错误的是
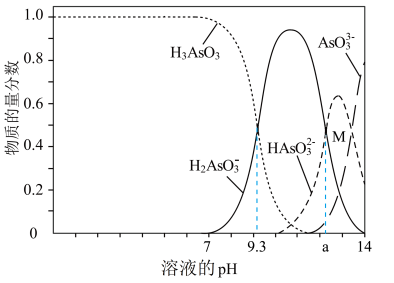
| A.人体血液的pH约为7.35-7.45,服用药物后血液中所含砷元素的主要微粒是H3AsO3 |
| B.该温度下,H3AsO3的电离平衡常数Ka的数量级为10-10 |
C. 时,溶液中: 时,溶液中: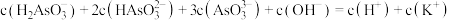 |
D.M点对应的溶液中: |
您最近一年使用:0次
名校
8 . 常温下,向某浓度的H2A溶液中滴加NaOH溶液,若定义pc=-lgc,则测得pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法错误的是

| A.pH=3时溶液中pc(A2-)<pc(H2A)<pc(HA-) |
| B.常温下,H2A的Ka1=10-0.80,Ka2=10-5.30 |
| C.NaHA溶液中c(H+)>c(OH-) |
D.从a点到c点,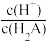 先减小后增大 先减小后增大 |
您最近一年使用:0次
解题方法
9 . 全球大气 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①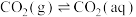

②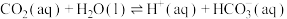

过程①的混合平衡常数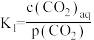 ,其中
,其中 表示溶液中的
表示溶液中的 浓度,
浓度,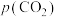 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
_______ (填“增大”或“减小”);当大气压强为akPa,溶液中的 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为_______ 。
(2)由 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应 。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。_______ ,有催化剂时决速步骤的活化能为_______ eV。
(3) 催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为
催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为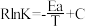 (其中Ea为活化能,K为速率常数,R和C为常数)。
(其中Ea为活化能,K为速率常数,R和C为常数)。
①该反应的活化能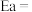
_______ kJ/mol;
②当使用更高效的催化剂时,在图中画出Rlnk与 关系的示意图
关系的示意图_______ 。 催化加氢制甲醇过程中也存在竞争反应
催化加氢制甲醇过程中也存在竞争反应
 ,在恒温密闭容器中,维持压强和投料比不变,将
,在恒温密闭容器中,维持压强和投料比不变,将 和
和 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲醇选择性
转化率和甲醇选择性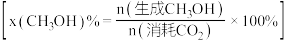 随温度变化关系如下图所示:
随温度变化关系如下图所示:_______ 。
②在压强为P的恒温恒压密闭容器中,加入 和
和 反应并达到平衡状态
反应并达到平衡状态 平衡转化率为20%,甲醇的选择性为50%,计算
平衡转化率为20%,甲醇的选择性为50%,计算 ,在该温度下的平衡常数
,在该温度下的平衡常数
_______ (列出计算式)。
 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:(1)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
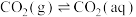

②
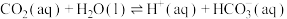

过程①的混合平衡常数
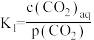 ,其中
,其中 表示溶液中的
表示溶液中的 浓度,
浓度,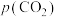 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为(2)由
 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应 。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
。在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。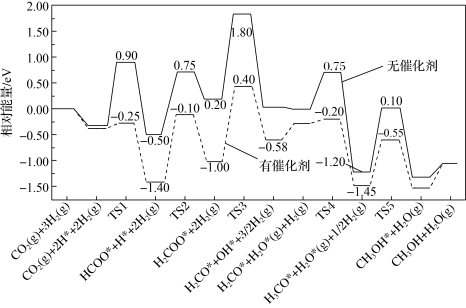
(3)
 催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为
催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知Arthenius经验公式为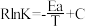 (其中Ea为活化能,K为速率常数,R和C为常数)。
(其中Ea为活化能,K为速率常数,R和C为常数)。①该反应的活化能
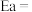
②当使用更高效的催化剂时,在图中画出Rlnk与
 关系的示意图
关系的示意图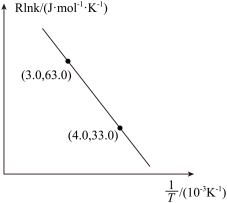
 催化加氢制甲醇过程中也存在竞争反应
催化加氢制甲醇过程中也存在竞争反应
 ,在恒温密闭容器中,维持压强和投料比不变,将
,在恒温密闭容器中,维持压强和投料比不变,将 和
和 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲醇选择性
转化率和甲醇选择性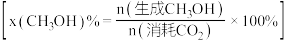 随温度变化关系如下图所示:
随温度变化关系如下图所示: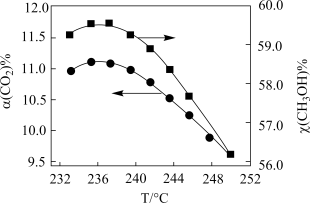
②在压强为P的恒温恒压密闭容器中,加入
 和
和 反应并达到平衡状态
反应并达到平衡状态 平衡转化率为20%,甲醇的选择性为50%,计算
平衡转化率为20%,甲醇的选择性为50%,计算 ,在该温度下的平衡常数
,在该温度下的平衡常数
您最近一年使用:0次
名校
10 . 某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法错误 的是

A.该酸 |
B.某 的缓冲溶液, 的缓冲溶液, |
C.当该溶液的 时, 时, |
D.NaA的水解平衡常数 |
您最近一年使用:0次
2024-05-04更新
|
89次组卷
|
2卷引用:陕西省西安市第八十三中学2023-2024学年高二下学期第一次月考化学试题



