名校
1 . 氢硫酸是 的水溶液,某小组做如下三组实验:
的水溶液,某小组做如下三组实验:
实验Ⅰ:向20mL0.1mol/L的 溶液中滴加20mL0.1mol/L的NaCl溶液,产生白色沉淀。
溶液中滴加20mL0.1mol/L的NaCl溶液,产生白色沉淀。
实验Ⅱ:向实验Ⅰ溶液中继续滴加0.1mol/L的HCN溶液至沉淀完全溶解。
实验Ⅲ:向实验Ⅱ溶液中继续滴加0.1mol/L的氢硫酸溶液,产生黑色沉淀。
[溶液混合后体积变化忽略不计。已知:常温下, 的电离常数
的电离常数 ,
, ,HCN的电离常数
,HCN的电离常数 ;
; ],下列说法不正确的是
],下列说法不正确的是
 的水溶液,某小组做如下三组实验:
的水溶液,某小组做如下三组实验:实验Ⅰ:向20mL0.1mol/L的
 溶液中滴加20mL0.1mol/L的NaCl溶液,产生白色沉淀。
溶液中滴加20mL0.1mol/L的NaCl溶液,产生白色沉淀。实验Ⅱ:向实验Ⅰ溶液中继续滴加0.1mol/L的HCN溶液至沉淀完全溶解。
实验Ⅲ:向实验Ⅱ溶液中继续滴加0.1mol/L的氢硫酸溶液,产生黑色沉淀。
[溶液混合后体积变化忽略不计。已知:常温下,
 的电离常数
的电离常数 ,
, ,HCN的电离常数
,HCN的电离常数 ;
; ],下列说法不正确的是
],下列说法不正确的是A.常温下,0.1mol/L的氢硫酸中存在 |
B.结合实验与数据分析,实验Ⅱ中发生反应 |
C.常温下,0.1mol/L的氢硫酸中 的电离度约为1% 的电离度约为1% |
D.由实验可知与 结合能力 结合能力 |
您最近一年使用:0次
解题方法
2 . 室温下某二元弱酸 的各含
的各含 微粒分布系数如图所示。向
微粒分布系数如图所示。向 溶液中滴加
溶液中滴加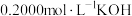 溶液。一般认为二元弱酸
溶液。一般认为二元弱酸 能被分步准确滴定的条件是
能被分步准确滴定的条件是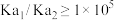 。下列说法错误的是
。下列说法错误的是
 的各含
的各含 微粒分布系数如图所示。向
微粒分布系数如图所示。向 溶液中滴加
溶液中滴加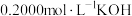 溶液。一般认为二元弱酸
溶液。一般认为二元弱酸 能被分步准确滴定的条件是
能被分步准确滴定的条件是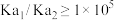 。下列说法错误的是
。下列说法错误的是
A.滴定开始时溶液 约为1.1 约为1.1 |
B.滴入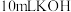 溶液时,混合体系中 溶液时,混合体系中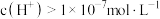 |
C.滴定理论终点时,溶液中存在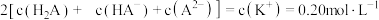 |
D.借助指示剂甲基橙和酚酞,用 标准溶液可测定 标准溶液可测定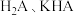 混合液中的KHA含量 混合液中的KHA含量 |
您最近一年使用:0次
3 . 实验发现,25℃下强酸弱碱盐MA的悬浊液中 与
与 呈现线性关系,如下图中所示:
呈现线性关系,如下图中所示:

MOH易溶于水,下列叙述错误的是
 与
与 呈现线性关系,如下图中所示:
呈现线性关系,如下图中所示:
MOH易溶于水,下列叙述错误的是
| A.MA在pH=9的溶液中的溶解度小于在pH=10的溶液中的溶解度 |
B.MA的溶度积 |
C.MOH的电离常数 |
D.溶液pH=7时, |
您最近一年使用:0次
4 . 向 的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
 的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
A.醋酸的电离平衡常数: |
| B.b点溶液呈中性 |
C.水的电离程度: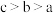 |
D.c点溶液中: |
您最近一年使用:0次
5 . 常温下,向浓度均为 的两种钾盐
的两种钾盐 溶液中加水,溶液的
溶液中加水,溶液的 与稀释倍数
与稀释倍数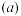 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 的两种钾盐
的两种钾盐 溶液中加水,溶液的
溶液中加水,溶液的 与稀释倍数
与稀释倍数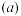 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是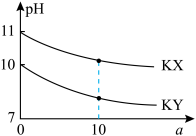
A.常温下, 的水解常数 的水解常数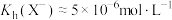 |
B.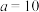 时, 时, 溶液中 溶液中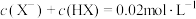 |
C.HY溶液可以与 溶液反应 溶液反应 |
D.浓度均为 的 的 和 和 溶液中离子总浓度: 溶液中离子总浓度: |
您最近一年使用:0次
名校
6 . 25℃时,向含有1 mol甘氨酸盐酸盐(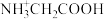 )的溶液中加入NaOH固体,溶液pH及体系中
)的溶液中加入NaOH固体,溶液pH及体系中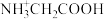 ,
, ,
,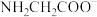 三种粒子的分布系数变化如图所示。
三种粒子的分布系数变化如图所示。 中
中 的分布系数:
的分布系数: ]
]
下列说法正确的是
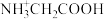 )的溶液中加入NaOH固体,溶液pH及体系中
)的溶液中加入NaOH固体,溶液pH及体系中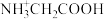 ,
, ,
,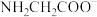 三种粒子的分布系数变化如图所示。
三种粒子的分布系数变化如图所示。
 中
中 的分布系数:
的分布系数: ]
]下列说法正确的是
A.a代表 |
| B.m点:pH小于2.35 |
C.n点溶液中 |
D.曲线上任意点溶液均存在: |
您最近一年使用:0次
7 . 已知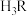 是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数(
是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数( )与溶液pH的关系如图所示,下列说法中错误的是
)与溶液pH的关系如图所示,下列说法中错误的是
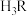 是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数(
是二元弱酸,常温下向其溶液中加入NaOH调节溶液的pH,测得溶液中含R微粒的物质的量分数( )与溶液pH的关系如图所示,下列说法中错误的是
)与溶液pH的关系如图所示,下列说法中错误的是
A.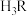 溶液中, 溶液中, |
B.常温下, 的数量级为 的数量级为 |
C.b点溶液中, |
D.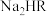 溶液中, 溶液中, |
您最近一年使用:0次
8 . 25℃时, 的电离常数分别为
的电离常数分别为 、
、 。
。 溶液中
溶液中 、
、 、
、 、
、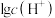 和
和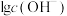 随pH变化的关系如下图所示(已知
随pH变化的关系如下图所示(已知 )。下列说法错误的是
)。下列说法错误的是
 的电离常数分别为
的电离常数分别为 、
、 。
。 溶液中
溶液中 、
、 、
、 、
、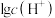 和
和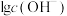 随pH变化的关系如下图所示(已知
随pH变化的关系如下图所示(已知 )。下列说法错误的是
)。下列说法错误的是
| A.NaHB溶液显弱酸性 | B. |
C.M点时, 的值约为-2.3 的值约为-2.3 | D.P点时, |
您最近一年使用:0次
2024-05-14更新
|
51次组卷
|
2卷引用:2024届河南省平许济洛四市高三下学期第四次质量检测理科综合试题-高中化学
9 . 已知:HA为一元弱酸;
 、
、
 。常温下,向
。常温下,向 和
和 的混合溶液中滴加NaA溶液,溶液中
的混合溶液中滴加NaA溶液,溶液中 [
[ 、
、 或
或 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是

 、
、
 。常温下,向
。常温下,向 和
和 的混合溶液中滴加NaA溶液,溶液中
的混合溶液中滴加NaA溶液,溶液中 [
[ 、
、 或
或 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是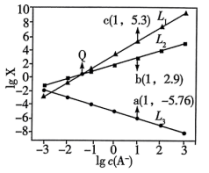
A. 代表 代表 与 与 的关系 的关系 |
B.常温下, |
C. 的K为 的K为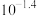 |
D.Q点溶液中 |
您最近一年使用:0次
10 . 若用 表示溶液的酸度,其表达式为
表示溶液的酸度,其表达式为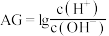 。常温下,实验室用
。常温下,实验室用 溶液滴定
溶液滴定 某二元酸
某二元酸 溶液,滴定曲线如图所示。下列说法错误的是
溶液,滴定曲线如图所示。下列说法错误的是
 表示溶液的酸度,其表达式为
表示溶液的酸度,其表达式为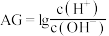 。常温下,实验室用
。常温下,实验室用 溶液滴定
溶液滴定 某二元酸
某二元酸 溶液,滴定曲线如图所示。下列说法错误的是
溶液,滴定曲线如图所示。下列说法错误的是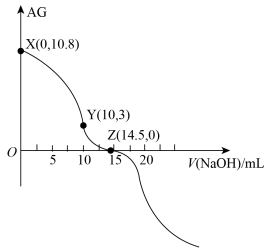
A.常温下,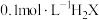 溶液的 溶液的 |
B.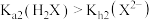 |
C. 点溶液中存在: 点溶液中存在: |
D. 的过程中,水的电离程度逐步增大 的过程中,水的电离程度逐步增大 |
您最近一年使用:0次



