23-24高二上·广东深圳·期末
名校
解题方法
1 . 下列颜色变化,与勒夏特列原理无关的是
| A.红棕色的NO2体系加压后,颜色先变深后逐渐变浅 |
| B.将0.01mol/LFeCl3溶液加热,溶液的颜色加深 |
| C.H2、I2、HI平衡混合气加压后颜色变深 |
| D.新制的氯水在光照下颜色变浅 |
您最近半年使用:0次
2 . 下列溶液中各离子的物质的量浓度关系正确的是
A. 溶液中:滴加几滴稀盐酸, 溶液中:滴加几滴稀盐酸, 增大 增大 |
B.饱和小苏打溶液中: |
C. 与 与 混合溶液呈酸性: 混合溶液呈酸性: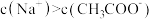 |
D. 时, 时, 的纯碱溶液: 的纯碱溶液: |
您最近半年使用:0次
名校
3 . 无水氯化铁,在空气中极易潮解,加热易升华,常应用于金属蚀刻和污水处理。某化学兴趣小组设计如下实验制备无水氯化铁,并进行其性质探究。回答下列问题:
I.无水氯化铁的制备
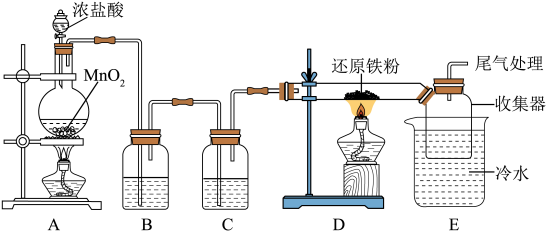
(1)盛装浓盐酸的仪器名称是_______ ,装置B中盛装的药品是_______ ,装置C的作用是_______ 。
(2)装置D中发生反应的化学方程式为_______ 。
(3)装置D、E之间用大口径玻璃管连接的原因是_______ 。
Ⅱ.氯化铁性质探究
(4)取收集器中固体配制成 溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和
溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和_______ 配制溶液时,应先将氯化铁固体溶于较浓的盐酸中,盐酸的作用是_______ 。
(5)向甲、乙两支试管中分别加入 溶液,向甲试管中滴加
溶液,向甲试管中滴加 溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加
溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加
溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加 溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加
溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。
溶液,溶液颜色加深,放置一小时后溶液变为绿色。
①甲试管中产生沉淀的化学式为_______ ,利用平衡移动原理解释产生该沉淀的原因:_______ 。
②甲、乙两支试管中最终溶液都变为绿色,发生反应的离子方程式为_______ 。
I.无水氯化铁的制备

(1)盛装浓盐酸的仪器名称是
(2)装置D中发生反应的化学方程式为
(3)装置D、E之间用大口径玻璃管连接的原因是
Ⅱ.氯化铁性质探究
(4)取收集器中固体配制成
 溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和
溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和(5)向甲、乙两支试管中分别加入
 溶液,向甲试管中滴加
溶液,向甲试管中滴加 溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加
溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加
溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加 溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加
溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。
溶液,溶液颜色加深,放置一小时后溶液变为绿色。①甲试管中产生沉淀的化学式为
②甲、乙两支试管中最终溶液都变为绿色,发生反应的离子方程式为
您最近半年使用:0次
2024-03-02更新
|
105次组卷
|
2卷引用:湖北省恩施州高中教育联盟2023-2024学年高二上学期期末考试化学试题
名校
4 . 下列实验操作、现象、结论均正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 取室温下少量 溶液,加热至60℃,并测定溶液的 溶液,加热至60℃,并测定溶液的 |  增大 增大 |  的水解是吸热反应 的水解是吸热反应 |
| B | 用 试纸测84消毒液的 试纸测84消毒液的 |  |  水解使溶液显碱性 水解使溶液显碱性 |
| C | 向 溶液中滴入稀 溶液中滴入稀 | 溶液橙色变浅 |  (橙色)转化为 (橙色)转化为 (黄色) (黄色) |
| D | 测某浓度 溶液和某浓度 溶液和某浓度 溶液的 溶液的 |  溶液 溶液 大 大 |  电离出 电离出 的能力比 的能力比 的强 的强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 石油天然气开采和炼制过程中会产生大量含硫废水(其中S元素主要化合价是-2价),对设备、环境等造成严重危害。已知:H2S有剧毒;常温下溶解度为1:2.6(体积)。
(1)如图为常温下H2S、HS—、S2—在水溶液中的物质的量分数随pH变化的分布曲线,回答下列问题:

①当pH≈8时,含硫废水中最主要的含硫微粒为___________ 。
②NaHS溶液呈___________ (填“酸性”、“碱性”或“中性”),NaHS水解的离子方程式为:___________ 。
③由图判断,NaHS在常温下发生水解的平衡常数Kh=___________ 。
(2)沉淀法处理含硫废水:向pH≈8的含硫废水中加入适量Cu2+的溶液,产生黑色沉淀且溶液的pH降低,用化学平衡移动的原理解释溶液pH降低的原因:___________ 。
(3)氧化还原法处理含硫废水:向pH≈8的含硫废水中加入一定浓度的Na2SO3溶液,加适量酸,溶液产生淡黄色沉淀。不同pH时,硫化物去除率随时间的变化曲线如图所示,试分析本工艺选择控制体系的pH≈6,而不是去除率更高的pH=3的主要原因:___________ 。

(4)已知:Ksp(AgI)=8.5×10-17、Ksp(AgCl)=1.8×10-10,向浓度均为0.1mol•L-1的NaCl和NaI的混合液中逐渐加入AgNO3粉末,当溶液中I—浓度下降到___________ mol•L-1时(保留一位小数),AgCl开始沉淀。
(1)如图为常温下H2S、HS—、S2—在水溶液中的物质的量分数随pH变化的分布曲线,回答下列问题:

①当pH≈8时,含硫废水中最主要的含硫微粒为
②NaHS溶液呈
③由图判断,NaHS在常温下发生水解的平衡常数Kh=
(2)沉淀法处理含硫废水:向pH≈8的含硫废水中加入适量Cu2+的溶液,产生黑色沉淀且溶液的pH降低,用化学平衡移动的原理解释溶液pH降低的原因:
(3)氧化还原法处理含硫废水:向pH≈8的含硫废水中加入一定浓度的Na2SO3溶液,加适量酸,溶液产生淡黄色沉淀。不同pH时,硫化物去除率随时间的变化曲线如图所示,试分析本工艺选择控制体系的pH≈6,而不是去除率更高的pH=3的主要原因:

(4)已知:Ksp(AgI)=8.5×10-17、Ksp(AgCl)=1.8×10-10,向浓度均为0.1mol•L-1的NaCl和NaI的混合液中逐渐加入AgNO3粉末,当溶液中I—浓度下降到
您最近半年使用:0次
名校
解题方法
6 . 下列操作能达到相应实验目的的是
| 实验操作 | 实验目的 | |
| A | 向等体积、等pH的两种酸溶液HA和HB中分别加入足量锌粉,充分反应后,HA溶液产生更多的氢气 | 说明Ka(HA)>Ka(HB) |
| B | 向5mL0.1mol/LCuSO4溶液中先加入2mL0.4mol/LNaOH溶液,再加入1mL0.1mol/LNa2S溶液 | 探究常温下Ksp[Cu(OH)2]>Ksp(CuS) |
| C | 向滴有酚酞的碳酸钠溶液中加入适量BaCl2固体,溶液颜色变浅 | 说明碳酸钠溶液中存在水解平衡 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-02-27更新
|
374次组卷
|
2卷引用:辽宁省五校联考2023-2024学年高二上学期期末考试化学试题
解题方法
7 . 实验测得 溶液、
溶液、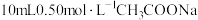 溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时
溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时 和
和 电离常数均为
电离常数均为 ,下列说法正确的是
,下列说法正确的是
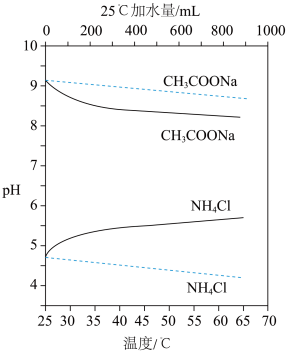
 溶液、
溶液、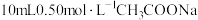 溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时
溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时 和
和 电离常数均为
电离常数均为 ,下列说法正确的是
,下列说法正确的是
| A.图中 |
B.将 溶液加水稀释至浓度 溶液加水稀释至浓度 ,溶液pH变化值小于 ,溶液pH变化值小于 |
C.随温度升高, 增大, 增大, 溶液中 溶液中 减小, 减小, 增大,pH减小 增大,pH减小 |
D.25℃时稀释相同倍数的 溶液与 溶液与 溶液中: 溶液中: |
您最近半年使用:0次
名校
解题方法
8 . “吃饺子要蘸醋”是很多中国人传统的饮食习惯,我们对醋酸的使用有着悠久的历史。
(1) 的醋酸和盐酸各
的醋酸和盐酸各 分别稀释至
分别稀释至 ,所得醋酸的
,所得醋酸的
_______ (填“>”“<”或“=”)所得盐酸的 。
。
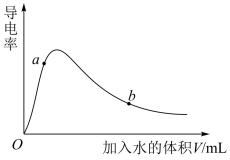
(2)取 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
①由水电离出的氢离子 :a
:a_______ b(填“>”“<”或“=”)。
②使图中b点对应的溶液中 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是_______ (填标号)。
A.加入 B.加入
B.加入 固体 C.加入浓硫酸 D.加入
固体 C.加入浓硫酸 D.加入 固体
固体
(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知 时,三种弱酸的电离平衡常数如下表,写出过量醋酸与
时,三种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ;判断 结合质子能力由大到小顺序为
结合质子能力由大到小顺序为_______ 。
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石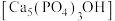 ,市面上含氟牙膏常添加了
,市面上含氟牙膏常添加了 来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:
来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:_______ [已知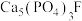 难溶于酸]。
难溶于酸]。
(5)常温下,某同学取 物质的量浓度为
物质的量浓度为 的醋酸,向其中滴入
的醋酸,向其中滴入
 溶液,当滴入的
溶液,当滴入的 溶液的体积为
溶液的体积为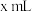 ,溶液呈中性,则醋酸的电离平衡常数
,溶液呈中性,则醋酸的电离平衡常数
_______ (用含x的代数式表示)。

(1)
 的醋酸和盐酸各
的醋酸和盐酸各 分别稀释至
分别稀释至 ,所得醋酸的
,所得醋酸的
 。
。(2)取
 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。①由水电离出的氢离子
 :a
:a②使图中b点对应的溶液中
 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是A.加入
 B.加入
B.加入 固体 C.加入浓硫酸 D.加入
固体 C.加入浓硫酸 D.加入 固体
固体(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知
 时,三种弱酸的电离平衡常数如下表,写出过量醋酸与
时,三种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
溶液反应的离子方程式: 结合质子能力由大到小顺序为
结合质子能力由大到小顺序为| 弱酸 |  |  |  |
| 电离平衡常数 | 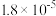 | 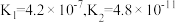 | 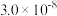 |
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石
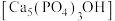 ,市面上含氟牙膏常添加了
,市面上含氟牙膏常添加了 来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:
来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因: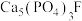 难溶于酸]。
难溶于酸]。(5)常温下,某同学取
 物质的量浓度为
物质的量浓度为 的醋酸,向其中滴入
的醋酸,向其中滴入
 溶液,当滴入的
溶液,当滴入的 溶液的体积为
溶液的体积为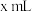 ,溶液呈中性,则醋酸的电离平衡常数
,溶液呈中性,则醋酸的电离平衡常数
您最近半年使用:0次
2024-02-26更新
|
115次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期期末考试化学试题
解题方法
9 . 化学实验是研究物质及其转化的基本方法,是科学探究的一种重要途径。
Ⅰ.为探究不同钠盐对 水解平衡的影响,化学小组设计如下实验。
水解平衡的影响,化学小组设计如下实验。
实验1:常温下,取10.00mL
 溶液置于烧杯中,加入0.01mol的
溶液置于烧杯中,加入0.01mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图1所示。
与时间的关系如图1所示。
实验2:常温下,取10.00mL
 溶液置于烧杯中,加入0.02mol的
溶液置于烧杯中,加入0.02mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图2所示。
与时间的关系如图2所示。

已知:①常温下, 的电离常数为
的电离常数为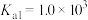 ,
,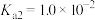 。
。
②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易水解的阳离子的活性会增强或减弱。
(1) 溶液呈酸性的原因是
溶液呈酸性的原因是______ (用离子方程式表示)。
(2)实验1中20s后溶液的 变化的主要原因为
变化的主要原因为______ 。
(3)实验2中10s后溶液的 变化的主要原因为
变化的主要原因为______ 。
实验结论:不同的钠盐对 溶液水解平衡的影响是不同的。
溶液水解平衡的影响是不同的。
(4)实验讨论:根据上述实验预测向10mL0.1mol/L 中加入少量
中加入少量 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液
______ (填“增大”、“不变”或“减小”)。
Ⅱ.探究Na₂SO₃溶液与溶液的反应原理,某兴趣小组进行了如下实验:
(5)配制
 溶液时;先将
溶液时;先将 固体溶于
固体溶于______ ,再稀释至指定浓度。
(6)针对上述现象,甲同学认为 与
与 发生了相互促进的水解反应得到一种胶体,其离子方程式为
发生了相互促进的水解反应得到一种胶体,其离子方程式为______ ;乙同学认为 与
与 还发生了氧化还原反应,请据此判断两种反应活化能较小的是
还发生了氧化还原反应,请据此判断两种反应活化能较小的是______ (填“水解反应”或“氧化还原反应”)。
提示:经查阅资料和进一步实验探究,证实了 与
与 既发生了水解反应又发生了氧化还原反应。
既发生了水解反应又发生了氧化还原反应。
Ⅰ.为探究不同钠盐对
 水解平衡的影响,化学小组设计如下实验。
水解平衡的影响,化学小组设计如下实验。实验1:常温下,取10.00mL

 溶液置于烧杯中,加入0.01mol的
溶液置于烧杯中,加入0.01mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图1所示。
与时间的关系如图1所示。实验2:常温下,取10.00mL

 溶液置于烧杯中,加入0.02mol的
溶液置于烧杯中,加入0.02mol的 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液 与时间的关系如图2所示。
与时间的关系如图2所示。
已知:①常温下,
 的电离常数为
的电离常数为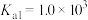 ,
,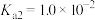 。
。②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易水解的阳离子的活性会增强或减弱。
(1)
 溶液呈酸性的原因是
溶液呈酸性的原因是(2)实验1中20s后溶液的
 变化的主要原因为
变化的主要原因为(3)实验2中10s后溶液的
 变化的主要原因为
变化的主要原因为实验结论:不同的钠盐对
 溶液水解平衡的影响是不同的。
溶液水解平衡的影响是不同的。(4)实验讨论:根据上述实验预测向10mL0.1mol/L
 中加入少量
中加入少量 固体,利用
固体,利用 传感器测得溶液
传感器测得溶液
Ⅱ.探究Na₂SO₃溶液与溶液的反应原理,某兴趣小组进行了如下实验:
装置 | 现象 |
| 现象ⅰ:一开始液体颜色加深,由棕黄色变为红褐色。 现象ⅱ:一段时间后液体颜色变浅,变为浅黄色。 |
(5)配制

 溶液时;先将
溶液时;先将 固体溶于
固体溶于(6)针对上述现象,甲同学认为
 与
与 发生了相互促进的水解反应得到一种胶体,其离子方程式为
发生了相互促进的水解反应得到一种胶体,其离子方程式为 与
与 还发生了氧化还原反应,请据此判断两种反应活化能较小的是
还发生了氧化还原反应,请据此判断两种反应活化能较小的是提示:经查阅资料和进一步实验探究,证实了
 与
与 既发生了水解反应又发生了氧化还原反应。
既发生了水解反应又发生了氧化还原反应。
您最近半年使用:0次
名校
解题方法
10 . 请根据所学知识,回答以下问题。
(1)甲烷是最简单的烷烃,下列关于甲烷的叙述中不正确的是___________。
(2)有机物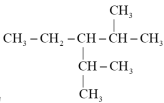 的系统命名是:
的系统命名是:___________ 。
(3)支链只有一个乙基且相对分子质量最小的烷烃的结构简式为___________ 。
(4)向 的
的 溶液中通入
溶液中通入 气体,
气体, 时,
时,
___________ 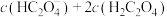 (填“>”,“<”或者“=”)。
(填“>”,“<”或者“=”)。
(5)已知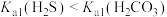 ,等浓度的①
,等浓度的① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ 中
中 由小到大的顺序为
由小到大的顺序为___________ (请填写序号)。
(6) 的
的 溶液与
溶液与 的
的 溶液中
溶液中
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(7)向 稀溶液中分别加入少量下列物质或改变条件,能使
稀溶液中分别加入少量下列物质或改变条件,能使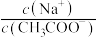 比值增大的是
比值增大的是___________ (请填写序号)。
①固体 ②固体
②固体 ③冰醋酸 ④降温
③冰醋酸 ④降温
(1)甲烷是最简单的烷烃,下列关于甲烷的叙述中不正确的是___________。
| A.甲烷是一种无色、无味、难溶于水的气体 |
B.甲烷分子具有正四面体结构,其中4个C—H键长度和强度相同,键角是 |
| C.二氯甲烷只有一种,证明甲烷是立体结构,而不是平面结构 |
D.甲烷与氯气的取代反应,反应的 的物质的量等于生成的 的物质的量等于生成的 的物质的量的两倍 的物质的量的两倍 |
 的系统命名是:
的系统命名是:(3)支链只有一个乙基且相对分子质量最小的烷烃的结构简式为
(4)向
 的
的 溶液中通入
溶液中通入 气体,
气体, 时,
时,
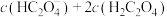 (填“>”,“<”或者“=”)。
(填“>”,“<”或者“=”)。(5)已知
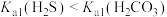 ,等浓度的①
,等浓度的① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ 中
中 由小到大的顺序为
由小到大的顺序为(6)
 的
的 溶液与
溶液与 的
的 溶液中
溶液中
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(7)向
 稀溶液中分别加入少量下列物质或改变条件,能使
稀溶液中分别加入少量下列物质或改变条件,能使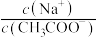 比值增大的是
比值增大的是①固体
 ②固体
②固体 ③冰醋酸 ④降温
③冰醋酸 ④降温
您最近半年使用:0次