解题方法
1 . 铁、铝在生产生活中有广泛的应用。完成下列填空:
(1)铝用作电线是利用了铝的_______ 性;铁用作炊具是利用了铁的_______ 性。
(2)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是_______ 物质。氢氧化铝和盐酸反应的离子方程式为_______ 。
(4)氯元素原子结构示意图为_______ ,其与钠元素组成的化合物的电子式为_______ 。
(5)钠、铝、铁三种金属元素中,_______ (填名称)是地壳中含量最高的金属元素,其在周期表中位于第_______ 周期_______ 族。
(6)以下不是铝和铁的共同性质的是_______ 。
a.导电性 b.导热性 c.延展性 d.两性
(7)列举一个可以说明氯和硫的非金属性强弱的事实用化学方程式表示_______ 。
(1)铝用作电线是利用了铝的
(2)常温下由于浓硫酸能使铁
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是
(4)氯元素原子结构示意图为
(5)钠、铝、铁三种金属元素中,
(6)以下不是铝和铁的共同性质的是
a.导电性 b.导热性 c.延展性 d.两性
(7)列举一个可以说明氯和硫的非金属性强弱的事实用化学方程式表示
您最近一年使用:0次
名校
解题方法
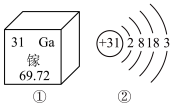
2 . 2019年是元素周期表年,镓是门捷列夫曾经预言的金属(类铝)。下图①是镓元素在元素周期表中的部分信息,②是镓原子的结构示意图。请回答:
A.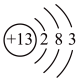 B.
B. 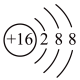 C.
C.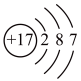 D.
D.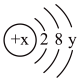
(1)镓原子的核电荷数为_______ ,镓元素的相对原子质量为_______ 。自然界中的镓共有两种稳定的同位素,其中69Ga的丰度为64.0%,则另一种镓的同位素质量数为_______ 。
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是_______ (填元素符号);微粒B的电子式为_______ ,则镓离子与B形成的化合物为_______ (填化学式)。
(3)D为某微粒的结构示意图,已知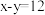 ,则x=
,则x=_______ ;写出C和D组成的化合物在水溶液中的电离方程式:_______ 。
(4)氮化镓(GaN)是第三代半导体材料,一般采用 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为_______ 。

A.
 B.
B.  C.
C. D.
D.
(1)镓原子的核电荷数为
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是
(3)D为某微粒的结构示意图,已知
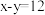 ,则x=
,则x=(4)氮化镓(GaN)是第三代半导体材料,一般采用
 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
您最近一年使用:0次
解题方法
3 . 下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是___________ ;
(2)N、O、F三种元素中,非金属性最强的是___________ (填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为___________ ;
(4)碘与氯是同主族元素。下面关于碘的推断错误的是___________ (选填字母);
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(1)钠元素在元素周期表中的位置是
(2)N、O、F三种元素中,非金属性最强的是
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为
(4)碘与氯是同主族元素。下面关于碘的推断错误的是
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
4 . 我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为: S+2KNO3+3C=K2S+3CO2↑+N2↑。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,
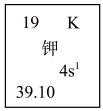
数据“39.10”表示的是___________ ;钾元素在周期表中的位置为___________ 。
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是___________ 。
(3)上述反应生成物中,属于非电解质的是___________ (写结构式);生成物中含有离子键的物质电子式是___________ 。
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为___________ ,它们的非金属性由强到弱的顺序为___________ ;列举一条能证明S和O非金属性强弱的实验事实___________ 。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,

数据“39.10”表示的是
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为
您最近一年使用:0次
名校
5 . 以下元素及物质与人类的生产生活紧密相关。完成下列填空:
(1)氯元素的原子结构示意图_______ ;氯与钠元素组成的化合物的电子式_______ 。
(2)钠、铝、铁三种元素中,_______ 元素是地壳中含量最高的金属元素,其在元素周期表中位于第_______ 周期_______ 族。
(3)以下不是铝、铁的共性的是_______
(4)浓硫酸具有强氧化性,它能与铜反应的化学方程式为_______ 。
(5)列举一个可以说明氯和硫非金属性强弱的事实_______ 。
(1)氯元素的原子结构示意图
(2)钠、铝、铁三种元素中,
(3)以下不是铝、铁的共性的是_______
| A.导电性 | B.导热性 | C.延展性 | D.能与碱溶液反应 |
(5)列举一个可以说明氯和硫非金属性强弱的事实
您最近一年使用:0次
6 . 1869年,门捷列夫总结出了元素周期表,还基于此预言了三种当时未被发现的元素,门捷列夫分别称它们为“类硼”、“类铝”与“类硅”。这三种元素在之后的几十年中陆续被发现,从而让人们意识到元素周期表具有重大价值。
(1)基态硼原子的最外层电子数为___________ 。“类硼”是与硼同族的第四周期元素,则“类硼”可能有的性质是___________ (填写下列字母)。
a.最高化合价为 b.该元素单质具有金属光泽
b.该元素单质具有金属光泽
c.该元素单质可与沸水反应置换出 d.该元素最高价氧化物对应水化物是强碱
d.该元素最高价氧化物对应水化物是强碱
(2)“类硼”最高价氯化物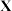 的熔点为
的熔点为 ,则
,则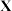 的化学式为
的化学式为___________ ,且该物质属于___________ 晶体。
(3)“类硅”与硅同族,且其基态原子中电子占据了4个能级组,则该元素处于第___________ 周期,其基态原子最外层有___________ 个未成对电子。“类硅”的原子半径___________ (填“>”、“<”或“=”)“类硼”的原子半径,“类硅”的电负性___________ (填“>”、“<”或“=”)“类硼”的电负性。
(4)“类铝”原子与铝原子具有相同的价电子数,与“类硼”是同一周期的两种不同元素。则“类铝”位于元素周期表___________ 区中,其基态原子的价电子的电子排布式为___________ 。
(1)基态硼原子的最外层电子数为
a.最高化合价为
 b.该元素单质具有金属光泽
b.该元素单质具有金属光泽c.该元素单质可与沸水反应置换出
 d.该元素最高价氧化物对应水化物是强碱
d.该元素最高价氧化物对应水化物是强碱(2)“类硼”最高价氯化物
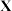 的熔点为
的熔点为 ,则
,则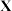 的化学式为
的化学式为(3)“类硅”与硅同族,且其基态原子中电子占据了4个能级组,则该元素处于第
(4)“类铝”原子与铝原子具有相同的价电子数,与“类硼”是同一周期的两种不同元素。则“类铝”位于元素周期表
您最近一年使用:0次
2022-06-29更新
|
246次组卷
|
3卷引用:上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题
上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题(已下线)专题03 晶体结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)福建省漳州市第三中学2022-2023学年高二下学期3月质量检测化学试题
名校
7 . 如图是元素周期表的一部分。回答下列问题:

溴被称为海洋元素。
(1)溴在元素周期表中位于第___________ 周期___________ 族。
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
(3)能够证明溴的非金属性强于碘的方法是___________ (写出一种即可)。

溴被称为海洋元素。
(1)溴在元素周期表中位于第
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
(3)能够证明溴的非金属性强于碘的方法是
您最近一年使用:0次
名校
8 . 下表是周期表中的一部分,根据①—⑧在周期表中的位置,用元素符号或化学式回答问题
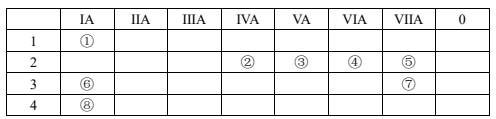
(1)画出表中元素中,非金属性最强的元素的离子结构示意图_______ ;
(2)这些元素的最高价氧化物对应水化物中酸性最强的是______ ,碱性最强的是______ ;
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程_______ ;
(4)表中⑤⑦两种元素氢化物的稳定性更强的是_______ ;
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是_______ ,简述判断理由_______ ;
(6)用一个化学方程式证明②③两种元素非金属性的强弱_______ 。

(1)画出表中元素中,非金属性最强的元素的离子结构示意图
(2)这些元素的最高价氧化物对应水化物中酸性最强的是
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程
(4)表中⑤⑦两种元素氢化物的稳定性更强的是
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是
(6)用一个化学方程式证明②③两种元素非金属性的强弱
您最近一年使用:0次
名校
9 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。如图是元素周期表的一部分,回答下列问题。
(1)周期表呈现的短周期元素中,次外层电子数等于其他电子层电子数之和的元素是_______ (写原子结构示意图);上述周期表呈现的元素中,金属性最强的元素在周期表中处于第_______ 周期第_______ 族 ,非金属性最强的元素是:_______ (写电子式)。
(2)Sn的最高正价为_______ ,写 出Cl的最高价氧化物对应水化物的化学式_______ 。
(3)比较微粒半径大小: Al_______ F; Al3+_______ F-。(选填“>”或“<”)
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是_______ 。
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②硅元素存在多种同位素。已知三种天然稳定同位素的数据如下:
请列出硅元素的近似相对原子质量的计算式_______ 。
③原子数相同,电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息如见表。
硼元素与Y、Q形成互为等电子体负离子: BY 、BQ
、BQ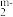 , 则m值为
, 则m值为_______ 。
| B | C | N | O | F |
| Al | Si | P | S | Cl |
| Ga | Ge | As | Se | Br |
| In | Sn | Sb | Te | I |
(2)Sn的最高正价为
(3)比较微粒半径大小: Al
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②硅元素存在多种同位素。已知三种天然稳定同位素的数据如下:
| 核素符号 | 28Si | 29Si | 30Si |
| 相对原子质量 | 27.977 | 28.976 | 29.974 |
| 丰度 | 92.2% | 4.7% | 3.1% |
③原子数相同,电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息如见表。
| Q | 与H可形成QH3的10电子结构分子 |
| Y | 带两个负电荷的负离子与氖原子结构相同 |
 、BQ
、BQ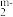 , 则m值为
, 则m值为
您最近一年使用:0次
10 . 已知某主族元素的原子结构示意图如下,请写出它们在周期表中的位置。
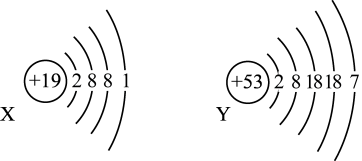
X:_______ ,Y:_______ 。

X:
您最近一年使用:0次
2022-04-28更新
|
561次组卷
|
2卷引用:上海市青浦区第一中学2021-2022学年高一下学期期中线上质量检测化学试题



