名校
1 . 如图是元素周期表的一部分。回答下列问题:

溴被称为海洋元素。
(1)溴在元素周期表中位于第___________ 周期___________ 族。
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
(3)能够证明溴的非金属性强于碘的方法是___________ (写出一种即可)。

溴被称为海洋元素。
(1)溴在元素周期表中位于第
(2)表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
(3)能够证明溴的非金属性强于碘的方法是
您最近一年使用:0次
名校
2 . 下表是周期表中的一部分,根据①—⑧在周期表中的位置,用元素符号或化学式回答问题
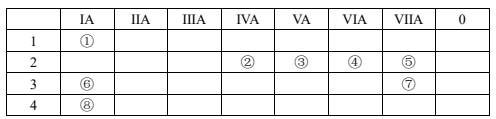
(1)画出表中元素中,非金属性最强的元素的离子结构示意图_______ ;
(2)这些元素的最高价氧化物对应水化物中酸性最强的是______ ,碱性最强的是______ ;
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程_______ ;
(4)表中⑤⑦两种元素氢化物的稳定性更强的是_______ ;
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是_______ ,简述判断理由_______ ;
(6)用一个化学方程式证明②③两种元素非金属性的强弱_______ 。

(1)画出表中元素中,非金属性最强的元素的离子结构示意图
(2)这些元素的最高价氧化物对应水化物中酸性最强的是
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程
(4)表中⑤⑦两种元素氢化物的稳定性更强的是
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是
(6)用一个化学方程式证明②③两种元素非金属性的强弱
您最近一年使用:0次
名校
3 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。如图是元素周期表的一部分,回答下列问题。
(1)周期表呈现的短周期元素中,次外层电子数等于其他电子层电子数之和的元素是_______ (写原子结构示意图);上述周期表呈现的元素中,金属性最强的元素在周期表中处于第_______ 周期第_______ 族 ,非金属性最强的元素是:_______ (写电子式)。
(2)Sn的最高正价为_______ ,写 出Cl的最高价氧化物对应水化物的化学式_______ 。
(3)比较微粒半径大小: Al_______ F; Al3+_______ F-。(选填“>”或“<”)
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是_______ 。
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②硅元素存在多种同位素。已知三种天然稳定同位素的数据如下:
请列出硅元素的近似相对原子质量的计算式_______ 。
③原子数相同,电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息如见表。
硼元素与Y、Q形成互为等电子体负离子: BY 、BQ
、BQ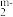 , 则m值为
, 则m值为_______ 。
| B | C | N | O | F |
| Al | Si | P | S | Cl |
| Ga | Ge | As | Se | Br |
| In | Sn | Sb | Te | I |
(2)Sn的最高正价为
(3)比较微粒半径大小: Al
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②硅元素存在多种同位素。已知三种天然稳定同位素的数据如下:
| 核素符号 | 28Si | 29Si | 30Si |
| 相对原子质量 | 27.977 | 28.976 | 29.974 |
| 丰度 | 92.2% | 4.7% | 3.1% |
③原子数相同,电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息如见表。
| Q | 与H可形成QH3的10电子结构分子 |
| Y | 带两个负电荷的负离子与氖原子结构相同 |
 、BQ
、BQ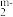 , 则m值为
, 则m值为
您最近一年使用:0次
4 . 铅的合金可作轴承、电缆外皮之用,还可做体育器材铅球等。
(1)铅元素位于元素周期表第六周期IVA族,该族中原子序数最小的元素的原子有_______ 种 能量不同的电子,其次外层的电子云有_______ 种不同的伸展方向。
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是_______ (填化学式),气态氢化物沸点最低的是_______ (填电子式)。
(3)配平下列化学方程式,把系数以及相关物质填写在空格上,并标出电子转移的方向和数目______ 。
_______PbO2+_______MnSO4+______HNO3→_______HMnO4+______Pb(NO3)2+_______PbSO4↓+_______
(4)把上述反应后的溶液稀释到1L,测出其中的Pb2+的浓度为0.6mol·L-1,则反应中转移的电子数为_______ 个,该反应中被氧化的元素是_______ 。 若将该反应设计成一原电池,则_______ 极 (填电极名称)附近溶液出现紫红色。
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______。
(6)已知如下热化学方程式:
Ca(s)+Cl2(g)→CaCl2(s)+ 795kJ
Sr(s)+Cl2(g)→SrCl2(s) + 828kJ
Ba(s)+ Cl2(g) → BaCl2(s) + 860kJ
则①CaCl2、②SrCl2、③BaCl2三种氯化物的稳定性由大到小的排列为_______ (填序号)。从能量的角度解释理由是_______ 。
(1)铅元素位于元素周期表第六周期IVA族,该族中原子序数最小的元素的原子有
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是
(3)配平下列化学方程式,把系数以及相关物质填写在空格上,并标出电子转移的方向和数目
_______PbO2+_______MnSO4+______HNO3→_______HMnO4+______Pb(NO3)2+_______PbSO4↓+_______
(4)把上述反应后的溶液稀释到1L,测出其中的Pb2+的浓度为0.6mol·L-1,则反应中转移的电子数为
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______。
| A.PbO2+4HCl →PbCl4+2H2O | B.PbO2+4HCl →PbCl2+ Cl2↑+2H2O |
| C.PbO2+2HCl+2H+→PbCl2+2H2O | D.PbO2+4HCl→PbCl2+2OH- |
Ca(s)+Cl2(g)→CaCl2(s)+ 795kJ
Sr(s)+Cl2(g)→SrCl2(s) + 828kJ
Ba(s)+ Cl2(g) → BaCl2(s) + 860kJ
则①CaCl2、②SrCl2、③BaCl2三种氯化物的稳定性由大到小的排列为
您最近一年使用:0次
5 . 已知某主族元素的原子结构示意图如下,请写出它们在周期表中的位置。
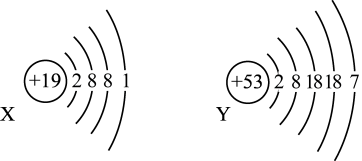
X:_______ ,Y:_______ 。

X:
您最近一年使用:0次
2022-04-28更新
|
558次组卷
|
2卷引用:上海市青浦区第一中学2021-2022学年高一下学期期中线上质量检测化学试题
解题方法
6 . Ⅰ.周期表可以帮我们认识一些未知元素的性质。锡(Sn)是很早便被发现和使用的金属,其原子结构示意图见下图。
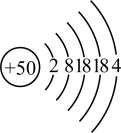
(1)锡为主族元素,在元素周期表中的位置是_______ 。 其最高正价为_______ 。
(2)SnO2能与NaOH反应生成钠盐,写出反应的化学方程式_______ 。
Ⅱ.硒与硫在元素周期表中相对位置如图所示。
(3)硒元素最高价氧化物对应水化物的化学式为_______ , 写出SeO2和H2Se反应的化学方程式_______ 。
(4)比较气态氢化物H2S、H2Se 的热稳定性_______ ,从原子结构及周期律角度分析气态氢化物稳定性强弱的原因:_______ 。

(1)锡为主族元素,在元素周期表中的位置是
(2)SnO2能与NaOH反应生成钠盐,写出反应的化学方程式
Ⅱ.硒与硫在元素周期表中相对位置如图所示。
| S |
| Se |
(4)比较气态氢化物H2S、H2Se 的热稳定性
您最近一年使用:0次
名校
7 . 《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)Be在周期表中的位置:___________ , 10Be和9Be___________ (填序号)。
a. 是同一种原子 b. 具有相同的中子数 c. 具有几乎相同的化学性质 d. 互为同位素
(2)写出Al(OH)3与NaOH溶液反应的化学方程式:___________ 。
(3)研究表明28Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是___________(填序号)。
(1)Be在周期表中的位置:
a. 是同一种原子 b. 具有相同的中子数 c. 具有几乎相同的化学性质 d. 互为同位素
(2)写出Al(OH)3与NaOH溶液反应的化学方程式:
(3)研究表明28Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是___________(填序号)。
| A.比较Mg(OH)2与Al(OH)3的碱性强弱 |
| B.比较这两种元素的最高正化合价 |
| C.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液 |
| D.比较这两种金属的硬度和熔点 |
您最近一年使用:0次
8 . 全球“青年化学家元素周期表”中多种元素由我国科学家代言,如氮、硫、钪(Sc)等。完成下列填空。
(1)钪(Sc)的原子结构示意图为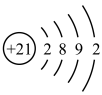 ,钪原子核外最外层电子排布式为
,钪原子核外最外层电子排布式为___________ ;Sc与第II主族相邻,Sc位于元素周期表的第___________ 族;钪的最高价态可能是___________ 。
(2)下列比较正确的是___________(选填选项)。
(3)工业上以N2为原料,以 、
、 为产品,实现了“向空气要氮肥”的目标。
为产品,实现了“向空气要氮肥”的目标。
①在如下价、类二维图中用“→”和途径中间产物的化学式,画出了由N2转化为 路径。
路径。
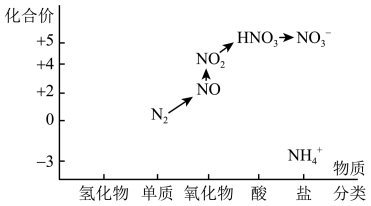
②工业上常以氨为原料制硝酸。写出氨催化氧化的化学方程式。___________
(4)硫酸铵[(NH4)2SO4],也称肥田粉,是我国生产和施用最早的氮肥之一、写出硫酸铵使用时的注意事项及对环境的影响(各一条),并说明理由。
①___________ 。
②___________ 。
(1)钪(Sc)的原子结构示意图为
 ,钪原子核外最外层电子排布式为
,钪原子核外最外层电子排布式为(2)下列比较正确的是___________(选填选项)。
A.原子半径: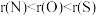 | B.热稳定性: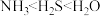 |
C.溶解性: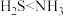 | D.微粒种类:氢硫酸<氨水 |
 、
、 为产品,实现了“向空气要氮肥”的目标。
为产品,实现了“向空气要氮肥”的目标。①在如下价、类二维图中用“→”和途径中间产物的化学式,画出了由N2转化为
 路径。
路径。
②工业上常以氨为原料制硝酸。写出氨催化氧化的化学方程式。
(4)硫酸铵[(NH4)2SO4],也称肥田粉,是我国生产和施用最早的氮肥之一、写出硫酸铵使用时的注意事项及对环境的影响(各一条),并说明理由。
①
②
您最近一年使用:0次
名校
9 . 黑火药爆炸时发生化学反应:S+2KNO3 +3C→ K2S +3CO2↑ +N2↑
(1)上述反应涉及的元素中,属于第二周期的元素有_______ 。
(2)上述反应的生成物中,属于非电解质的是_______ ,其电子式是_______ 。
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式:_______ 。
(1)上述反应涉及的元素中,属于第二周期的元素有
(2)上述反应的生成物中,属于非电解质的是
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式:
您最近一年使用:0次
名校
10 . 下表为元素周期表的一部分,①~⑧分别代表8种不同的元素。
用化学用语 回答下列问题:
(1)②在元素周期表中的位置是___________ 。
(2)③、④、⑤、⑥的离子半径由大到小的顺序是___________ 。
(3)①~⑧的最高价氧化物对应水化物,酸性最强的是___________ 。
(4)①、④、⑤可组成既含离子键,又含共价键的化合物,其电子式为___________ 。
(5)含元素①的某种复盐晶体可以用作净水剂。其化学式是___________ ,用离子方程式表示它能净水的原因___________ 。
| ① | |||||||||
| ② | ③ | ④ | |||||||
| ⑤ | ⑥ | ⑦ | ⑧ |
用
(1)②在元素周期表中的位置是
(2)③、④、⑤、⑥的离子半径由大到小的顺序是
(3)①~⑧的最高价氧化物对应水化物,酸性最强的是
(4)①、④、⑤可组成既含离子键,又含共价键的化合物,其电子式为
(5)含元素①的某种复盐晶体可以用作净水剂。其化学式是
您最近一年使用:0次
2021-11-08更新
|
125次组卷
|
2卷引用:上海市向明中学2021-2022学年高二上学期期中考试化学试题



