1 . 19世纪初,许多新的元素被相继发现,化学家开始关注这些元素在化学性质和物理性质上的相似性和递变性。1869年,俄国化学家门捷列夫编制了一份元素周期表,是化学发展史上的一个里程碑。
(1)请写出下列元素在周期表中的位置:
Na_______ ; O_______ ;He_______ 。
(2)某元素位于第二周期第17族,它是_______ 元素(元素名称);与P相邻的同族元素的原子序数是_______ 、_______ 。
(1)请写出下列元素在周期表中的位置:
Na
(2)某元素位于第二周期第17族,它是
您最近一年使用:0次
2 . 19世纪初,许多新的元素被相继发现,化学家开始关注这些元素在化学性质和物理性质上的相似性和递变性。1869年,俄国化学家门捷列夫编制了一份元素周期表,是化学发展史上的一个里程碑。
(1)下列关于元素周期表的认识,错误的是
(2)某一周期第IIA族元素的原子序数为x,则同周期的第IIIA族元素的原子序数不可能是
(3)有人认为位于元素周期表第IA族的氢元素,也可以放在第VIIA族,下列物质能支持这种观点的是
(1)下列关于元素周期表的认识,错误的是
| A.元素周期表有7个周期 | B.前4周期叫短周期 |
| C.元素周期表有18个族 | D.第15族也叫第VA族 |
| A.x+1 | B.x+8 | C.x+11 | D.x+25 |
| A.HF | B.H3O+ | C.NaH | D.H2O2 |
您最近一年使用:0次
解题方法
3 . 含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有NO等氮氧化物的尾气,反应方程式如下:NaClO + NO + H2O —— NaCl + HNO3 (未配平)。完成下列填空。
(1)氯在元素周期表中的位置是______________________________ ,其所在主族的元素中,最高价氧化物对应的水化物酸性最强的是_______________ (填化学式)。
(2)配平上述反应方程式_______ 。
每有0.3mol电子发生转移,可消耗标准状况下NO气体的体积约为____________ L。
(3)NaClO溶液中存在如下关系:c(OH-)_____ c(HClO)(填“>”、“=”、或“<”)。
其他条件相同,随着NaClO溶液初始pH(用稀硫酸调节)的不同,NO转化率如图。
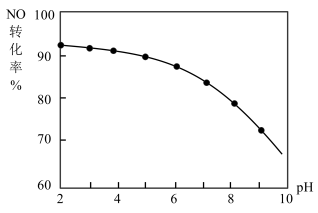
(4)NaClO溶液的初始pH越大,NO的转化率越________________ (填“高”或“低”),其原因是_____________________ 。取少量NaClO溶液和KClO3溶液,分别置于A试管和B试管,滴加试剂,观察现象,记录于下表。
(5)取少量NaClO溶液和KClO3溶液,分别置于A试管和B试管,滴加试剂,观察现象,记录于下表。
请将表格填写完整。
(1)氯在元素周期表中的位置是
(2)配平上述反应方程式
每有0.3mol电子发生转移,可消耗标准状况下NO气体的体积约为
(3)NaClO溶液中存在如下关系:c(OH-)
其他条件相同,随着NaClO溶液初始pH(用稀硫酸调节)的不同,NO转化率如图。

(4)NaClO溶液的初始pH越大,NO的转化率越
(5)取少量NaClO溶液和KClO3溶液,分别置于A试管和B试管,滴加试剂,观察现象,记录于下表。
请将表格填写完整。
滴加KI溶液 | 再滴加CCl4,振荡、静置 | 结论 | |
A试管 | 溶液变为棕黄色 | 溶液分层,下层显 | 氧化性强弱:(填“>”或“<”) KClO3 |
B试管 | 无现象 | 溶液分层,均无色 |
您最近一年使用:0次
4 . 铁、铝在生产生活中有广泛的应用。回答下列问题:
(1)铝的原子结构示意图为_______ 。它位于元素周期表的第_______ 周期,第_______ 族。
(2)Na、Al最高价氧化物的水化物之间反应的化学方程式是_______ 。
(3)实验室制备氢氧化铝的常用方法是在氯化铝溶液中滴加氨水,反应的离子方程式为_______ 。
(4)检验某溶液中是否含有 Fe3+的操作方法是_______ 。
(1)铝的原子结构示意图为
(2)Na、Al最高价氧化物的水化物之间反应的化学方程式是
(3)实验室制备氢氧化铝的常用方法是在氯化铝溶液中滴加氨水,反应的离子方程式为
(4)检验某溶液中是否含有 Fe3+的操作方法是
您最近一年使用:0次
解题方法
5 . 铁、铝在生产生活中有广泛的应用。完成下列填空:
(1)铝用作电线是利用了铝的_______ 性;铁用作炊具是利用了铁的_______ 性。
(2)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是_______ 物质。氢氧化铝和盐酸反应的离子方程式为_______ 。
(4)氯元素原子结构示意图为_______ ,其与钠元素组成的化合物的电子式为_______ 。
(5)钠、铝、铁三种金属元素中,_______ (填名称)是地壳中含量最高的金属元素,其在周期表中位于第_______ 周期_______ 族。
(6)以下不是铝和铁的共同性质的是_______ 。
a.导电性 b.导热性 c.延展性 d.两性
(7)列举一个可以说明氯和硫的非金属性强弱的事实用化学方程式表示_______ 。
(1)铝用作电线是利用了铝的
(2)常温下由于浓硫酸能使铁
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是
(4)氯元素原子结构示意图为
(5)钠、铝、铁三种金属元素中,
(6)以下不是铝和铁的共同性质的是
a.导电性 b.导热性 c.延展性 d.两性
(7)列举一个可以说明氯和硫的非金属性强弱的事实用化学方程式表示
您最近一年使用:0次
名校
解题方法
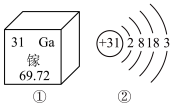
6 . 2019年是元素周期表年,镓是门捷列夫曾经预言的金属(类铝)。下图①是镓元素在元素周期表中的部分信息,②是镓原子的结构示意图。请回答:
A.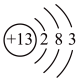 B.
B. 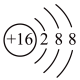 C.
C.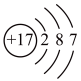 D.
D.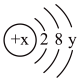
(1)镓原子的核电荷数为_______ ,镓元素的相对原子质量为_______ 。自然界中的镓共有两种稳定的同位素,其中69Ga的丰度为64.0%,则另一种镓的同位素质量数为_______ 。
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是_______ (填元素符号);微粒B的电子式为_______ ,则镓离子与B形成的化合物为_______ (填化学式)。
(3)D为某微粒的结构示意图,已知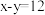 ,则x=
,则x=_______ ;写出C和D组成的化合物在水溶液中的电离方程式:_______ 。
(4)氮化镓(GaN)是第三代半导体材料,一般采用 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为_______ 。

A.
 B.
B.  C.
C. D.
D.
(1)镓原子的核电荷数为
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是
(3)D为某微粒的结构示意图,已知
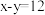 ,则x=
,则x=(4)氮化镓(GaN)是第三代半导体材料,一般采用
 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
您最近一年使用:0次
解题方法
7 . 下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是___________ ;
(2)N、O、F三种元素中,非金属性最强的是___________ (填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为___________ ;
(4)碘与氯是同主族元素。下面关于碘的推断错误的是___________ (选填字母);
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(1)钠元素在元素周期表中的位置是
(2)N、O、F三种元素中,非金属性最强的是
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为
(4)碘与氯是同主族元素。下面关于碘的推断错误的是
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为: S+2KNO3+3C=K2S+3CO2↑+N2↑。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,
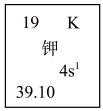
数据“39.10”表示的是___________ ;钾元素在周期表中的位置为___________ 。
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是___________ 。
(3)上述反应生成物中,属于非电解质的是___________ (写结构式);生成物中含有离子键的物质电子式是___________ 。
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为___________ ,它们的非金属性由强到弱的顺序为___________ ;列举一条能证明S和O非金属性强弱的实验事实___________ 。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,

数据“39.10”表示的是
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为
您最近一年使用:0次
名校
9 . 以下元素及物质与人类的生产生活紧密相关。完成下列填空:
(1)氯元素的原子结构示意图_______ ;氯与钠元素组成的化合物的电子式_______ 。
(2)钠、铝、铁三种元素中,_______ 元素是地壳中含量最高的金属元素,其在元素周期表中位于第_______ 周期_______ 族。
(3)以下不是铝、铁的共性的是_______
(4)浓硫酸具有强氧化性,它能与铜反应的化学方程式为_______ 。
(5)列举一个可以说明氯和硫非金属性强弱的事实_______ 。
(1)氯元素的原子结构示意图
(2)钠、铝、铁三种元素中,
(3)以下不是铝、铁的共性的是_______
| A.导电性 | B.导热性 | C.延展性 | D.能与碱溶液反应 |
(5)列举一个可以说明氯和硫非金属性强弱的事实
您最近一年使用:0次
10 . 1869年,门捷列夫总结出了元素周期表,还基于此预言了三种当时未被发现的元素,门捷列夫分别称它们为“类硼”、“类铝”与“类硅”。这三种元素在之后的几十年中陆续被发现,从而让人们意识到元素周期表具有重大价值。
(1)基态硼原子的最外层电子数为___________ 。“类硼”是与硼同族的第四周期元素,则“类硼”可能有的性质是___________ (填写下列字母)。
a.最高化合价为 b.该元素单质具有金属光泽
b.该元素单质具有金属光泽
c.该元素单质可与沸水反应置换出 d.该元素最高价氧化物对应水化物是强碱
d.该元素最高价氧化物对应水化物是强碱
(2)“类硼”最高价氯化物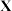 的熔点为
的熔点为 ,则
,则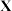 的化学式为
的化学式为___________ ,且该物质属于___________ 晶体。
(3)“类硅”与硅同族,且其基态原子中电子占据了4个能级组,则该元素处于第___________ 周期,其基态原子最外层有___________ 个未成对电子。“类硅”的原子半径___________ (填“>”、“<”或“=”)“类硼”的原子半径,“类硅”的电负性___________ (填“>”、“<”或“=”)“类硼”的电负性。
(4)“类铝”原子与铝原子具有相同的价电子数,与“类硼”是同一周期的两种不同元素。则“类铝”位于元素周期表___________ 区中,其基态原子的价电子的电子排布式为___________ 。
(1)基态硼原子的最外层电子数为
a.最高化合价为
 b.该元素单质具有金属光泽
b.该元素单质具有金属光泽c.该元素单质可与沸水反应置换出
 d.该元素最高价氧化物对应水化物是强碱
d.该元素最高价氧化物对应水化物是强碱(2)“类硼”最高价氯化物
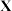 的熔点为
的熔点为 ,则
,则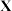 的化学式为
的化学式为(3)“类硅”与硅同族,且其基态原子中电子占据了4个能级组,则该元素处于第
(4)“类铝”原子与铝原子具有相同的价电子数,与“类硼”是同一周期的两种不同元素。则“类铝”位于元素周期表
您最近一年使用:0次
2022-06-29更新
|
237次组卷
|
3卷引用:上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题
上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题(已下线)专题03 晶体结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)福建省漳州市第三中学2022-2023学年高二下学期3月质量检测化学试题



