解题方法
1 . 过渡元素在材料和化工生产中占有重要地位。
(1) 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(
中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(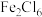 ),写出氯化铁双聚分子的结构式
),写出氯化铁双聚分子的结构式___________ 。
(2)元素Mn和Fe的部分电离能如下表所示,发现Mn元素的第三电离能( )要大于Fe元素的第三电离能,原因是
)要大于Fe元素的第三电离能,原因是___________ 。
(3)Mn的一种配合物化学式为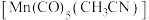 ,下列说法正确的是___________。
,下列说法正确的是___________。
(4)某晶体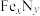 的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,
的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,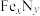 转化为两种Cu替代型产物的能量变化如图2所示。
转化为两种Cu替代型产物的能量变化如图2所示。___________ 。
②下列关于晶体的说法正确的是___________ 。
A.晶体的形成与晶体的自范性有关
B.测定某一固体是否属于晶体可以用X-射线衍射仪进行实验
C.晶体和非晶体的根本区别在于固体是否有规则的几何外形
D.由玻璃制成规则的玻璃球体现了晶体的自范性
E.晶胞是晶体结构中最小的重复单元
(1)
 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(
中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(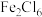 ),写出氯化铁双聚分子的结构式
),写出氯化铁双聚分子的结构式(2)元素Mn和Fe的部分电离能如下表所示,发现Mn元素的第三电离能(
 )要大于Fe元素的第三电离能,原因是
)要大于Fe元素的第三电离能,原因是| 元素 | Mn | Fe | |
| 电离能 (  ) ) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
(3)Mn的一种配合物化学式为
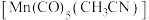 ,下列说法正确的是___________。
,下列说法正确的是___________。A. 与Mn原子配位时,提供孤电子对的是C原子 与Mn原子配位时,提供孤电子对的是C原子 |
| B.电负性:H<C<N<O |
C. 中两个C原子的杂化类型均为 中两个C原子的杂化类型均为 |
D. 中σ键与π键数目之比为5:2 中σ键与π键数目之比为5:2 |
(4)某晶体
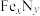 的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,
的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,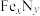 转化为两种Cu替代型产物的能量变化如图2所示。
转化为两种Cu替代型产物的能量变化如图2所示。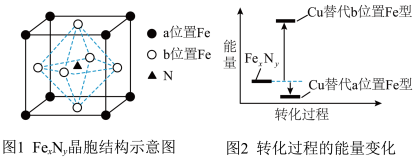
②下列关于晶体的说法正确的是
A.晶体的形成与晶体的自范性有关
B.测定某一固体是否属于晶体可以用X-射线衍射仪进行实验
C.晶体和非晶体的根本区别在于固体是否有规则的几何外形
D.由玻璃制成规则的玻璃球体现了晶体的自范性
E.晶胞是晶体结构中最小的重复单元
您最近一年使用:0次
2024·浙江·模拟预测
解题方法
2 . 根据物质的组成和结构可推测其性质,下列推测不合理 的是
| 物质 | 性质描述 | 推测 | |
| A | 三甲基铝Al(CH3)3 | 暴露空气中瞬间着火,与水反应剧烈 | 水反应可得到CH4和Al(OH)3 |
| B | 三氟化氯 ClF3 | 极强助燃剂,能发生自耦电离: 2ClF3  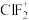 + + | BrF3比ClF3更易发生自耦电离 |
| C | 亚铁氰化钾K4[Fe(CN)6] | 食盐的抗结剂,3K4[Fe(CN)6] 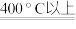 12KCN+Fe3C+5C+3N2↑ 12KCN+Fe3C+5C+3N2↑ | 在空气中灼烧,生成K2CO3、FeO、CO2和N2 |
| D | 魔酸SbF5∙HSO3F | 五氟化锑和氟磺酸的混合物,是一种酸性比普通无机酸强106~1010倍的超强酸 | SbF5∙HF是超强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 已知A、B、C、D、E是中学化学常见的几种元素,原子序数依次增大。
其结构或性质信息如下表所示:
(1)A元素位于___________ 区,A、B、C三种元素原子第一电离能由大到小顺序为:___________ (用元素符号填空);
(2)B、C、D三种元素原子电负性由大到小顺序为:___________ (用元素符号填空); 分子的空间构型:
分子的空间构型:___________ ;
(3)化合物EC、ED其化学键的离子键百分数较大的化合物为:___________ 。(用化学式填空)
其结构或性质信息如下表所示:
| 元素 | 结构或者信息 |
| A | 基态A原子p能级上有两个未成对电子 |
| B | 基态B原子中有7个运动状态不同的电子 |
| C | C元素是地壳中含量最高的元素 |
| D | 基态D的价层电子排布是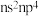 |
| E | 基态E原子次外层全充满,最外层电子数为1 |
(2)B、C、D三种元素原子电负性由大到小顺序为:
 分子的空间构型:
分子的空间构型:(3)化合物EC、ED其化学键的离子键百分数较大的化合物为:
您最近一年使用:0次
名校
4 . 连花清瘟胶囊的有效成分大黄素的结构如图所示,该成分有很强的抗炎抗菌药理活性,基于结构视角,下列说法正确的是
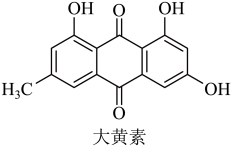
A.该分子中氧原子的杂化类型均为 |
| B.分子中所含元素的电负性O>C>H |
| C.基态碳原子核外电子的空间运动状态有6种 |
| D.该分子为非极性分子 |
您最近一年使用:0次
名校
5 . 下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构与性质 | 解释 |
| A | 键角: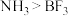 |  中 中 的孤电子对数比 的孤电子对数比 中 中 的孤电子对数多 的孤电子对数多 |
| B | 酸性: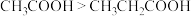 | 烃基(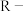 )越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱 )越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱 |
 |  的熔点比干冰高 的熔点比干冰高 |  比 比 相对分子量大,分子间作用力大 相对分子量大,分子间作用力大 |
 | 稳定性: |  分子间存在氢键 分子间存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 硼、碳、氮元素形成的化合物极为丰富。
(1)吡啶( )是一种常见的配体,其中含有与苯类似的大
)是一种常见的配体,其中含有与苯类似的大 键,则吡啶中N原子的价层孤电子对占据的轨道为__________(填标号)。
键,则吡啶中N原子的价层孤电子对占据的轨道为__________(填标号)。
(2) 、
、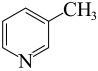 、
、 均可作为配体,则三者中配位能力最弱的是
均可作为配体,则三者中配位能力最弱的是__________ ,其原因为__________ 。
(3)某种新型储氢材料的晶胞如图所示,其中八面体中心为 ,顶点均为配体
,顶点均为配体 ;四面体中心为硼原子,顶点均为氢原子。该晶胞为立方体形,边长为a pm,则
;四面体中心为硼原子,顶点均为氢原子。该晶胞为立方体形,边长为a pm,则__________ ,晶体类型是__________ , 与硼原子间的最短距离为
与硼原子间的最短距离为__________ cm(用含a代数式表示)。
(4)下列有关说法正确的是__________。
(1)吡啶(
 )是一种常见的配体,其中含有与苯类似的大
)是一种常见的配体,其中含有与苯类似的大 键,则吡啶中N原子的价层孤电子对占据的轨道为__________(填标号)。
键,则吡啶中N原子的价层孤电子对占据的轨道为__________(填标号)。A. 轨道 轨道 | B. 轨道 轨道 | C. 杂化轨道 杂化轨道 | D. 杂化轨道 杂化轨道 |
(2)
 、
、 、
、 均可作为配体,则三者中配位能力最弱的是
均可作为配体,则三者中配位能力最弱的是(3)某种新型储氢材料的晶胞如图所示,其中八面体中心为
 ,顶点均为配体
,顶点均为配体 ;四面体中心为硼原子,顶点均为氢原子。该晶胞为立方体形,边长为a pm,则
;四面体中心为硼原子,顶点均为氢原子。该晶胞为立方体形,边长为a pm,则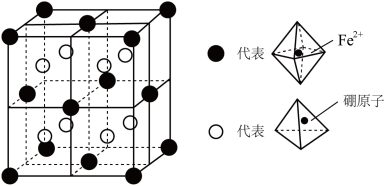
 与硼原子间的最短距离为
与硼原子间的最短距离为(4)下列有关说法正确的是__________。
| A.电负性:N>H>B | B.沸点:吡啶>苯 |
| C.第一电离能:N>C>O | D.基态 的简化电子排布式: 的简化电子排布式: |
您最近一年使用:0次
名校
7 . SiCl4与N-甲基咪唑(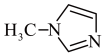 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
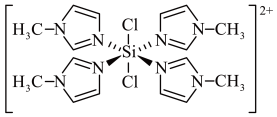
| A.N-甲基咪唑分子中氮原子的杂化轨道类型为sp2和sp3 |
| B.H、C、N的电负性由大到小的顺序为N>C>H |
| C.1个M2+中含有54个σ键(包括配键) |
| D.中心原子硅的氧化数为+6 |
您最近一年使用:0次
名校
8 . 按自由基稳定性由大到小排列的顺序是

| A.cadb | B.cdab | C.acdb | D.acbd |
您最近一年使用:0次
名校
9 . 下面关于四种短周期元素的原子比较正确的是
①基态原子的电子排布式: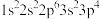 ;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子
;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子
①基态原子的电子排布式:
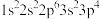 ;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子
;②3p轨道半充满的原子;③原子核外有4种不同能量的电子,且只有一个单电子;④s能级电子总数等于p能级电子总数的p区原子| A.最高正化合价:④=①>②>③ | B.原子半径:③>②>①>④ |
| C.电负性;③>②>①>④ | D.第一电离能:④>①>②>③。 |
您最近一年使用:0次
2024-04-11更新
|
194次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
10 . 优氯净(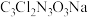 )是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是
)是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是
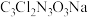 )是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是
)是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是| A.电负性:O>N>C | B.原子半径:Cl>Na>O |
| C.O在周期表中的位置是第2周期ⅣA族 | D.热稳定性: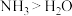 |
您最近一年使用:0次
2024-04-11更新
|
106次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题



