名校
解题方法
1 . 有A、B、C、D、E五种元素,其相关信息如表:
请回答下列问题:
(1)CA3分子的电子式_______ ;在元素E的硫酸盐溶液中逐渐通入CA3,可以观察到的实验现象是_______ ;CA3是_______ 分子(填“极性”或者“非极性”),CA3极易溶于水的原因:①_______ 、②_______ 。
(2)C与A还可形成CA5,CA5是由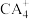 与A-组成的离子化合物,可与水反应产生无色气体,且所得溶液显碱性,则与水反应的化学方程式
与A-组成的离子化合物,可与水反应产生无色气体,且所得溶液显碱性,则与水反应的化学方程式_______ 。
(3)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有_______ (填序号);1 mol该离子中含有_______ 个σ键。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
(4)若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______(填序号)。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | 基态原子的2p轨道中有3个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有2个运动状态不同的电子 |
| E | E的+1价离子的M能层中所有能级各轨道都有电子且没有未成对电子 |
(1)CA3分子的电子式
(2)C与A还可形成CA5,CA5是由
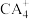 与A-组成的离子化合物,可与水反应产生无色气体,且所得溶液显碱性,则与水反应的化学方程式
与A-组成的离子化合物,可与水反应产生无色气体,且所得溶液显碱性,则与水反应的化学方程式(3)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
(4)若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______(填序号)。
| A.平面正方形 | B.正四面体 | C.三角锥形 | D.V形 |
您最近一年使用:0次
2 . 我国科学家用如图所示大阴离子的盐作水系锌离子电池的电解质溶液,显示了优良的循环性能。X、Y、Z、W均为短周期元素且原子序数依次增大,其中X、Y、Z位于同一周期,Y、W核外最外层电子数相等。下列叙述正确的是
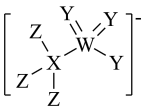
| A.电负性由大到小的顺序是Z>Y>W | B.Y和Z不能形成二元化合物 |
| C.简单氢化物的稳定性:Y>Z>W | D.简单离子半径大小顺序为W>Z>Y |
您最近一年使用:0次
3 . 新型光催化剂 具有较高的催化活性。下列有关其组成元素的说法
具有较高的催化活性。下列有关其组成元素的说法不正确 的是
 具有较高的催化活性。下列有关其组成元素的说法
具有较高的催化活性。下列有关其组成元素的说法A.Ge的价电子排布式为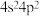 |
| B.Zn为第四周期ⅡB族的元素 |
C.三种元素电负性由大到小的顺序: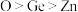 |
| D.基态O原子中成对电子数是未成对电子数的2倍 |
您最近一年使用:0次
解题方法
4 . 砷化镓是优良的半导体材料,其晶胞结构如图所示。下列说法错误的是
已知:设砷和镓的原子半径分别为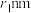 和
和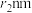 ,砷化镓晶体的密度为
,砷化镓晶体的密度为 ,
, 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。
已知:设砷和镓的原子半径分别为
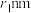 和
和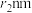 ,砷化镓晶体的密度为
,砷化镓晶体的密度为 ,
, 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。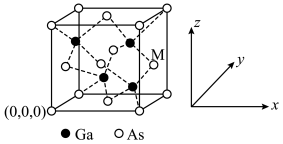
A.M原子的坐标参数为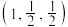 |
B.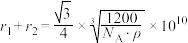 |
C.电负性: |
D.该晶胞的俯视投影图为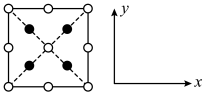 |
您最近一年使用:0次
5 . 下列关于Mg和Al原子结构的分析中正确的是
| A.原子半径 :Al> Mg | B.第一电离能:Al> Mg |
| C.电负性: Al> Mg | D.成对电子数:Al> Mg |
您最近一年使用:0次
解题方法
6 . 氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质,某氨基吡啶衍生物铜配合物X的结构简式如图所示。___________ ;下列不同状态的氮原子中,能量最高的是___________ (填字母)。
A.1s22s22p3 B.1s22s12p4 C.1s22s22p23s1 D.1s22s22p23p1
(2)C、N、O元素原子的电负性由大到小的顺序为___________ 。
(3)X中Cu2+的配位数是___________ ;铜元素有不同价态氧化物,高温下稳定性Cu2O___________ CuO(填“大于”或“小于”),从离子的电子层结构角度分析,主要原因是___________ 。
(4)X中N原子的杂化方式为___________ 。
(5)下列关于X的说法中不正确的是___________ (填字母)。
A.存在氢键、配位键等化学键
B.碳、氧原子间形成的σ键和 键个数比为2:1
键个数比为2:1
C.铜属于d区元素
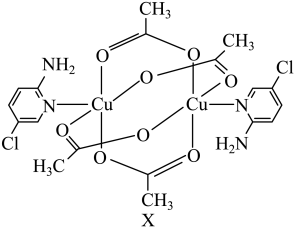
A.1s22s22p3 B.1s22s12p4 C.1s22s22p23s1 D.1s22s22p23p1
(2)C、N、O元素原子的电负性由大到小的顺序为
(3)X中Cu2+的配位数是
(4)X中N原子的杂化方式为
(5)下列关于X的说法中不正确的是
A.存在氢键、配位键等化学键
B.碳、氧原子间形成的σ键和
 键个数比为2:1
键个数比为2:1C.铜属于d区元素
您最近一年使用:0次
名校
7 . 关于化学键和分子间作用力的理论是关于物质结构的基本理论。
(1)N、P、As电负性由大到小的顺序为___________ 。
(2)用“>”或“<”填空:
(3)MgCl2在工业上应用广泛,可由MgO制备。MgO的熔点比BaO的熔点___________ (填“高”或“低”)。
(4)HCHO分子的立体构型为___________ 形。
(5)已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93o52′,而两个O—H键与O—O 键的夹角均为96o52′。___________ 键和___________ 键的___________ (填“极性”或“非极性”)分子。
②H2O2难溶于CS2,简要说明理由:___________ 。
(1)N、P、As电负性由大到小的顺序为
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si | O2- | NaCl | H2SO4 |
(3)MgCl2在工业上应用广泛,可由MgO制备。MgO的熔点比BaO的熔点
(4)HCHO分子的立体构型为
(5)已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93o52′,而两个O—H键与O—O 键的夹角均为96o52′。
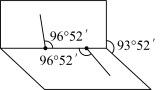
②H2O2难溶于CS2,简要说明理由:
您最近一年使用:0次
解题方法
8 . 下列关于物质性质的解释错误的是
选项 | 性质 | 解释 |
A | 沸点:NH3>PH3 | NH3分子间可以形成氢键 |
B | Ka:三氟乙酸>三氯乙酸 | 电负性:氟元素>氯元素 |
C | 熔点:MgO>NaCl | 晶格能:MgO>NaCl |
D | 稳定性:聚四氟乙烯>聚乙烯 | 相对分子质量:四氟乙烯>乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,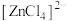 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: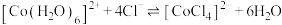
 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,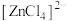 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: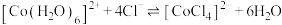
 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
A.由实验①可推知 ,实验②平衡逆向移动 ,实验②平衡逆向移动 |
B.等物质的量的 和 和 中σ键数之比为3:2 中σ键数之比为3:2 |
C.由实验③可知配离子的稳定性: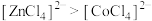 |
D.以上离子涉及的元素的电负性顺序为 |
您最近一年使用:0次
名校
10 . 某锂盐的结构如图所示,其阴离子是由原子序数依次增大的短周期主族元素X、Y、Z、W形成,X、Y与Z同一周期,Y与W同族。下列性质规律按照W、X、Y、Z依次递增是是

| A.第一电离能 | B.元素的电负性 |
| C.简单氢化物的还原性 | D.简单离子半径 |
您最近一年使用:0次



