名校
1 . 新型光催化剂Zn2GeO4具有较高的催化活性。下列有关其组成元素的说法正确的是
| A.Zn处于元素周期表中的d区 |
| B.Ge的价电子排布式为3d104s24p2 |
| C.基态O原子中成对电子数是未成对电子数的2倍 |
| D.三种元素电负性由大到小的顺序是:O>Ge>Zn |
您最近一年使用:0次
2022-12-14更新
|
245次组卷
|
2卷引用:海南省三亚华侨学校(南新校区)2020-2021学年高二下学期3月月考化学试jgh同
解题方法
2 . 铜是应用最广泛的金属之一,其抗氧化防腐技术一直是化学研究的热点课题。
(1)基态铜原子的价电子排布图为_____ ,铜元素位于元素周期表中_____ 区。
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为_____ 。
②HCOO-中碳原子的杂化方式为_____ ,其空间构型为____ 。
③HCOOH能与水任意比互溶的原因为_____ 。
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于_____ 晶体。
(1)基态铜原子的价电子排布图为
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为
②HCOO-中碳原子的杂化方式为
③HCOOH能与水任意比互溶的原因为
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于
您最近一年使用:0次
解题方法
3 . N、O、S、Cl、Cu五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
(1)第一电离能:N_____ O(填“ ”或“
”或“ ”,下同),电负性:S
”,下同),电负性:S____ Cl。
(2) 的沸点比
的沸点比 高的原因是
高的原因是___________ ; 属于
属于________ (填“极性”或“非极性”)分子,
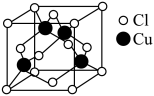
(3)Cu与Cl形成化合物的晶胞如图所示。该晶体的化学式为________ 。
(1)第一电离能:N
 ”或“
”或“ ”,下同),电负性:S
”,下同),电负性:S(2)
 的沸点比
的沸点比 高的原因是
高的原因是 属于
属于(3)Cu与Cl形成化合物的晶胞如图所示。该晶体的化学式为

您最近一年使用:0次
名校
4 . 下列各组元素中,电负性依次减小的是
| A.O、Cl、H | B.K、Na、Al | C.As、P、H | D.O、S、Cl |
您最近一年使用:0次
2020-04-27更新
|
377次组卷
|
11卷引用:海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题
海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题2015-2016学年湖北省长阳一中高二第一学期第一次月考化学试卷2014-2015学年宁夏平罗中学高二上学期期中化学试卷河北省唐山市第十一中学2018-2019学年高二下学期期中考试化学试题辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题新疆喀什地区巴楚县第一中学2020-2021学年高二上学期期中考试化学试题海南省海南鑫源高级中学2020-2021学年高二下学期第一次月考化学试题福建省福州市金山中学2020-2021学年高二下期中考试化学试题第二节 原子结构与元素的性质 第2课时 元素周期律——原子半径、电离能、电负性的递变规律1.3.2元素的电离能、电负性及其变化规律(课中)-鲁科版选择性必修21.2.2 元素周期律-课堂例题
5 . (1)元素C、N、O、K的电负性从大到小依次为______ 。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为______ 。
(3)下图是周期表中短周期的一部分,A的单质是空气中含量最多的物质,其中第一电离能最小的元素是______ (填“A”“B”“C”或“D”)。

(4)氮化硼(BN)是一种重要的功能陶瓷材料。基态B原子的电子排布式为______ ;B和N相比,电负性较大的是______ ,BN中B元素的化合价为______ 。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(3)下图是周期表中短周期的一部分,A的单质是空气中含量最多的物质,其中第一电离能最小的元素是

(4)氮化硼(BN)是一种重要的功能陶瓷材料。基态B原子的电子排布式为
您最近一年使用:0次
2019-07-07更新
|
183次组卷
|
3卷引用:海南省三亚华侨学校(南新校区)2020-2021学年高二下学期3月月考化学试jgh同
名校
6 . 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示.

(1)S2Cl2的结构式为_____ ,其化学键类型有_____ (填“极性键”“非极性键”或“极性键和非极性键”).
(2)电负性:S_____ (填“>”或“<”)Cl,S2Cl2中硫的化合价为_____ .
(3)S2Cl2分子中S原子的杂化轨道类型为_____ ,每个S原子有_____ 对孤电子对.

(1)S2Cl2的结构式为
(2)电负性:S
(3)S2Cl2分子中S原子的杂化轨道类型为
您最近一年使用:0次
2016-12-09更新
|
625次组卷
|
6卷引用:海南省三亚华侨学校(南新校区)2020-2021学年高二下学期期中考试化学试题



