解题方法
1 . 氧和硫是元素周期表中第ⅥA族元素。下列说法正确的是
| A.电负性:O<S | B.沸点: |
C. 是极性分子 是极性分子 | D. 空间构型为平面三角形 空间构型为平面三角形 |
您最近一年使用:0次
2024-04-07更新
|
236次组卷
|
2卷引用:海南省海口市2024届高三上学期摸底考试化学试卷
2 . 按要求回答下列问题:
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为________ ,基态原子核外有________ 种空间运动状态。
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是________________________________ 。
③光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________ 。
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子 的空间构型为
的空间构型为________ ,Na在空气中燃烧则发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为________ 光谱(填“发射”或“吸收”)。
(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:
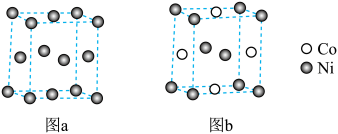
①镍钴合金若写作NixCo1-x,则图b合金中x=________
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为________ g/cm3(列出计算式)。
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
A. | B.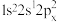 | C. | D.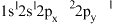 |
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子
 的空间构型为
的空间构型为(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:

①镍钴合金若写作NixCo1-x,则图b合金中x=
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为
您最近一年使用:0次
名校
3 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是


A.该分子的分子式为 |
B.该分子中相邻C原子之间均以 杂化轨道重叠形成σ键 杂化轨道重叠形成σ键 |
| C.组成该分子的所有元素中氟的电负性最大 |
| D.该分子中有2个手性碳原子 |
您最近一年使用:0次
名校
解题方法
4 . 一氯化碘(ICl)、三氯化碘(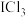 )是卤素互化物,它们的性质与卤素单质相似,如:2ICl+2Zn=ZnI2+ZnCl2,以下判断正确的是
)是卤素互化物,它们的性质与卤素单质相似,如:2ICl+2Zn=ZnI2+ZnCl2,以下判断正确的是
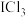 )是卤素互化物,它们的性质与卤素单质相似,如:2ICl+2Zn=ZnI2+ZnCl2,以下判断正确的是
)是卤素互化物,它们的性质与卤素单质相似,如:2ICl+2Zn=ZnI2+ZnCl2,以下判断正确的是A.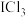 与水反应的产物为HI和HClO 与水反应的产物为HI和HClO |
B.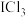 与KI反应时,氯元素被还原 与KI反应时,氯元素被还原 |
| C.ICl与冷NaOH溶液反应的离子方程式为ICl+2OH−=IO−+Cl−+H2O |
| D.ICl与水的反应不属于氧化还原反应 |
您最近一年使用:0次
2023-12-18更新
|
75次组卷
|
2卷引用:海南省海口市琼山华侨中学2023-2024学年高三上学期第二次月考化学试题
5 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。回答下列问题:

(1)j元素基态原子的电子排布式是___________ 。
(2)元素k位于周期表中___________ 区,其基态原子有___________ 个未成对电子,有___________ 种空间运动状态不同的电子。
(3)下列正确的是___________。
(4)基态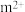 的离子结构示意图为
的离子结构示意图为___________ ,已知高温下化合物 比化合物
比化合物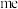 更稳定,试从
更稳定,试从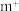 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因___________ 。
(5)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(6)传闻某国合成了第166号元素,若已知原子结构规律不变,该元素应是第___________ 周期、第___________ 族。

(1)j元素基态原子的电子排布式是
(2)元素k位于周期表中
(3)下列正确的是___________。
A.原子半径 | B.第一电离能 |
C.电负性 | D.最高价氧化物的水化物的酸性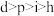 |
(4)基态
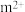 的离子结构示意图为
的离子结构示意图为 比化合物
比化合物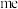 更稳定,试从
更稳定,试从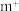 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因(5)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与
 溶液反应的离子方程式
溶液反应的离子方程式(6)传闻某国合成了第166号元素,若已知原子结构规律不变,该元素应是第
您最近一年使用:0次
名校
解题方法
6 . C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式______ ,C、O、Si三种元素的电负性由大到小的顺序为______ 。
(2)干冰是分子晶体,其密度比冰大的原因是____________ 。
(3)氧化物XO的电子总数与SiC的相等,则X为______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是__________________ 。
(4)在30 g 晶体中含
晶体中含______ mol Si-O键。
(1)写出Si的基态原子核外最外层电子排布式
(2)干冰是分子晶体,其密度比冰大的原因是
(3)氧化物XO的电子总数与SiC的相等,则X为
(4)在30 g
 晶体中含
晶体中含
您最近一年使用:0次
名校
解题方法
7 . DDQ是一种常用的有机氧化剂,结构式如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,W半径大于Z。下列说法正确的是
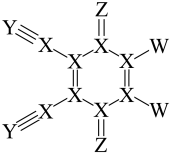
| A.简单离子半径:Z>Y | B.元素的电负性:Z>W |
| C.简单气态氢化物沸点:Y<X | D.含氧酸的酸性:W>X |
您最近一年使用:0次
2023-07-28更新
|
132次组卷
|
3卷引用:海南省海南中学2022-2023学年高二下学期期末考试化学试题
海南省海南中学2022-2023学年高二下学期期末考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)宁夏银川市贺兰县第一中学2023-2024学年高二下学期第一阶段考试化学试卷
名校
解题方法
8 . 铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用。回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如图:
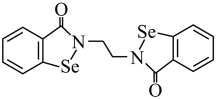
①基态Se原子的核外电子排布式为______ 。
②比较键角大小:气态SeO3分子______ SeO 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是______ 。
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:
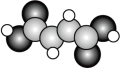
①富马酸分子中σ键与π键的数目比为______ 。
②富马酸亚铁中各元素的电负性由小到大的顺序为______ 。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为NH ,反应过程如图所示:
,反应过程如图所示:
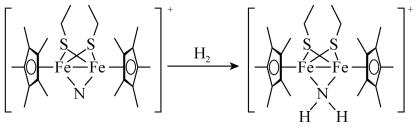
①产物中N原子的杂化轨道类型为______ 。
②与N3-互为等电子体的一种分子为______ (填化学式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如图:

①基态Se原子的核外电子排布式为
②比较键角大小:气态SeO3分子
 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:

①富马酸分子中σ键与π键的数目比为
②富马酸亚铁中各元素的电负性由小到大的顺序为
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为NH
 ,反应过程如图所示:
,反应过程如图所示:
①产物中N原子的杂化轨道类型为
②与N3-互为等电子体的一种分子为
您最近一年使用:0次
名校
解题方法
9 . 前四周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是次外层的2倍,基态Y原子的价层电子排布式为2s22p4,Z是第四周期主族元素中原子半径最大的元素,W与X同主族,下列说法正确 的是
| A.原子半径:Y> X | B.电负性:Y<W |
| C.W的第一电离能大于Z的第一电离能 | D.Y形成的单质可能是极性分子 |
您最近一年使用:0次
10 . 冠醚是由多个二元醇分子之间失水形成的环状醚,X是其中的一种, 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中
因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原子间能形成化学键。下列说法中错误的是
与氧原子间能形成化学键。下列说法中错误的是

 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中
因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原子间能形成化学键。下列说法中错误的是
与氧原子间能形成化学键。下列说法中错误的是
| A.X可形成分子晶体 | B.Y中 与氧原子间形成的是离子键 与氧原子间形成的是离子键 |
| C.K⁺不能与X形成超分子 | D.电负性:O>C>Li |
您最近一年使用:0次
2023-04-22更新
|
250次组卷
|
2卷引用:海南省海口市2023届高三下学期4月学生学科能力诊断化学试题



