1 . 碳酸丙烯酯是一种水溶性颜料的分散剂,工业上常用 作催化剂用1,2-丙二醇和尿素合成,原理如下:
作催化剂用1,2-丙二醇和尿素合成,原理如下:

回答下列问题:
(1)基态Zn原子的价电子排布式为___________ ,其位于元素周期表的___________ (填“d”或“ds”)区。
(2)尿素分子中,各元素电负性大小顺序为___________ ,第三电离能
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)碳酸丙烯酸酯中C原子的杂化方式为___________ ;其常温下呈液态,易溶于水,也易溶于乙醚、苯等有机溶剂,则碳酸丙烯酸酯的晶体类型为___________ 。
(4) 能与
能与 形成稳定的配离子
形成稳定的配离子 ,其中配体的立体结构为
,其中配体的立体结构为___________ ,配离子中 的键角比
的键角比 的键角大,试从物质结构的角度解释其原因
的键角大,试从物质结构的角度解释其原因___________ 。
(5) 有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为
有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为___________ ;该晶体的密度为___________  (写出计算式,阿伏加德罗常数的值为
(写出计算式,阿伏加德罗常数的值为 )。
)。

 作催化剂用1,2-丙二醇和尿素合成,原理如下:
作催化剂用1,2-丙二醇和尿素合成,原理如下:
回答下列问题:
(1)基态Zn原子的价电子排布式为
(2)尿素分子中,各元素电负性大小顺序为

 (填“>”或“<”)。
(填“>”或“<”)。(3)碳酸丙烯酸酯中C原子的杂化方式为
(4)
 能与
能与 形成稳定的配离子
形成稳定的配离子 ,其中配体的立体结构为
,其中配体的立体结构为 的键角比
的键角比 的键角大,试从物质结构的角度解释其原因
的键角大,试从物质结构的角度解释其原因(5)
 有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为
有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为 (写出计算式,阿伏加德罗常数的值为
(写出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
解题方法
2 . 工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是______ (填字母序号)。
a.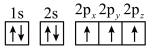 b.
b.
c.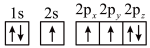 d.
d.
(2)写出CO的一种常见等电子体的结构式:_______ ;C、N、O的电负性由大到小的顺序为______ (用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们简单氢化物的沸点从高到低的顺序为______ ,其原因为______ 。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价, [Cu(NH3)2]+中中心离子的电子排布式为______ ,其中碳原子的杂化轨道类型是______ ,NH3分子的VSEPR模型为______ 。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:
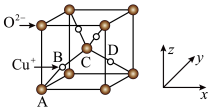
①若以A点为原点建立坐标系,A的坐标为(0,0,0),B的坐标为(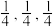 ),则D的坐标为
),则D的坐标为______ ;
②若阿伏加 德罗常数为NA,该晶胞的边长为a pm,则晶体的密度为______ g•cm-3。
(1)下列氮原子的电子排布图表示的状态中,能量最低的是
a.
 b.
b.
c.
 d.
d.
(2)写出CO的一种常见等电子体的结构式:
(3)与O同族的元素还有S、Se、Te,它们简单氢化物的沸点从高到低的顺序为
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价, [Cu(NH3)2]+中中心离子的电子排布式为
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:

①若以A点为原点建立坐标系,A的坐标为(0,0,0),B的坐标为(
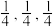 ),则D的坐标为
),则D的坐标为②若阿伏加 德罗常数为NA,该晶胞的边长为a pm,则晶体的密度为
您最近一年使用:0次



