解题方法
1 . 黑火药是我国古代四大发明之一,黑火药成分是硝酸钾、硫磺、木炭,反应原理为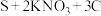


(1)氮原子的价层电子排布图为___________ ,K、S、N、O四种元素第一电离能由大到小的顺序为 ___________ 。上述反应涉及的五种元素中电负性最大的是 ___________ (填元素符号)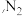 中
中 键与
键与 键个数比为
键个数比为 ___________ 。
(2) 与
与 相对分子质量值相差2,但二者熔沸点相差很大,原因是
相对分子质量值相差2,但二者熔沸点相差很大,原因是 ___________ 。
(3) 晶体中,
晶体中, 中中心原子杂化轨道类型是
中中心原子杂化轨道类型是 ___________ , 离子的立体构型是
离子的立体构型是 ___________ 。
(4)硫化钾的晶胞结构图如图。硫离子的配位数为___________ ,若晶胞中A点坐标为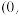 0,
0, ,B点坐标是
,B点坐标是 ,C点坐标是
,C点坐标是 ,则D点坐标为
,则D点坐标为 ___________ ,若晶胞参数为dpm,则该晶体的密度为 ___________  。(用含d、
。(用含d、 的代数式表示,设
的代数式表示,设 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)

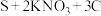


(1)氮原子的价层电子排布图为
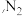 中
中 键与
键与 键个数比为
键个数比为 (2)
 与
与 相对分子质量值相差2,但二者熔沸点相差很大,原因是
相对分子质量值相差2,但二者熔沸点相差很大,原因是 (3)
 晶体中,
晶体中, 中中心原子杂化轨道类型是
中中心原子杂化轨道类型是  离子的立体构型是
离子的立体构型是 (4)硫化钾的晶胞结构图如图。硫离子的配位数为
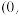 0,
0, ,B点坐标是
,B点坐标是 ,C点坐标是
,C点坐标是 ,则D点坐标为
,则D点坐标为  。(用含d、
。(用含d、 的代数式表示,设
的代数式表示,设 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)
您最近一年使用:0次
2 . 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为________ ;
②Fe的基态原子共有______ 种不同能级的电子;
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是_______ ;
②COCl2分子中σ键和π键的个数比为______ ,中心原子的杂化方式为_______ ;
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2 nm和7.8×10-2 nm,则熔点:NiO____ (填“>”、“<”或“=”)FeO;
(4)铁的某种单质的晶胞为面心立方结构,原子的配位数为_______ ,若铁原子半径为a nm,则该单质的密度为_______ g/cm3。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为
②Fe的基态原子共有
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是
②COCl2分子中σ键和π键的个数比为
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2 nm和7.8×10-2 nm,则熔点:NiO
(4)铁的某种单质的晶胞为面心立方结构,原子的配位数为
您最近一年使用:0次
名校
解题方法
3 . 利用 合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
(1)Mn2+的核外电子排布式为:________________ ,其单电子数为_________________ 。
(2)C、N、O、Mn电负性由大到小的顺序是___________ 。
(3) 也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为
也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为_____ 。
(4)蓝色物质KFe(Ⅲ)x[Fe(Ⅱ)(CN)6]可缓解重金属中毒,x=_______ ;该物质中不存在的作用力有_____ 。
A.范德华力 B.离子键 C.σ键 D.π键 E.氢键
(5)副族元素钴的氧化物可以在室温下完全氧化甲醛(HCHO)。甲醛分子的立体构型为_____ ;甲醛常温下为气体而甲醇(CH3OH)为液体的原因是________________________________ 。
(6)副族元素Mn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中(○为Se, 为Mn),该化合物的化学式为
为Mn),该化合物的化学式为________ ,Se的配位数为______ ,Mn和Se的摩尔质量分别为M1g/mol、M2g/mol,该晶体的密度为ρg/cm3,则Mn—Se键的键长为_____________ nm(计算表达式)。

 合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:(1)Mn2+的核外电子排布式为:
(2)C、N、O、Mn电负性由大到小的顺序是
(3)
 也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为
也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为(4)蓝色物质KFe(Ⅲ)x[Fe(Ⅱ)(CN)6]可缓解重金属中毒,x=
A.范德华力 B.离子键 C.σ键 D.π键 E.氢键
(5)副族元素钴的氧化物可以在室温下完全氧化甲醛(HCHO)。甲醛分子的立体构型为
(6)副族元素Mn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中(○为Se,
 为Mn),该化合物的化学式为
为Mn),该化合物的化学式为
您最近一年使用:0次
2018-01-11更新
|
660次组卷
|
4卷引用:四川省广安市眉山市2018届高三第一次诊断性考试理综化学试题
名校
解题方法
4 . 砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]________ 。
(2)根据元素周期律,元素的电负性Ga________ (填“大于”或“小于”,下同)As,第一电离能B________ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______________________ 。
(3)杀虫剂Na3AsO4中阴离子的空间构型为________ ,As原子采取________ 杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体,从F-和Cl-结构的不同分析其原因是_____________ 。
(5)原子晶体GaAs的晶胞参数a=x pm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为________ ;A原子距离B原子所在六面体的侧面的最短距离为________ (用x表示)pm;该晶体的密度为________ g·cm-3(阿伏伽德罗常数的值用NA表示)
 。
。
(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)杀虫剂Na3AsO4中阴离子的空间构型为
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体,从F-和Cl-结构的不同分析其原因是
(5)原子晶体GaAs的晶胞参数a=x pm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为
 。
。
您最近一年使用:0次
2017-03-11更新
|
129次组卷
|
3卷引用:四川省广安市第二中学2019届高三上学期第一次月考化学试题



