解题方法
1 . 按要求回答下列问题:
(1)KZnF3是一种良好的光学材料,基态F原子的价电子排布式为___________ ;基态Zn原子核外最高能层电子的电子云轮廓图形状为___________ ;K2CO3中阴离子的立体构型为___________ 。
(2)(CN)2、(SCN)2的性质与卤素单质相似,称为拟卤素,分子中每个原子最外层均满足8电子稳定结构,则(CN)2结构式为___________ ,其分子中σ键和π键的个数之比为___________ ;(SCN)2对应的氢化物有2种,测得硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S),其原因是___________ 。
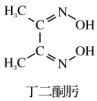
(3)丁二酮肟中C原子的杂化轨道类型为___________ ,其所含元素电负性由大到小的顺序为___________ (用元素符号表示)。
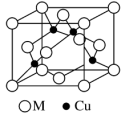
(4)某原子M的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示。该晶体中M原子和M原子之间的最短距离为apm,阿伏加德罗常数为NA,则该晶体的密度为___________ g·cm-3(只写计算式)。
(1)KZnF3是一种良好的光学材料,基态F原子的价电子排布式为
(2)(CN)2、(SCN)2的性质与卤素单质相似,称为拟卤素,分子中每个原子最外层均满足8电子稳定结构,则(CN)2结构式为
(3)丁二酮肟中C原子的杂化轨道类型为

(4)某原子M的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示。该晶体中M原子和M原子之间的最短距离为apm,阿伏加德罗常数为NA,则该晶体的密度为

您最近一年使用:0次
名校
解题方法
2 . 电镀工业上,为了提高镀锌的效果,通常采用Zn(CN)42-溶液代替Zn2+溶液进行电解。请回答下列问题:
(1)元素锌在周期表中的位置为_____________ ,基态Zn的价电子排布式为_____________ 。
(2)Zn(CN) 42-所含元素中,电负性最大的元素是_____________ ,Zn(CN) 42-中含有的化学键类型有σ键和_____________ 。
(3)CN-中C的杂化类型为_____________ ,与CN-互为等电子体的单质为_____________ 。
(4)H2CO3与HNO3的酸性相差较大,请解释其原因_____________ 。
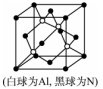
(5)N和Al可组成一种新型半导体材料AlN;AlN具有耐高温,耐磨性能。其晶体类型为_____________ ,其晶体结构如图,已知晶胞边长为apm,则AlN的密度为_____________ (用含a、NA的代数式表示)g/cm3。
(1)元素锌在周期表中的位置为
(2)Zn(CN) 42-所含元素中,电负性最大的元素是
(3)CN-中C的杂化类型为
(4)H2CO3与HNO3的酸性相差较大,请解释其原因
(5)N和Al可组成一种新型半导体材料AlN;AlN具有耐高温,耐磨性能。其晶体类型为

您最近一年使用:0次
2019-01-13更新
|
479次组卷
|
2卷引用:【市级联考】四川省资阳市高中2019届高三上学期第二次诊断性考试理科综合化学试题



