名校
解题方法
1 . NH3与甲醛CH2O反应可以制备乌洛托品(六亚甲基四胺,分子结构为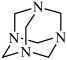 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
(1)基态氮原子的价电子轨道表达式为___________ ,第三电离能I3(C)___________ I3(N)(填“>”或“<)。
(2)NH3的空间构型为___________ ,CH2O中C采取的杂化类型为___________ 。CH2O中碳氢键与NH3中氮氢键相比,键长较长的是___________ 。
(3)乌洛托品为___________ (填“极性”或“非极性”)分子,分子中的所有N原子呈正四面体分布,所有C原子呈___________ 几何体分布,该分子可与H+形成配位键,电子对给予体为___________ 原子。
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为___________ 。乌洛托品比金刚烷(C10H16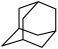 )水溶性更高,理由是
)水溶性更高,理由是___________ 。
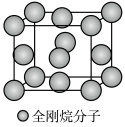
(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为___________ g/cm3。
 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:(1)基态氮原子的价电子轨道表达式为
(2)NH3的空间构型为
(3)乌洛托品为
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为
 )水溶性更高,理由是
)水溶性更高,理由是(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为

您最近一年使用:0次
2022-03-27更新
|
625次组卷
|
5卷引用:河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)
(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)四川省南充市2022届高三 适应性考试(二模)理综化学试题贵州省贵阳市五校2021-2022学年高三下学期联考理科综合化学试题(七)湖南省湘西自治州古丈县第一中学2021-2022学年高三下学期第二次模拟化学试题湖南省邵阳市第二中学2022-2023学年高三上学期第五次月考化学试题
名校
解题方法
2 . 金属冶炼过程中一种用有机化合物从水溶液中提取 的流程如下:
的流程如下:
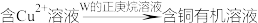
(1)有机化合物W的结构简式为:___________ 种,N、O杂化轨道类型分别为___________ 、___________ 。
(2)W可与 形成化合物Q,其结构如下所示:
形成化合物Q,其结构如下所示: 的价电子排布式为
的价电子排布式为___________ 。
②氢键对Q在水中溶解性的影响是___________ (填“增大”或“减小”)。
③W与 之间以共价键和配位键相结合,其中一定是配位键的是
之间以共价键和配位键相结合,其中一定是配位键的是___________ 键(填“Cu—O”或“Cu—N”)。
(3)有机化合物的合成通常使用催化剂,一种催化剂 晶体的晶胞示意图如下:
晶体的晶胞示意图如下:___________ (填元素符号)。与每个Y原子距离最近且等距的X原子有___________ 个。
②该晶胞边长为a nm,阿伏加德罗常数为 ,则该晶体的密度
,则该晶体的密度
___________  (列出计算式,
(列出计算式, 的摩尔质量为123
的摩尔质量为123  )。
)。
 的流程如下:
的流程如下: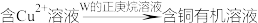
(1)有机化合物W的结构简式为:

(2)W可与
 形成化合物Q,其结构如下所示:
形成化合物Q,其结构如下所示:
 的价电子排布式为
的价电子排布式为②氢键对Q在水中溶解性的影响是
③W与
 之间以共价键和配位键相结合,其中一定是配位键的是
之间以共价键和配位键相结合,其中一定是配位键的是(3)有机化合物的合成通常使用催化剂,一种催化剂
 晶体的晶胞示意图如下:
晶体的晶胞示意图如下:
②该晶胞边长为a nm,阿伏加德罗常数为
 ,则该晶体的密度
,则该晶体的密度
 (列出计算式,
(列出计算式, 的摩尔质量为123
的摩尔质量为123  )。
)。
您最近一年使用:0次
2022-03-25更新
|
778次组卷
|
6卷引用:必刷卷03-2022年高考化学考前信息必刷卷(河北专用)
(已下线)必刷卷03-2022年高考化学考前信息必刷卷(河北专用)北京市丰台区2022届高三一模化学试题(已下线)化学-2022年高考押题预测卷02(山东卷)北京市第八中学2022-2023 学年高三上学期12 月月考化学试题 北京市第八中学2022-2023学年高二下学期期中考试化学练习题广东省广州市越秀区广东实验中学2023-2024学年高二下学期5月期中考试化学试题
2022·河北·模拟预测
解题方法
3 . 叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定等方面越来越引起人们的重视,其中氢叠氮酸( )是一种弱酸,分子结构示意图可表示为
)是一种弱酸,分子结构示意图可表示为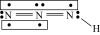 ,联氨被亚硝酸氧化时便可生成氢叠氮酸(
,联氨被亚硝酸氧化时便可生成氢叠氮酸( ):
): ,它的酸性类似于醋酸,微弱电离出
,它的酸性类似于醋酸,微弱电离出 和
和 。试回答下列问题:
。试回答下列问题:
(1)下列有关说法正确的是___________(填序号)。
(2)叠氮化物能与部分金属离子形成配合物,如 ,在该配合物中钴显
,在该配合物中钴显___________ 价,根据价层电子对互斥理论可知 的空间构型为
的空间构型为___________ ,写出钴原子在基态时的核外电子排布式:___________ 。
(3)与 互为等电子体的分子有
互为等电子体的分子有___________ (举2例)。
(4)人造立方氮化硼的硬度仅次于金刚石而远远高于其他材料,因它与金刚石统称为超硬材料。立方氮化硼晶胞如图所示,试分析:

①该晶体的类别为___________ 晶体。
②晶体中每个N原子同时吸引___________ 个B原子。
③设该晶体的摩尔质量为Mg/mol,晶体的密度为 ,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为
,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为___________ cm。
 )是一种弱酸,分子结构示意图可表示为
)是一种弱酸,分子结构示意图可表示为 ,联氨被亚硝酸氧化时便可生成氢叠氮酸(
,联氨被亚硝酸氧化时便可生成氢叠氮酸( ):
): ,它的酸性类似于醋酸,微弱电离出
,它的酸性类似于醋酸,微弱电离出 和
和 。试回答下列问题:
。试回答下列问题:(1)下列有关说法正确的是___________(填序号)。
A. 中含有5个σ键 中含有5个σ键 |
B. 中三个氮原子采用的都是sp2杂化 中三个氮原子采用的都是sp2杂化 |
C. 、 、 、 、 , , 都是极性分子 都是极性分子 |
D.肼( )沸点高达113.5℃,说明肼分子间可形成氢键 )沸点高达113.5℃,说明肼分子间可形成氢键 |
 ,在该配合物中钴显
,在该配合物中钴显 的空间构型为
的空间构型为(3)与
 互为等电子体的分子有
互为等电子体的分子有(4)人造立方氮化硼的硬度仅次于金刚石而远远高于其他材料,因它与金刚石统称为超硬材料。立方氮化硼晶胞如图所示,试分析:

①该晶体的类别为
②晶体中每个N原子同时吸引
③设该晶体的摩尔质量为Mg/mol,晶体的密度为
 ,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为
,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B原子之间的距离为
您最近一年使用:0次
名校
解题方法
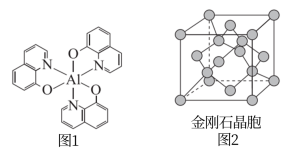
4 . 光电材料在能源军事等领域有重要应用,分为无机光电材料如ZnS、ZnSe、GaAs、 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:
(1)基态Zn原子的价层电子排布图为_____ ;Ga、As、Se的第一电离能由大到小的顺序为___________ 。
(2)图1所示化合物中所含有的化学键类型有_____ (填选项字母),N原子的杂化方式为_____ 。
A.共价键 B.离子键 C.配位键 D.氢键
(3)在水溶液中,以 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:
①表中氧化物之间沸点差异的原因为___________ 。
② 的VSEPR模型为
的VSEPR模型为___________ 。
③ 和
和 分子中,键角更大的是
分子中,键角更大的是___________ 。
(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为___________ 。
②若阿伏加德罗常数的值为 ,ZnS晶体的密度为
,ZnS晶体的密度为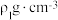 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为___________ 。
 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:(1)基态Zn原子的价层电子排布图为
(2)图1所示化合物中所含有的化学键类型有
A.共价键 B.离子键 C.配位键 D.氢键

(3)在水溶液中,以
 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:| 氧化物 |  |  |  |
| 沸点/℃ | 100 | -10 | -78.5 |
②
 的VSEPR模型为
的VSEPR模型为③
 和
和 分子中,键角更大的是
分子中,键角更大的是(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为
②若阿伏加德罗常数的值为
 ,ZnS晶体的密度为
,ZnS晶体的密度为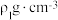 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
您最近一年使用:0次
2022-03-23更新
|
296次组卷
|
2卷引用:河北省张家口市2022届高三第一次模拟考试化学试题
解题方法
5 . 国内外学者近年来对金属-有机框架(MOFs)作为催化剂光解制氢和还原CO2等方面的研究取得了丰硕的成果。其中Masaya 等人利用Ti- MOF-NH2、H2PtCl6、 DMF 等原料制备了催化剂Pt/Ti- MOF-NH2。回答下列问题:
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是___________ ,处于_____ 区,未成对电子数是________ 。
(2)PtCl 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是___________ , 中心原子采用的杂化类型可能是___________ (填 “dsp2”“sp3”“sp2”或“sp3d2”)。

(3)DMF的结构是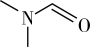 ,σ键与π键的数目比是
,σ键与π键的数目比是___________ ,其中N原子的杂化方式是___________ 。
(4)已知pKa=—lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因______ 。
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有___________ 个。若阿伏加德罗常数为NA, 干冰的密度为ρg·cm-3, 则晶胞体对角线长度是___________ cm。
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是
(2)PtCl
 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
(3)DMF的结构是
 ,σ键与π键的数目比是
,σ键与π键的数目比是(4)已知pKa=—lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有

您最近一年使用:0次
名校
解题方法
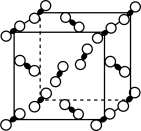
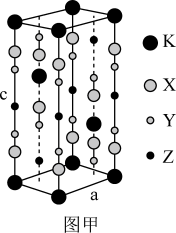
6 . 氟代硼铍酸钾晶体KBBF(KBe2BO3F2)是一种非线性光学晶体材料,广泛应用于激光、光刻录等领域,长方体晶胞如下图甲所示(其中K原子已经给出,氧原子略去)。回答下列问题:
(1)下列铍元素的不同微粒,若再失去一个电子需要能量最大的是 ___________。
(2)K2O2的阴阳离子比为___________ 。第四周期,与基态钾原子最外层电子数相同的原子有___________ (填元素符号)。
(3)OF2分子中氧原子的杂化类型是___________ ,空间构型为___________ 。
(4)KBBF所含元素中非金属元素的电负性由大到小的顺序是___________ 。
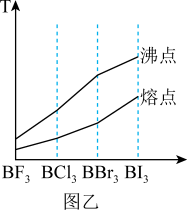
(5)三卤化硼的熔沸点如图乙所示,BF3、BCl3、BBr3、BI3的熔沸点变化的原因是___________ 。
(6)指出图甲中代表硼原子的字母为___________ ,该KBBF晶体的晶胞参数分别为apm和cpm,则晶体密度为___________ g·cm-3(M代表KBBF的摩尔质量,NA表示阿伏加德罗常数的值)。

(1)下列铍元素的不同微粒,若再失去一个电子需要能量最大的是 ___________。
A. | B.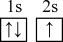 | C.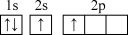 | D.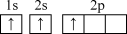 |
(3)OF2分子中氧原子的杂化类型是
(4)KBBF所含元素中非金属元素的电负性由大到小的顺序是
(5)三卤化硼的熔沸点如图乙所示,BF3、BCl3、BBr3、BI3的熔沸点变化的原因是

(6)指出图甲中代表硼原子的字母为
您最近一年使用:0次
2022-02-02更新
|
576次组卷
|
4卷引用:河北省衡水中学2021-2022学年高三下学期二调考试化学试题
河北省衡水中学2021-2022学年高三下学期二调考试化学试题安徽省蚌埠市2021-2022学年高三上学期第二次教学质量检查理综化学试题(已下线)【直击双一流】05-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)
名校
解题方法
7 . 铜是人类广泛使用的第一种金属,含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)基态 原子最高能层的电子排布式为
原子最高能层的电子排布式为___________ 。
(2) 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。
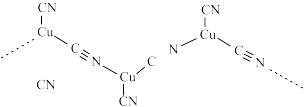
(3) 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为___________ 。
(4)铜能与拟卤素 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸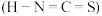 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为___________ ;写出一种与 互为等电子体的分子式
互为等电子体的分子式___________ 。
(5) 可形成
可形成 ,其中
,其中 代表
代表 。
。
①该化合物分子中, 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有___________ 个。
②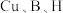 的电负性由大到小的顺序为
的电负性由大到小的顺序为___________ 。
(6)一种由 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
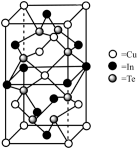
① 的配位数为
的配位数为___________ ;晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ 。
②若晶胞底边的边长均为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态
 原子最高能层的电子排布式为
原子最高能层的电子排布式为(2)
 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。A. | B. | C. | D. |
 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为
(4)铜能与拟卤素
 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸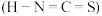 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为 互为等电子体的分子式
互为等电子体的分子式(5)
 可形成
可形成 ,其中
,其中 代表
代表 。
。①该化合物分子中,
 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有②
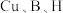 的电负性由大到小的顺序为
的电负性由大到小的顺序为(6)一种由
 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
①
 的配位数为
的配位数为 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为②若晶胞底边的边长均为
 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2021-12-03更新
|
1003次组卷
|
5卷引用:河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题
河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题河北省石家庄市2022届高三上学期教学质量检测(一)化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】20(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广东省佛山市李兆基中学、郑裕彤中学两校2021-2022学年高三下学期3月联考化学试题
解题方法
8 . 碳、氮及其化合物广泛存在于自然界中,回答下列问题:
(1)科学家已证实,存在一种空心且类似于足球结构的物质N60,它可能成为一种很好的火箭燃料。固态N60的晶体类型为_______ 。
(2)氰酸是一种无机物,化学式为HCNO,是一种具有挥发性和腐蚀性的液体,高毒。HCNO的组成元素中第一电离能最小的是_______ (填元素符号,下同),电负性最大的是_______ 。
(3)镍能形成多种配合物,如正四面体形的Ni(CO)4,、正方形的 和正八面体形的
和正八面体形的 。下列说法不正确的是
。下列说法不正确的是_______ (填标号)。
A. CO分子内σ键和π键的数目之比为1:2
B. NH3的空间构型为平面三角形
C. Ni2+在形成配合物时,其配位数可能为4或6
D. Ni(CO)4和 中,镍元素均是sp3杂化
中,镍元素均是sp3杂化
(4)化合物(CH3)3N能溶于水,其原因是_______ ,(CH3)3N与盐酸反应生成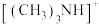 ,
,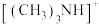 中新生成的化学键的类型为
中新生成的化学键的类型为_______ 。
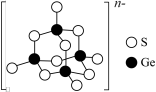
(5)阳离子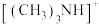 和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是
和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是_______ ,阴离子A的化学式为_______ 。
(6)某碳单质的晶胞结构如图所示,回答下列问题:

①该晶胞中含_______ 个C原子。
②将每个C原子视为一个球,若C原子的半径为R,1个C原子的体积为V,1个晶胞的体积为V0,堆积系数 ,则该晶体的堆积系数
,则该晶体的堆积系数
_______ (保留1位有效数字,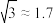 ,
, )。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
)。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
(1)科学家已证实,存在一种空心且类似于足球结构的物质N60,它可能成为一种很好的火箭燃料。固态N60的晶体类型为
(2)氰酸是一种无机物,化学式为HCNO,是一种具有挥发性和腐蚀性的液体,高毒。HCNO的组成元素中第一电离能最小的是
(3)镍能形成多种配合物,如正四面体形的Ni(CO)4,、正方形的
 和正八面体形的
和正八面体形的 。下列说法不正确的是
。下列说法不正确的是A. CO分子内σ键和π键的数目之比为1:2
B. NH3的空间构型为平面三角形
C. Ni2+在形成配合物时,其配位数可能为4或6
D. Ni(CO)4和
 中,镍元素均是sp3杂化
中,镍元素均是sp3杂化(4)化合物(CH3)3N能溶于水,其原因是
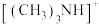 ,
,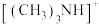 中新生成的化学键的类型为
中新生成的化学键的类型为(5)阳离子
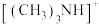 和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是
和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是
(6)某碳单质的晶胞结构如图所示,回答下列问题:

①该晶胞中含
②将每个C原子视为一个球,若C原子的半径为R,1个C原子的体积为V,1个晶胞的体积为V0,堆积系数
 ,则该晶体的堆积系数
,则该晶体的堆积系数
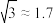 ,
, )。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
)。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
您最近一年使用:0次
2021-07-15更新
|
150次组卷
|
2卷引用:河北省部分名校2020-2021学年高二下学期期末联考化学试题
名校
9 . 南京理工大学化工学院胡炳成教授团队成功合成世界首个全氮阴离子盐,其局部结构如图所示。下列说法错误的是

A.经 射线衍射可以测得全氮阴离子盐晶体结构 射线衍射可以测得全氮阴离子盐晶体结构 |
| B.全氮阴离子盐两种阳离子中心原子的杂化轨道类型相同 |
C.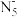 中所有的氮原子在同一平面内 中所有的氮原子在同一平面内 |
D. 的键角比全氮阴离子盐的两种阳离子键角都大 的键角比全氮阴离子盐的两种阳离子键角都大 |
您最近一年使用:0次
2021-07-07更新
|
763次组卷
|
3卷引用:河北省秦皇岛市第一中学2022-2023学年高二上学期期末考试化学试题
真题
解题方法
10 . KH2PO4晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是__ (填离子符号)。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为___ 。
(3)已知有关氮、磷的单键和三键的键能(kJ•mol-1)如表:
___ ,其中P采取___ 杂化方式。
(5)与PO 电子总数相同的等电子体的分子式为
电子总数相同的等电子体的分子式为__ 。
(6)磷酸通过分子间脱水缩合形成多磷酸,如:___ 。
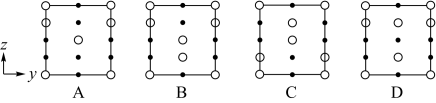
(7)分别用○、●表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置:
、K+在晶胞xz面、yz面上的位置:__ g•cm-3(写出表达式)。
②晶胞在x轴方向的投影图为__ (填标号)。
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为(3)已知有关氮、磷的单键和三键的键能(kJ•mol-1)如表:
| N—N | N≡N | P—P | P≡P |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以N2、而白磷以P4(结构式可表示为 )形式存在的原因是
)形式存在的原因是
(5)与PO
 电子总数相同的等电子体的分子式为
电子总数相同的等电子体的分子式为(6)磷酸通过分子间脱水缩合形成多磷酸,如:

(7)分别用○、●表示H2PO
 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置:
、K+在晶胞xz面、yz面上的位置:
②晶胞在x轴方向的投影图为
您最近一年使用:0次
2021-06-09更新
|
10150次组卷
|
12卷引用:2021年新高考河北化学高考真题
2021年新高考河北化学高考真题2021年河北省高考化学试卷变式题10-18题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷15题 物质结构与性质综合题-备战2022年高考化学临考题号押题(新高考通版)广东省广州市天河区2022届高三第三次模拟考试化学试题(已下线)专题18 物质结构与性质(综合题)-三年(2020-2022)高考真题分项汇编(已下线)专题20 结构与性质(已下线)专题20 结构与性质



