江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题
江西
高二
阶段练习
2020-12-22
262次
整体难度:
容易
考查范围:
化学反应原理、认识化学科学
江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题
江西
高二
阶段练习
2020-12-22
262次
整体难度:
容易
考查范围:
化学反应原理、认识化学科学
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
您最近一年使用:0次
2021-10-22更新
|
173次组卷
|
12卷引用:安徽省广德县实验中学2020-2021学年高二上学期10月月考化学试题
安徽省广德县实验中学2020-2021学年高二上学期10月月考化学试题江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题四川省广安市北京师范大学广安实验学校2020-2021学年高二上学期12月考试化学试题吉林省延边第二中学2020-2021学年高二上学期第一次考试月考化学试题四川省成都市简阳市阳安中学2021-2022学年高二上学期9月月考化学试卷河北深州市长江中学2021-2022学年高二上学期10月月考化学(理)试题青海省西宁市北外附属新华联国际学校2021-2022学年高二上学期第一次月考化学(理)试题广西百色中学2021-2022学年高二上学期第一次月考化学试题安徽省肥东凯悦中学2021-2022学年高二上学期第一次月考化学试题浙江省海盐第二高级中学2022-2023学年高二上学期10月第一阶段检测化学试题陕西省西安市鄠邑区第二中学2021-2022学年高二上学期第一次月考化学试题云南省昆明市昆明行知中学2021-2022学年高二上学期第一次质量检测(10月)化学试题
单选题
|
适中(0.65)
名校
2. 下列说法或表示方法中正确的是( )
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=-2×57.3kJ·mol-1 |
| B.相同条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| C.由C(金刚石)=C(石墨)ΔH=-1.9kJ·mol-1可知,金刚石比石墨稳定 |
| D.若CO(g)的燃烧热ΔH=-283.0kJ·mol-1,则反应2CO2(g)=2CO(g)+O2(g)的ΔH=+2×283.0kJ·mol-1 |
【知识点】 中和热 燃烧热 化学能与物质稳定性之间的关系解读
您最近一年使用:0次
2020-11-13更新
|
223次组卷
|
7卷引用:广西壮族自治区柳江中学2020-2021学年度高二上学期期中检测化学试题
单选题
|
较易(0.85)
名校
解题方法
3. 化学反应4A(s)+3B(g) 2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示正确的是( )
2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示正确的是( )
 2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示正确的是( )
2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示正确的是( )| A.用A表示的反应速率是0.4 mol·L-1·min-1 |
| B.前2 min,v正(B)和v逆(C)表示的反应速率的值都是逐渐减小的 |
| C.2 min末的反应速率用B表示是0.3 mol·L-1·min-1 |
| D.用C表示的反应速率是0.2 mol·L-1·min-1 |
您最近一年使用:0次
2020-11-10更新
|
164次组卷
|
2卷引用:河北省黄骅中学2020-2021学年高二上学期第一次月考化学试题
单选题
|
较易(0.85)
名校
4. 已知反应2CO(g)+4H2(g) CH2=CH2(g)+2H2O(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
CH2=CH2(g)+2H2O(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
 CH2=CH2(g)+2H2O(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
CH2=CH2(g)+2H2O(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )| A.v(H2O)=0.1mol·L-1·s-1 | B.v(H2)=4.5mol·L-1·s-1 |
| C.v(CH2=CH2)=0.03mol·L-1·s-1 | D.v(CO)=1.5mol·L-1·s-1 |
您最近一年使用:0次
2020-11-10更新
|
169次组卷
|
3卷引用:河北省邢台市2020-2021学年高二上学期期中考试化学试题
5. 把lmol CO2和3mol H2通入1L的密闭容器中,在某温度下发生反应:CO2 (g)+3H2 (g) CH3OH (g) +H2O(g)(△H<0)。测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是
CH3OH (g) +H2O(g)(△H<0)。测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是

 CH3OH (g) +H2O(g)(△H<0)。测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是
CH3OH (g) +H2O(g)(△H<0)。测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是
| A.3min时,v正=v逆 |
| B.0-10min 内,用H2表示的反应速率为2.25 mol·L·min-1 |
| C.该温度下,反应达到平衡时,H2的转化率为75% |
| D.若升高温度,则CO2的转化率增大 |
您最近一年使用:0次
2020-11-13更新
|
440次组卷
|
6卷引用:鲁科版(2019)高一必修第二册 模块综合测评 A卷
单选题
|
适中(0.65)
名校
6. 对可逆反应2A(s)+3B(g) C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动;②升高温度,平衡向逆反应方向移动,v(逆)增大,v(正)减小;③压强增大一倍,平衡不移动,v(正)、v(逆)不变;④增大B的浓度,v(正)>v(逆);⑤加入催化剂,B的转化率提高
 C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )①增加A的量,平衡向正反应方向移动;②升高温度,平衡向逆反应方向移动,v(逆)增大,v(正)减小;③压强增大一倍,平衡不移动,v(正)、v(逆)不变;④增大B的浓度,v(正)>v(逆);⑤加入催化剂,B的转化率提高
| A.①② | B.④ | C.③④ | D.④⑤ |
您最近一年使用:0次
2020-11-13更新
|
149次组卷
|
2卷引用:广西壮族自治区柳江中学2020-2021学年度高二上学期期中检测化学试题
单选题
|
适中(0.65)
名校
解题方法
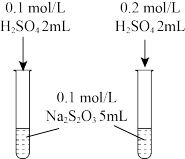
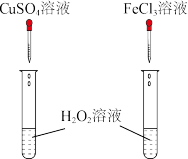
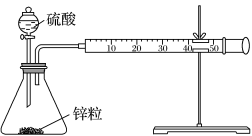
7. 下列实验方案,不能达到相应实验目的的是( )
| A | B | C | D |
|
|
|
|
| 探究H2SO4浓度对化学反应速率的影响 | 比较Cu2+、Fe3+对H2O2分解速率的影响 | 定量测量化学反应速率 | 探究反应中的热量变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-24更新
|
546次组卷
|
9卷引用:河北省邢台市巨鹿中学2020-2021学年高二上学期第一次月考化学试题
河北省邢台市巨鹿中学2020-2021学年高二上学期第一次月考化学试题成都市实验外国语学校(西区)2020-2021学年高二上学期化学学科期中测试卷江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题重庆市第七中学校2020-2021学年高二上学期12月考化学试题河北省巨鹿中学2020-2021学年高二下学期第一次月考化学试题吉林省长春市农安县2021-2022学年高一下学期学情调研化学试题(已下线)第05练 化学反应的速率与限度-2023年【暑假分层作业】高一化学(人教版2019必修第二册)吉林省长春市绿园区长春市新解放学校2022-2023学年高一下学期6月期中化学试题(已下线)清单04 化学反应的速率和限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
单选题
|
适中(0.65)
名校
解题方法
8. 已知:NO2(g)+CO(g) NO(g)+CO2(g)△H。一定温度下, 1 mol NO2(g)与1 molCO(g)完全反应生成CO2(g)和NO(g)过程中的能量变化如图所示。下列说法不正确的是
NO(g)+CO2(g)△H。一定温度下, 1 mol NO2(g)与1 molCO(g)完全反应生成CO2(g)和NO(g)过程中的能量变化如图所示。下列说法不正确的是
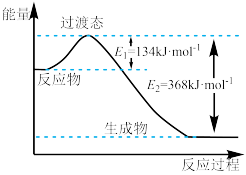
 NO(g)+CO2(g)△H。一定温度下, 1 mol NO2(g)与1 molCO(g)完全反应生成CO2(g)和NO(g)过程中的能量变化如图所示。下列说法不正确的是
NO(g)+CO2(g)△H。一定温度下, 1 mol NO2(g)与1 molCO(g)完全反应生成CO2(g)和NO(g)过程中的能量变化如图所示。下列说法不正确的是
| A.△H=-234kJ•mol-1 |
| B.该反应的逆反应的活化能为368kJ•mol-1 |
| C.加入高效催化剂,E1、E2均减小 |
| D.其他条不变,缩小容器体积,活化分子百分数增大 |
【知识点】 焓变 碰撞理论及活化能解读 催化剂对化学反应速率的影响解读
您最近一年使用:0次
2020-11-12更新
|
282次组卷
|
3卷引用:河北省武安市第三中学2021届高三上学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
9. 在一个绝热恒容的密闭容器中发生可逆反应:mA(g)+nB(g) pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明该反应达到平衡状态的是
pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明该反应达到平衡状态的是
| A.体系的压强不再改变 | B.混合气体的密度不再改变 |
| C.v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q | D.体系的温度不再变化 |
【知识点】 化学平衡状态本质及特征解读 化学平衡状态的判断方法解读
您最近一年使用:0次
2020-11-10更新
|
108次组卷
|
3卷引用:河北省保定市唐县第一中学20202-2021学年高二上学期第二次月考化学试卷题
单选题
|
适中(0.65)
名校
解题方法
10. 25℃时,水的电离达到平衡H2O H++OH-△H>0,下列叙述正确的是( )
H++OH-△H>0,下列叙述正确的是( )
 H++OH-△H>0,下列叙述正确的是( )
H++OH-△H>0,下列叙述正确的是( )| A.将水加热,Kw增大,pH不变 |
| B.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| C.向水中加入少量固体NaHSO4,c(H+)增大,Kw不变 |
| D.该温度下的0.01mol/L稀盐酸溶液中,由水电离的c(H+)=1×10-2mol/L |
您最近一年使用:0次
2020-11-12更新
|
261次组卷
|
4卷引用:成都市实验外国语学校(西区)2020-2021学年高二上学期化学学科期中测试卷
单选题
|
适中(0.65)
名校
解题方法
11. 25 ℃时,某溶液中水电离出的c(H+)=10-5mol·L-1,则该溶液可能是下列情况中的( )
| A.该溶液可能是酸溶液 |
| B.该溶液可能是碱溶液 |
| C.该溶液中c(OH-)可能是10-5mol·L-1 |
| D.该溶液与pH=9的氢氧化钠等体积混合,混合后溶液肯定呈中性 |
您最近一年使用:0次
2020-11-11更新
|
215次组卷
|
4卷引用:甘肃省静宁县第一中学2020-2021学年高二上学期第二次月考(实验班)化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 关于下列各实验或装置的叙述中,不正确的是
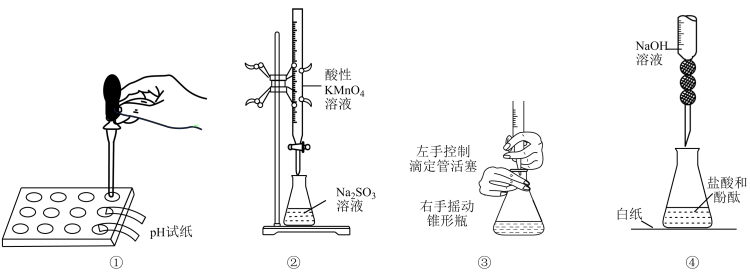

| A.①可用于测溶液pH |
B.②是用酸性 溶液滴定 溶液滴定 溶液 溶液 |
| C.③是滴定操作时手的操作 |
| D.④中滴入半滴NaOH标准液使溶液由无色变为粉红色,即达到滴定终点 |
您最近一年使用:0次
2021-08-07更新
|
616次组卷
|
15卷引用:第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)
(已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时3 酸碱中和滴定河南省焦作市博爱县英才学校2020-2021学年高二上学期11月月考化学试题江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题山西省太原市第五中学2020-2021学年高二上学期12月阶段性检测化学试题四川省成都市郫都区川科外国语学校2020-2021学年高二11月月考化学试题陕西省咸阳市2020-2021学年高二上学期期末质量检测化学试题选择性必修1(SJ)专题3第二单元课时2 酸碱中和滴定选择性必修1 专题3 第二单元 课时2 酸碱中和滴定辽宁省铁岭市调兵山市第二高级中学2020-2021学年度高二下学期期末考试化学试题(已下线)3.2.2 酸碱中和滴定-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第11练 酸碱中和滴定-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)黑龙江省七台河市勃利县高级中学2021-2022学年高二上学期9月月考化学试题安徽省涡阳第一中学2021-2022学年高二上学期第二次教学质量检测化学试题3.2.2酸碱中和滴定 课中
单选题
|
较易(0.85)
名校
13. 下列说法正确的是
| A.pH=1的醋酸加水稀释到原体积的100倍,稀释后pH=3 |
| B.室温下pH=3的醋酸溶液和pH=11的Ba(OH)2溶液等体积混合后溶液呈酸性 |
| C.把pH试纸直接插入待测溶液中,测其pH |
| D.某温度下,水的离子积常数为1×10-12,该温度下pH=7的溶液呈中性 |
您最近一年使用:0次
2020-11-04更新
|
293次组卷
|
4卷引用:黑龙江省齐齐哈尔市第八中学2020-2021学年高二上学期期中考试化学试题
单选题
|
较易(0.85)
名校
14. 醋酸溶液中存在电离平衡 CH3COOH H++ CH3COO-,下列叙述不正确的是( )
H++ CH3COO-,下列叙述不正确的是( )
 H++ CH3COO-,下列叙述不正确的是( )
H++ CH3COO-,下列叙述不正确的是( )| A.升高温度,平衡正向移动,醋酸的电离常数 Ka 值增大 |
| B.0.10 mol·L-1 的 CH3 COOH 溶液中加水稀释,溶液中 c(H+)减小 |
| C.CH3COOH 溶液中加少量的 CH3COONa 固体,平衡逆向移动 |
| D.25℃时,欲使醋酸的电离常数 Ka 和电离程度都减小,可加入少量冰醋酸 |
您最近一年使用:0次
2020-11-12更新
|
267次组卷
|
3卷引用:甘肃省兰州市第一中学2020-2021学年高二上学期期中考试化学(理)试题
单选题
|
较易(0.85)
名校
15. 常温下,下列各溶液中微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1的Na2CO3溶液中:c(OH-)=c( )+c(H+)+c(H2CO3) )+c(H+)+c(H2CO3) |
B.将pH=6的H2SO4稀释1000倍后,c(H+)=2c( ) ) |
| C.浓度分别为0.1 mol·L-1和0.01 mol·L-1的CH3COOH溶液中:c(CH3COO-)前者是后者的10倍 |
| D.NaA溶液的pH=8,c(Na+)-c(A-)=9.9×10-7 mol·L-1 |
您最近一年使用:0次
2020-11-13更新
|
279次组卷
|
4卷引用:天津地区2021届高三上学期期中考试模拟测化学试题
天津地区2021届高三上学期期中考试模拟测化学试题江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题(已下线)小题必刷29 弱电解质的电离平衡——2021年高考化学一轮复习小题必刷(通用版本)山西省沁县中学2020-2021学年高二上学期第二次月考化学试题
单选题
|
适中(0.65)
名校
16. 现有室温下四种溶液,有关叙述不正确的是
| 序号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A.③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 |
| B.分别取③、④溶液等体积加入足量的锌粒,产生氢气的量③>④ |
| C.分别加水稀释10倍,四种溶液的pH ①>②>④>③ |
| D.V1 L① 与V2 L ④混合,若混合后溶液pH=7,则V1=V2 |
您最近一年使用:0次
2019-11-13更新
|
1809次组卷
|
11卷引用:黑龙江省哈尔滨市第六中学2020届高三上学期期中考试化学试题
黑龙江省哈尔滨市第六中学2020届高三上学期期中考试化学试题辽宁省大连市第三中学2019-2020学年高三上学期第三次月考化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时1 水的电离 溶液的酸碱性与pH黑吉两省十校2020-2021学年高二上学期期中联考(吉雅2校用)化学试题江西省南昌市八一中学2020-2021学年高二上学期期中考试化学试题江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题山西省沁县中学2020-2021学年高二上学期第二次月考化学试题吉林省吉林市江城中学2021届高三上学期12月月考化学试题选择性必修1 专题3 第二单元 课时1 溶液的酸碱性云南省马关县第一中学2021-2022学年高二下学期开学考试化学试题3.2.1溶液的酸碱性 课后
二、填空题 添加题型下试题
填空题
|
容易(0.94)
名校
17. 2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1 mol气态水过程中的能量变化图。

(1)该反应反应物的总能量______ 生成物的总能量,属于_______ (填“吸热”或“放热”)反应。
(2)写出该火箭推进器中相关反应的热化学方程式:___________ 。
(3)若该火箭推进器中有36g H2O生成,则转移的电子数为___________ mol。

(1)该反应反应物的总能量
(2)写出该火箭推进器中相关反应的热化学方程式:
(3)若该火箭推进器中有36g H2O生成,则转移的电子数为
您最近一年使用:0次
2020-12-13更新
|
379次组卷
|
5卷引用:江西省鹰潭市贵溪市实验中学2020--2021学年高二上学期第二次月考化学试题
填空题
|
适中(0.65)
名校
解题方法
18. T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C的变化如图所示。
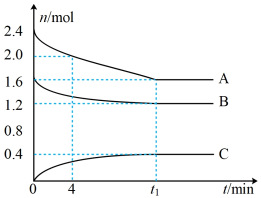
(1)写出反应的化学方程式______ 。
(2)0~4min时,A的平均反应速率为______ 。
(3)已知:K(300℃)>K(350℃),该反应是______ (填“吸热”或“放热”)反应。
(4)T℃时,反应的平衡常数为______ (保留到小数点后2位)。
(5)到达平衡时B的转化率为______ 。
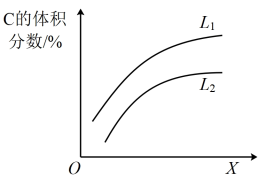
(6)如图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是______ (填“温度”或“压强”)。判断L1_____ L2(填“>”或“<”),理由是_____ 。

(1)写出反应的化学方程式
(2)0~4min时,A的平均反应速率为
(3)已知:K(300℃)>K(350℃),该反应是
(4)T℃时,反应的平衡常数为
(5)到达平衡时B的转化率为
(6)如图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是

您最近一年使用:0次
2020-11-09更新
|
438次组卷
|
5卷引用:北京市丰台区 2020-2021 学年高三上学期期中考试化学试题
填空题
|
较易(0.85)
名校
19. 水体中的含氮化合物是引起富营养化的主要污染物,分析监测水体中的硝酸(盐)和亚硝酸(盐)含量,控制水体中的含氮污染物,对水资源的循环利用意义重大。
(1)亚硝酸(HNO2)是一种弱酸,其电离方程式为___________ ,其电离平衡常数的表达式为___________ 。
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为___________ 。
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为___________ ,其中氧化产物为___________ (写化学式)。
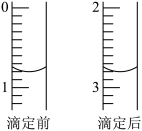
③取20mL含NaNO2的水样,酸化后用0.001mol/L的KI标准溶液滴定(反应中含N的生成物为NO),滴定前和滴定后的滴定管内液面高度如图所示,由此可知水样中NaNO2的浓度为___________ mg/L。
(1)亚硝酸(HNO2)是一种弱酸,其电离方程式为
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为
③取20mL含NaNO2的水样,酸化后用0.001mol/L的KI标准溶液滴定(反应中含N的生成物为NO),滴定前和滴定后的滴定管内液面高度如图所示,由此可知水样中NaNO2的浓度为

您最近一年使用:0次
填空题
|
较易(0.85)
名校
20. 弱酸的电离平衡常数与对应酸根的水解平衡常数存在某种定量关系。
(1)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是___ (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___ (填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为___ mol·L-1(NH3·H2O的电离平衡常数取Kb=2×10-5)。
(2)已知常温下CN-的水解常数Kh=1.61×10-5。
①含等物质的量浓度HCN与NaCN的混合溶液显___ (填“酸”“碱”或“中”)性,c(CN-)___ (填“>”“<”或“=”)c(HCN)。溶液中各离子浓度由大到小的顺序为___ 。
②常温下,若将cmol·L-1的盐酸与0.62mol·L-1的KCN等体积混合后恰好得到中性溶液,则c=___ (小数点后保留4位数字)。
(1)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是
(2)已知常温下CN-的水解常数Kh=1.61×10-5。
①含等物质的量浓度HCN与NaCN的混合溶液显
②常温下,若将cmol·L-1的盐酸与0.62mol·L-1的KCN等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
2020-11-04更新
|
131次组卷
|
2卷引用:安徽涡阳县育萃中学2020-2021学年高二上学期第二次月考化学试题
试卷分析
整体难度:适中
考查范围:化学反应原理、认识化学科学
试卷题型(共 20题)
题型
数量
单选题
16
填空题
4
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 吸热反应和放热反应 | |
| 2 | 0.65 | 中和热 燃烧热 化学能与物质稳定性之间的关系 | |
| 3 | 0.85 | 化学反应速率含义、单位 化学反应速率计算 化学反应速率与化学计量数之间的关系 浓度对化学反应速率的影响 | |
| 4 | 0.85 | 化学反应的速率 化学反应速率的定量表示方法 化学反应速率计算 化学反应速率与化学计量数之间的关系 | |
| 5 | 0.85 | 化学反应速率与化学计量数之间的关系 转化率的相关计算及判断 化学平衡题中基于图表数据的相关计算 | |
| 6 | 0.65 | 影响化学反应速率的因素 浓度对化学平衡移动的影响 温度对化学平衡移动的影响 压强对化学平衡移动的影响 | |
| 7 | 0.65 | 测定某些反应的反应速率 浓度对化学反应速率的影响 催化剂对化学反应速率的影响 化学反应条件控制的相关实验 | |
| 8 | 0.65 | 焓变 碰撞理论及活化能 催化剂对化学反应速率的影响 | |
| 9 | 0.65 | 化学平衡状态本质及特征 化学平衡状态的判断方法 | |
| 10 | 0.65 | 水的离子积常数 影响水电离的因素 | |
| 11 | 0.65 | 溶液pH的计算 水溶液中水的电离程度及的计算 溶液的酸碱性与pH的关系 | |
| 12 | 0.65 | 酸碱中和滴定实验基本操作及步骤 酸碱中和滴定实验相关仪器 酸碱中和滴定指示剂选择 | |
| 13 | 0.85 | 溶液的酸碱性与pH的关系 测定溶液pH的方法 酸碱混合时的定性判断及计算 浓度对电离平衡的影响 | |
| 14 | 0.85 | 电离平衡常数及影响因素 浓度对电离平衡的影响 同离子效应对电离的影响 温度对电离平衡的影响 | |
| 15 | 0.85 | 浓度对电离平衡的影响 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 16 | 0.65 | 溶液稀释后pH的计算 弱电解质的电离平衡 弱电解质电离平衡的影响因素 一元强酸与一元弱酸的比较 | |
| 二、填空题 | |||
| 17 | 0.94 | 化学反应热的计算 热化学方程式 | |
| 18 | 0.65 | 化学平衡的有关计算 化学平衡图像分析 产物的物质的量与温度、压强的图像关系分析 化学反应速率与化学平衡的综合应用 | |
| 19 | 0.85 | 氧化还原反应方程式的配平 酸碱中和滴定原理的应用 弱电解质的电离平衡常数 | |
| 20 | 0.85 | 弱电解质的电离平衡 电离平衡常数及影响因素 影响盐类水解程度的主要因素 盐的水解常数 | |

 稀释
稀释 溶于水
溶于水 在
在 中燃烧
中燃烧