30. 某小组进行测定某变质的铁铝合金(杂质主要为Al
2O
3和Fe
2O
3)样品中铁含量,并制备Fe
3O
4胶体粒子,相关实验方案设计如下:
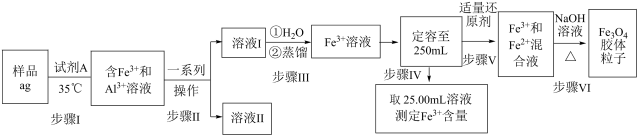
已知:乙醚[(C
2H
5)
2O]易燃,沸点为34.5度,微溶于水,密度比水小。在较高的盐酸浓度下,Fe
3+与HCl、乙醚形成化合物[(C
2H
5)
2OH][FeCl
4]而溶于乙醚;当盐酸浓度降低时,该化合物解离。
请回答下列问题:
(1)溶液II中主要金属阳离子是
__________________。
(2)步骤I中试剂A
最佳选择的是
_____________。
A.浓硝酸
B.浓硫酸
C.浓盐酸+双氧水
D.稀盐酸+双氧水
(3)步骤II的“一系列操作”包括如下实验步骤,选出其正确操作并按序列出字母:分液漏斗中加水检验是否漏水→向溶液中加入适量浓盐酸和乙醚,转移至分液漏斗→
( )→
( )→
( )→
( )→f→
( )→a→
( )→d→
( )。
a.左手拇指和食指旋开旋塞放气;
b.用右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转,并用力振摇;
c.静置分层;
d.打开上口玻璃塞,将下层液体从下口放出,上层液体从上口倒出;
e.混合两次分液后的上层液体;
f.向下层液体中加入浓盐酸和乙醚并转移至分液漏斗;
(4)下列关于步骤Ⅲ和步骤VI的涉及的操作说法正确的是
_______________。
A.步骤Ⅲ中蒸馏操作时,为加快蒸馏速度,采用酒精灯大火加热,收集34.5℃的馏分
B.为减少乙醚挥发,在蒸馏操作时,收集乙醚的锥形瓶应放置在冰水浴中
C.步骤VI由混合溶液制得Fe
3O
4胶体粒子的过程中,须持续通入N
2,防止Fe
2+被氧化
D.析出Fe
3O
4胶体粒子后通过抽滤,洗涤,干燥获得Fe
3O
4胶体粒子
(5)步骤IV测定Fe
3+方法有多种,如转化为Fe
2O
3,间接碘量滴定,分光光度法等。
①步骤IV主要作用是测定样品中的铁总含量和
______________________。
②步骤IV实验时采用间接碘量法测定Fe
3+含量,具体过程如下:向25.00mL溶液中加入过量KI溶液,充分反应后,滴入几滴淀粉作指示剂,用0.1000mol·L
-1Na
2S
2O
3标准溶液进行滴定,到达滴定终点时,消耗Na
2S
2O
3标准溶液体积为VmL。已知滴定反应为:I
2+2Na
2S
2O
3=2NaI+Na
2S
4O
6。不考虑Fe
3+和I
-反应限度和滴定操作问题,实际测定的Fe含量往往偏高,其主要原因是
________________________________________。