名校
解题方法
1 . 在密闭系统中有反应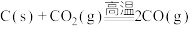 能使反应速率增大的措施是
能使反应速率增大的措施是
①升高温度 ②将炭粉碎 ③增加炭的量 ④恒容条件下通入 ⑤恒容条件下分离出一氧化碳
⑤恒容条件下分离出一氧化碳
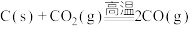 能使反应速率增大的措施是
能使反应速率增大的措施是①升高温度 ②将炭粉碎 ③增加炭的量 ④恒容条件下通入
 ⑤恒容条件下分离出一氧化碳
⑤恒容条件下分离出一氧化碳| A.①②③④ | B.①②④⑤ | C.①②④ | D.①②③④⑤ |
您最近一年使用:0次
名校
2 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 与足量的S反应转移的电子数为 与足量的S反应转移的电子数为 |
B.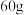 二氧化硅含有 二氧化硅含有 键的数目为 键的数目为 |
C.一定条件下,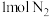 与足量氢气反应,产生 与足量氢气反应,产生 的分子数为 的分子数为 |
D.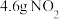 与 与 的混合气体中含有的原子数目为 的混合气体中含有的原子数目为 |
您最近一年使用:0次
名校
解题方法
3 . 化学反应速率的调控在工农业生产和日常生活中有重要作用,下列说法正确的是
| A.压强越大,反应速率越快,因此在化工生产中采取的压强越大越好 |
| B.对于任何化学反应来说,反应速率越大,反应现象越明显 |
| C.在钢铁护栏表面刷油漆可以减慢钢铁生锈的速率 |
| D.在室外,夏天面粉发酵速度与冬天面粉发酵速度相差不大 |
您最近一年使用:0次
4 . 化学与生产、生活、科技、环境等密切相关。下列说法正确的是
A.研发新型催化剂将CO,分解成碳和 ,同时放出大量热 ,同时放出大量热 |
| B.用于光学望远镜的高致密碳化硅特种陶瓷材料,是一种传统无机非金属材料 |
| C.大力发展新能源汽车,如混合动力汽车、电动汽车,可以减少碳、氮氧化物的排放 |
D.碲化镉(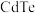 )薄膜太阳能电池将光能转化为化学能 )薄膜太阳能电池将光能转化为化学能 |
您最近一年使用:0次
解题方法
5 .  是一种剧毒气体,直接排放会造成严重的环境污染。某种利用硫化氢气体生产硫黄的工艺为
是一种剧毒气体,直接排放会造成严重的环境污染。某种利用硫化氢气体生产硫黄的工艺为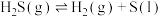 ,反应为放热反应。回答下列问题:
,反应为放热反应。回答下列问题:
(1)相同条件下,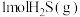 具有的能量
具有的能量_____ (填“>”“<”或“=”) 和
和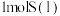 具有的总能量。
具有的总能量。
(2)在2L恒容密闭容器中充入 发生反应,20min时测得气体质量减少了16g。
发生反应,20min时测得气体质量减少了16g。
①前20min的平均反应速率
_____ 。20min时 的转化率为
的转化率为_____ 。
②下列说法不能说明反应已达平衡状态的是_____ (填字母,下同)。
A. B.
B.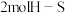 键断裂的同时生成
键断裂的同时生成 键
键
C.混合气体的密度不再变化 D.混合气体的平均摩尔质量不再变化
③下列措施可以加快该反应的化学反应速率的是_____ 。
A.恒温充入He B.降低温度 C.恒温充入 D.使用合适的催化剂
D.使用合适的催化剂
④下列曲线表示某物理量随时间的变化,其中错误的是_____ 。 中含有
中含有 杂质,反应过程中测得所得
杂质,反应过程中测得所得 的物质的是少于所得S的物质的量,同时检测到有水生成,可能的原因是
的物质的是少于所得S的物质的量,同时检测到有水生成,可能的原因是_____ 。
 是一种剧毒气体,直接排放会造成严重的环境污染。某种利用硫化氢气体生产硫黄的工艺为
是一种剧毒气体,直接排放会造成严重的环境污染。某种利用硫化氢气体生产硫黄的工艺为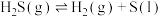 ,反应为放热反应。回答下列问题:
,反应为放热反应。回答下列问题:(1)相同条件下,
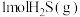 具有的能量
具有的能量 和
和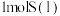 具有的总能量。
具有的总能量。(2)在2L恒容密闭容器中充入
 发生反应,20min时测得气体质量减少了16g。
发生反应,20min时测得气体质量减少了16g。①前20min的平均反应速率

 的转化率为
的转化率为②下列说法不能说明反应已达平衡状态的是
A.
 B.
B.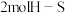 键断裂的同时生成
键断裂的同时生成 键
键C.混合气体的密度不再变化 D.混合气体的平均摩尔质量不再变化
③下列措施可以加快该反应的化学反应速率的是
A.恒温充入He B.降低温度 C.恒温充入
 D.使用合适的催化剂
D.使用合适的催化剂④下列曲线表示某物理量随时间的变化,其中错误的是
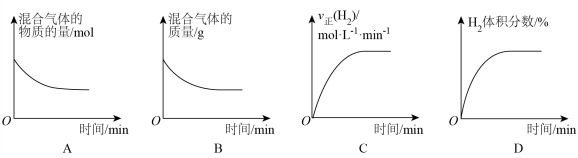
 中含有
中含有 杂质,反应过程中测得所得
杂质,反应过程中测得所得 的物质的是少于所得S的物质的量,同时检测到有水生成,可能的原因是
的物质的是少于所得S的物质的量,同时检测到有水生成,可能的原因是
您最近一年使用:0次
解题方法
6 . 我国在新能源汽车领域世界领先,新能源汽车动力电池的制备和回收利用技术至关重要。回答下列问题:
I.磷酸铁锂电池放电时电池反应为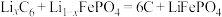 。
。
(1)磷酸铁锂电池正极的电极反应式为_____ 。
(2)将 、磷酸铁与足量炭黑混合高温灼烧可制备
、磷酸铁与足量炭黑混合高温灼烧可制备 ,同时生成一种有毒的气体。写出该反应的化学方程式:
,同时生成一种有毒的气体。写出该反应的化学方程式:_____ 。
Ⅱ.回收含的废旧电池制备 的流程如图所示(已知
的流程如图所示(已知 加热时可溶于盐酸):
加热时可溶于盐酸):_____ ,若要提高 的浸出速率和浸出率,可采取的措施是
的浸出速率和浸出率,可采取的措施是_____ (任写两点)。
(4)写出 与
与 在盐酸中发生反应的离子方程式:
在盐酸中发生反应的离子方程式:_____ 。
(5)欲证明 已沉淀完全,应采用的实验操作是
已沉淀完全,应采用的实验操作是_____ 。
(6)“操作a”所需玻璃仪器有_____ 。
I.磷酸铁锂电池放电时电池反应为
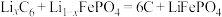 。
。(1)磷酸铁锂电池正极的电极反应式为
(2)将
 、磷酸铁与足量炭黑混合高温灼烧可制备
、磷酸铁与足量炭黑混合高温灼烧可制备 ,同时生成一种有毒的气体。写出该反应的化学方程式:
,同时生成一种有毒的气体。写出该反应的化学方程式:Ⅱ.回收含的废旧电池制备
 的流程如图所示(已知
的流程如图所示(已知 加热时可溶于盐酸):
加热时可溶于盐酸):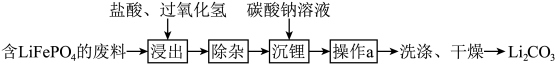
 的浸出速率和浸出率,可采取的措施是
的浸出速率和浸出率,可采取的措施是(4)写出
 与
与 在盐酸中发生反应的离子方程式:
在盐酸中发生反应的离子方程式:(5)欲证明
 已沉淀完全,应采用的实验操作是
已沉淀完全,应采用的实验操作是(6)“操作a”所需玻璃仪器有
您最近一年使用:0次
解题方法
7 . 在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法正确的是

A. 可以由 可以由 与 与 直接化合得到 直接化合得到 | B.催化剂可以改变汽车尾气净化速率 |
C. , , 均为酸性氧化物 均为酸性氧化物 | D.处理1molNO,总反应中共转移2mol电子 |
您最近一年使用:0次
名校
解题方法
8 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.46 g由NO2和N2O4组成的混合气体中,所含氧原子的数目为4NA |
B.1 L1 mol/L NH4NO3溶液中,所含 的总数小于NA 的总数小于NA |
| C.56 g Fe与一定量的浓硝酸恰好反应,转移的电子数一定为3NA |
| D.常温下,22.4 L氨气所含NH3的分子数为NA |
您最近一年使用:0次
名校
解题方法
9 . 中国的地热能开发和利用过程中,硫磺温泉常伴有H2S气体生成。H2S为无色、有臭鸡蛋气味的剧毒气体,H2S脱硫技术是当前的重点研究方向。
(1)20世纪30年代,德国法本公司将H2S的氧化分两阶段完成。
第一阶段反应为H2S(g)+ O2(g)=SO2(g)+H2O(g) ΔH=−518.9kJ·mol−1,
O2(g)=SO2(g)+H2O(g) ΔH=−518.9kJ·mol−1,
第二阶段反应为2H2S(g)+SO2(g)=2H2O(g)+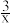 Sx(s) ΔH=−96.1kJ·mol−1。
Sx(s) ΔH=−96.1kJ·mol−1。
19世纪英国化学家Claus开发了H2S氧化制硫的方法,即:3H2S(g)+ O2(g)=
O2(g)=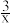 Sx(s)+3H2O(g),ΔH=
Sx(s)+3H2O(g),ΔH=_______ kJ·mol−1。
(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:ZnO(s)+H2S(g) ZnS(s)+H2O(g) ΔH=−76.63kJ·mol−1,文献显示,工业上氧化锌法控制温度在300~400℃,分析控制此温度区间的原因:温度过低
ZnS(s)+H2O(g) ΔH=−76.63kJ·mol−1,文献显示,工业上氧化锌法控制温度在300~400℃,分析控制此温度区间的原因:温度过低_______ ,温度过高_______ 。
(3)热解H2S制H2。根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(g) 2H2(g)+S2(g) ΔH1=+170kJ·mol−1
2H2(g)+S2(g) ΔH1=+170kJ·mol−1
Ⅱ.CH4(g)+S2(g) CS2(g)+2H2(g) ΔH2=+64kJ·mol−1
CS2(g)+2H2(g) ΔH2=+64kJ·mol−1
总反应:Ⅲ.2H2S(g)+CH4(g) CS2(g)+4H2(g)
CS2(g)+4H2(g)
投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释。
①反应Ⅱ能自发进行的条件是_______ (填“高温或低温”)。
②恒温恒压下,增加N2的体积分数,H2的物质的量_______ (填“增大,减小或不变”)。
③在TK、pkPa反应条件下,只充入H2S和Ar气体进行H2S热分解反应。已知反应一开始,c(H2S)∶c(Ar)=1∶3,平衡时混合气中H2S与H2的分压相等,则平衡常数Kp=_______ kPa。
(4)用CH4燃料电池连接成如图b装置。_______ 极,写出乙池总反应的离子方程式_______ 。
②当甲池中消耗标准状况下4.48LO2时,丙中a、b均为惰性电极,W为足量硝酸银溶液,停止电解后要加入_______ 克Ag2O才能复原。
(5)燃油汽车尾气中含有 和氮氧化物,氮氧化物包括
和氮氧化物,氮氧化物包括 等,研究
等,研究 还原氮氧化物及氮氧化物的分解对环境的治理有重要意义。已知:
还原氮氧化物及氮氧化物的分解对环境的治理有重要意义。已知:
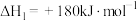 ,
, 的燃烧热为
的燃烧热为 。
。
写出 与
与 催化转化成
催化转化成 和
和 的热化学方程式
的热化学方程式_______ 。
(1)20世纪30年代,德国法本公司将H2S的氧化分两阶段完成。
第一阶段反应为H2S(g)+
 O2(g)=SO2(g)+H2O(g) ΔH=−518.9kJ·mol−1,
O2(g)=SO2(g)+H2O(g) ΔH=−518.9kJ·mol−1,第二阶段反应为2H2S(g)+SO2(g)=2H2O(g)+
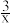 Sx(s) ΔH=−96.1kJ·mol−1。
Sx(s) ΔH=−96.1kJ·mol−1。19世纪英国化学家Claus开发了H2S氧化制硫的方法,即:3H2S(g)+
 O2(g)=
O2(g)=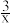 Sx(s)+3H2O(g),ΔH=
Sx(s)+3H2O(g),ΔH=(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:ZnO(s)+H2S(g)
 ZnS(s)+H2O(g) ΔH=−76.63kJ·mol−1,文献显示,工业上氧化锌法控制温度在300~400℃,分析控制此温度区间的原因:温度过低
ZnS(s)+H2O(g) ΔH=−76.63kJ·mol−1,文献显示,工业上氧化锌法控制温度在300~400℃,分析控制此温度区间的原因:温度过低(3)热解H2S制H2。根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(g)
 2H2(g)+S2(g) ΔH1=+170kJ·mol−1
2H2(g)+S2(g) ΔH1=+170kJ·mol−1Ⅱ.CH4(g)+S2(g)
 CS2(g)+2H2(g) ΔH2=+64kJ·mol−1
CS2(g)+2H2(g) ΔH2=+64kJ·mol−1总反应:Ⅲ.2H2S(g)+CH4(g)
 CS2(g)+4H2(g)
CS2(g)+4H2(g)投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释。
①反应Ⅱ能自发进行的条件是
②恒温恒压下,增加N2的体积分数,H2的物质的量
③在TK、pkPa反应条件下,只充入H2S和Ar气体进行H2S热分解反应。已知反应一开始,c(H2S)∶c(Ar)=1∶3,平衡时混合气中H2S与H2的分压相等,则平衡常数Kp=
(4)用CH4燃料电池连接成如图b装置。

②当甲池中消耗标准状况下4.48LO2时,丙中a、b均为惰性电极,W为足量硝酸银溶液,停止电解后要加入
(5)燃油汽车尾气中含有
 和氮氧化物,氮氧化物包括
和氮氧化物,氮氧化物包括 等,研究
等,研究 还原氮氧化物及氮氧化物的分解对环境的治理有重要意义。已知:
还原氮氧化物及氮氧化物的分解对环境的治理有重要意义。已知:
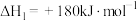 ,
, 的燃烧热为
的燃烧热为 。
。写出
 与
与 催化转化成
催化转化成 和
和 的热化学方程式
的热化学方程式
您最近一年使用:0次
10 . 按要求回答下列问题:
(1)已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO +H2O
+H2O H2SO3+OH- ①
H2SO3+OH- ①
HSO
 H++SO
H++SO ②
②
向0.1 mol·L-1的NaHSO3溶液中加入少量NaOH固体,则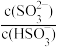
_______ (填“增大”“减小”或“不变”)。
(2)氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。
25 ℃时氯气—氯水体系中存在以下平衡关系:
Cl2(g) Cl2(aq) ①
Cl2(aq) ①
Cl2(aq) + H2O HClO + H+ + Cl- ②
HClO + H+ + Cl- ②
HClO H+ + ClO- ③
H+ + ClO- ③
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。_______ ,
由图可知该常数值为_______ 。
②用氯处理饮用水时,夏季的杀菌效果比冬季_______ (填“好”或“差”)。
(1)已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO
 +H2O
+H2O H2SO3+OH- ①
H2SO3+OH- ①HSO

 H++SO
H++SO ②
②向0.1 mol·L-1的NaHSO3溶液中加入少量NaOH固体,则
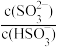
(2)氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。
25 ℃时氯气—氯水体系中存在以下平衡关系:
Cl2(g)
 Cl2(aq) ①
Cl2(aq) ①Cl2(aq) + H2O
 HClO + H+ + Cl- ②
HClO + H+ + Cl- ②HClO
 H+ + ClO- ③
H+ + ClO- ③其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
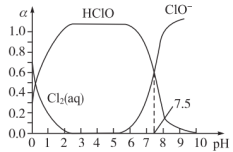
由图可知该常数值为
②用氯处理饮用水时,夏季的杀菌效果比冬季
您最近一年使用:0次



