名校
解题方法
1 . 氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:_______ (填“氧化剂”或“还原剂”)。
(2)写出氧化炉中反应的化学方程式_______ 。
(3)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其它条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 和
和 ,其离子方程式为
,其离子方程式为_______ 。
②NaClO溶液的初始pH越小,NO转化率越高,其原因是_______ 。
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是NH3催化还原氮氧化物(SCR)技术。反应原理如图所示:_______ 。
(5)某实验小组用足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.12LO2(标准状况)混合后通入水中,所得气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入2 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是_______ mL。

(2)写出氧化炉中反应的化学方程式
(3)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其它条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高,其原因是
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是NH3催化还原氮氧化物(SCR)技术。反应原理如图所示:

(5)某实验小组用足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.12LO2(标准状况)混合后通入水中,所得气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入2
 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
您最近一年使用:0次
2022-03-18更新
|
1009次组卷
|
7卷引用:湖南省名校联盟2021-2022学年高一下学期3月大联考化学试题
名校
2 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)钠有多种化合物,其中俗称“纯碱”的是___________ (填“Na2CO3”或“Na2SO4”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填“SiO2”或“Na2SiO3”)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式:2CO+2NO 2CO2 +
2CO2 +___________
(1)钠有多种化合物,其中俗称“纯碱”的是
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式:2CO+2NO
 2CO2 +
2CO2 +
您最近一年使用:0次
名校
3 . 完成下列问题。
(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:
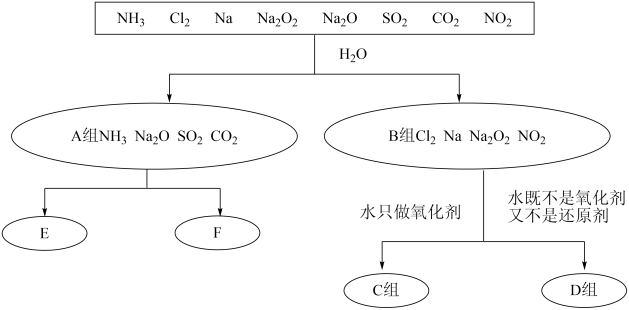
①上述分类中,分成A、B两组的依据是___________ ;
②C组物质与水反应的离子方程式为___________ ;
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有___________ 。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是___________ →___________ 。
②写出该反应的化学方程式,___________
③H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称,H2O2被称为绿色氧化剂的理由是_______
(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:

①上述分类中,分成A、B两组的依据是
②C组物质与水反应的离子方程式为
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是
②写出该反应的化学方程式,
③H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称,H2O2被称为绿色氧化剂的理由是
您最近一年使用:0次
4 . 请按要求回答下列问题:
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为___________ ;
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种___________ (填“酸性”、“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式___________ ;
(4)氨气极易溶于水,其水溶液显___________ (填“酸”、“碱”或“中”)性;
(5)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性;
(6)向试管中的品红溶液中通入一段时间的SO2,观察到品红溶液褪色,然后再加热试管,已褪色的溶液___________ (填“恢复”或“不恢复”)红色。
(7)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式___________ ;
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式
(4)氨气极易溶于水,其水溶液显
(5)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(6)向试管中的品红溶液中通入一段时间的SO2,观察到品红溶液褪色,然后再加热试管,已褪色的溶液
(7)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式
您最近一年使用:0次
2022-02-15更新
|
578次组卷
|
2卷引用:湖南省娄底市新化县2021-2022学年高一上学期期末考试化学试题
5 . Ⅰ.次磷酸( )常用于化学镀银,反应为:
)常用于化学镀银,反应为: 。请回答下列问题:
。请回答下列问题:
(1) 中,P元素的化合价为
中,P元素的化合价为___________ ;该反应中,氧化产物是___________ 。
(2)配平该离子方程式:___________ 。
(3) 是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:
是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:___________ 。
(4)若该反应消耗 ,则镀件镀上银的质量为
,则镀件镀上银的质量为___________ g。
Ⅱ.酸性高锰酸钾溶液常用于物质的定性检验与定量分析。现用酸性高锰酸钾溶液测定某补血剂中亚铁的含量:称取含的补血剂a克,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与cmol/L的酸性高锰酸钾溶液反应,消耗酸性高锰酸钾溶液25.00mL。上述过程发生反应的化学方程式为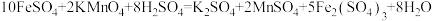 。
。
(5)该补血剂中 的质量分数为
的质量分数为___________ (用含a、c的代数式表示)。
 )常用于化学镀银,反应为:
)常用于化学镀银,反应为: 。请回答下列问题:
。请回答下列问题:(1)
 中,P元素的化合价为
中,P元素的化合价为(2)配平该离子方程式:
(3)
 是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:
是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:(4)若该反应消耗
 ,则镀件镀上银的质量为
,则镀件镀上银的质量为Ⅱ.酸性高锰酸钾溶液常用于物质的定性检验与定量分析。现用酸性高锰酸钾溶液测定某补血剂中亚铁的含量:称取含的补血剂a克,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与cmol/L的酸性高锰酸钾溶液反应,消耗酸性高锰酸钾溶液25.00mL。上述过程发生反应的化学方程式为
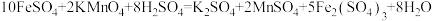 。
。(5)该补血剂中
 的质量分数为
的质量分数为
您最近一年使用:0次
6 . 按要求填空。
(1)下列物质中:①稀硫酸②液氯③熔融氯化钠④Fe⑤二氧化碳⑥乙醇⑦BaSO4,属于电解质的是______ (填序号,下同);能直接导电的是______ 。
(2)请写出下列反应的离子方程式。
①盐酸除去铁锈(主要成分为氧化铁)______ 。
②溴水与NaI溶液反应______ 。
③FeCl2溶液与新制氯水反应______ 。
(3)1.204×1024个H2SO4分子的质量为______ g,共含______ 个氢原子。
(4)工业废水中含有有毒的重铬酸根离子( ),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原
),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原 得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原
得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原 的离子方程式
的离子方程式______ 。
(1)下列物质中:①稀硫酸②液氯③熔融氯化钠④Fe⑤二氧化碳⑥乙醇⑦BaSO4,属于电解质的是
(2)请写出下列反应的离子方程式。
①盐酸除去铁锈(主要成分为氧化铁)
②溴水与NaI溶液反应
③FeCl2溶液与新制氯水反应
(3)1.204×1024个H2SO4分子的质量为
(4)工业废水中含有有毒的重铬酸根离子(
 ),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原
),必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)还原 得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原
得Cr3+和Fe3+,再通过沉淀处理法来处理该污水。写出该过程中Fe2+还原 的离子方程式
的离子方程式
您最近一年使用:0次
名校
7 . 电解法制取高纯镍的原料液中含Cu(II)(主要以Cu2+、CuCl+、CuCl2等形式存在)杂质,为保证高纯镍产品的纯度,电解前须将Cu(II)除去,方法如下。
(1)S−SO2除铜:向原料液中加入适量细硫粉并鼓入SO2,将Cu(II)转化为CuS沉淀除去。Cu2+沉淀时发生反应的离子方程式为___________ 。
(2)NiS除铜:向原料液中加入活性NiS粉末,将Cu(II)转化为CuS沉淀除去。过滤后的滤渣即为除铜渣(含NiS、CuS等)。
① 室温下,CuCl+和活性NiS粉末反应的离子方程式为___________ ;该反应的平衡常数表达式为K=___________ 。
② 如图−1所示,将活性NiS粉末陈化(露置)超过7小时后再用于除铜的效果明显变差,其原因可能是___________ 。

③ 除铜渣中铜镍质量比随原料液pH的变化如图−2所示,实验测得溶液pH=3.5时除铜渣中铜镍质量比最大,其原因可能是___________ 。
(1)S−SO2除铜:向原料液中加入适量细硫粉并鼓入SO2,将Cu(II)转化为CuS沉淀除去。Cu2+沉淀时发生反应的离子方程式为
(2)NiS除铜:向原料液中加入活性NiS粉末,将Cu(II)转化为CuS沉淀除去。过滤后的滤渣即为除铜渣(含NiS、CuS等)。
① 室温下,CuCl+和活性NiS粉末反应的离子方程式为
② 如图−1所示,将活性NiS粉末陈化(露置)超过7小时后再用于除铜的效果明显变差,其原因可能是

③ 除铜渣中铜镍质量比随原料液pH的变化如图−2所示,实验测得溶液pH=3.5时除铜渣中铜镍质量比最大,其原因可能是
您最近一年使用:0次
2022-01-11更新
|
873次组卷
|
4卷引用:湖南师范大学附属中学2022届高三月考(七)化学试题
湖南师范大学附属中学2022届高三月考(七)化学试题江苏省南京市、盐城市2021-2022学年高三第一次模拟考试化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(原理综合题)
名校
8 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是84消毒液,可以说化学让生活更美好。下图为84消毒液说明书。请回答下列问题。
(1)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25g·L-1计算,该消毒液的NaClO的物质的量浓度是___________ 。
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:___________ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为___________ ,从氧化还原角度分析Cl2表现了___________ 性。
(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)___________ (已知酸性:H2CO3>HClO>HCO )。
)。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会___________ (填“增强”或“减弱”)。
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g·L-1~60.00g·L-1 | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等1∶200水溶液 餐饮具、瓜果等1∶100水溶液 |
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)
 )。
)。(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
| A.增强漂白能力和消毒作用 |
| B.使它转化为较稳定物质,便于保存和运输 |
| C.使它转化为较易溶于水的物质 |
| D.提高氯的质量分数,有利于漂白、消毒 |
您最近一年使用:0次
2021-12-21更新
|
183次组卷
|
2卷引用:湖南省湘潭凤凰中学2021-2022学年高一上学期12月月考化学试题
9 . 高铁酸钠( )是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):
)是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):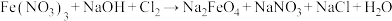
(1)高铁酸钠中,铁元素的化合价是___________
(2)上述反应中的还原产物为___________ ,配平并书写出上述方程式___________ 。
(3)高铁酸钠溶解于水,立即与水发生反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力可以用来给水杀菌消毒。根据氧化还原反应的基本规律判断其与水反应的过程中还会生成另外一种具有净水作用的胶体,该胶体是___________ 。
(4)次磷酸( )是一种化工产品,具有弱酸性,
)是一种化工产品,具有弱酸性, 的工业制法是:将白磷(P4)与
的工业制法是:将白磷(P4)与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应。配平白磷与
反应。配平白磷与 溶液反应的化学方程式(
溶液反应的化学方程式( )依次写出各物质的系数
)依次写出各物质的系数___________
(5)少量的次磷酸与足量的NaOH溶液反应能生成 ,根据上述信息写出次磷酸(
,根据上述信息写出次磷酸( )在水中的电离方程式
)在水中的电离方程式___________ ,从分类来看, 属于
属于___________ (书写弱酸电离方程式时需要用 连接弱酸与电离出来的离子)
连接弱酸与电离出来的离子)
a.酸式盐 B.碱 C.正盐 D.钠盐
 )是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):
)是经常使用的一种新型净水剂,它的氧化性很强。工业上制取高铁酸钠的化学方程式是(未配平):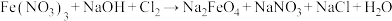
(1)高铁酸钠中,铁元素的化合价是
(2)上述反应中的还原产物为
(3)高铁酸钠溶解于水,立即与水发生反应,放出氧气,正是这些在水中新产生出的氧原子发挥其极强的氧化能力可以用来给水杀菌消毒。根据氧化还原反应的基本规律判断其与水反应的过程中还会生成另外一种具有净水作用的胶体,该胶体是
(4)次磷酸(
 )是一种化工产品,具有弱酸性,
)是一种化工产品,具有弱酸性, 的工业制法是:将白磷(P4)与
的工业制法是:将白磷(P4)与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应。配平白磷与
反应。配平白磷与 溶液反应的化学方程式(
溶液反应的化学方程式( )依次写出各物质的系数
)依次写出各物质的系数(5)少量的次磷酸与足量的NaOH溶液反应能生成
 ,根据上述信息写出次磷酸(
,根据上述信息写出次磷酸( )在水中的电离方程式
)在水中的电离方程式 属于
属于 连接弱酸与电离出来的离子)
连接弱酸与电离出来的离子)a.酸式盐 B.碱 C.正盐 D.钠盐
您最近一年使用:0次
名校
10 . 摩尔是将微观粒子和宏观物质联系起来的桥梁,回答以下问题
(1)同温同压下,同质量的 和
和 ,两者密度之比为
,两者密度之比为_______ ,氧原子数之比为_______ 。
(2)若 中含有0.4
中含有0.4 钠离子,
钠离子, 的摩尔质量是
的摩尔质量是_______ 。
(3)在相同的温度和压强下,A容器中 气体和B容器中
气体和B容器中 气体所含有的氢原子总数相等,则两个容器的体积比为
气体所含有的氢原子总数相等,则两个容器的体积比为_______ 。
(4)在一密闭容器中充入 和
和 ,可发生如下反应:
,可发生如下反应: ,充分反应后容器中氮原子和氧原子的个数之比为
,充分反应后容器中氮原子和氧原子的个数之比为_______ 。
(5)向100 的
的 溶液中通入标准状况下
溶液中通入标准状况下 ,反应后的溶液中
,反应后的溶液中 和
和 的物质的量浓度相等,则反应的离子方程式为
的物质的量浓度相等,则反应的离子方程式为_______ 。
(1)同温同压下,同质量的
 和
和 ,两者密度之比为
,两者密度之比为(2)若
 中含有0.4
中含有0.4 钠离子,
钠离子, 的摩尔质量是
的摩尔质量是(3)在相同的温度和压强下,A容器中
 气体和B容器中
气体和B容器中 气体所含有的氢原子总数相等,则两个容器的体积比为
气体所含有的氢原子总数相等,则两个容器的体积比为(4)在一密闭容器中充入
 和
和 ,可发生如下反应:
,可发生如下反应: ,充分反应后容器中氮原子和氧原子的个数之比为
,充分反应后容器中氮原子和氧原子的个数之比为(5)向100
 的
的 溶液中通入标准状况下
溶液中通入标准状况下 ,反应后的溶液中
,反应后的溶液中 和
和 的物质的量浓度相等,则反应的离子方程式为
的物质的量浓度相等,则反应的离子方程式为
您最近一年使用:0次



