名校
1 . 高铜酸钾是一种难溶于水的黑色粉末状固体,与高铁酸钾性质相似。可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①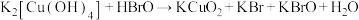 (未配平)。高铜酸钾在酸性条件下不稳定:②
(未配平)。高铜酸钾在酸性条件下不稳定:② (未配平)。下列说法不正确的是
(未配平)。下列说法不正确的是
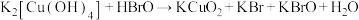 (未配平)。高铜酸钾在酸性条件下不稳定:②
(未配平)。高铜酸钾在酸性条件下不稳定:② (未配平)。下列说法不正确的是
(未配平)。下列说法不正确的是| A.①中氧化剂和还原剂的物质的量之比为1:2 |
B.②若有标况下5.6L 生成,转移电子 生成,转移电子 |
C.②中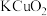 既表现氧化性,又表现还原性 既表现氧化性,又表现还原性 |
D.由①②可知氧化性强弱顺序为: |
您最近一年使用:0次
2022-06-07更新
|
965次组卷
|
6卷引用:山东省德州市2022届高考三模化学试题
山东省德州市2022届高考三模化学试题(已下线)1.3.2 氧化性、还原性强弱的判断(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)(已下线)第03讲 氧化还原反应(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题03 氧化还原反应-备战2023年高考化学母题题源解密(全国通用)江西省新余市第一中学2022-2023学年高三上学期新生入学考试化学试题宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题
解题方法
2 . 空间站中的物质循环利用是重要研究课题。关于如下“转化图”,说法正确的是


| A.Sabatier反应器中反应的氧化剂与还原剂物质的量之比为1∶4 |
| B.水电解系统的阳极产物应该输送进入Sabatier反应器 |
| C.采用高压和合适催化剂均有利于提高Sabatier反应器中的反应 |
| D.由图可知,该系统中H2O的循环利用率为100% |
您最近一年使用:0次
2022-05-27更新
|
284次组卷
|
4卷引用:山东省名校联盟2022届高三下学期5月模拟考试化学试题
山东省名校联盟2022届高三下学期5月模拟考试化学试题(已下线)第09练 以隔膜在电化学中的功能突破电解原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)1.3.1 氧化还原反应的基本概念(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)陕西省咸阳市2021-2022学年高二下学期期末考试化学试题
3 . 对 溶液氧化
溶液氧化 的反应,若加入
的反应,若加入 ,科研人员猜想其反应历程如下:
,科研人员猜想其反应历程如下:
Mn(VII)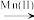 Mn(VI)
Mn(VI)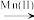 Mn(IV)
Mn(IV)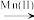 Mn(III)
Mn(III)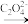 [Mn(C2O4)n]3-2n→Mn2++CO2
[Mn(C2O4)n]3-2n→Mn2++CO2
下列说法错误的是
 溶液氧化
溶液氧化 的反应,若加入
的反应,若加入 ,科研人员猜想其反应历程如下:
,科研人员猜想其反应历程如下:Mn(VII)
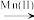 Mn(VI)
Mn(VI)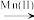 Mn(IV)
Mn(IV)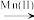 Mn(III)
Mn(III)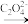 [Mn(C2O4)n]3-2n→Mn2++CO2
[Mn(C2O4)n]3-2n→Mn2++CO2下列说法错误的是
A.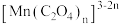 既有氧化性,又有还原性 既有氧化性,又有还原性 |
B.起始时加入 ,若反应产生气泡速率明显加快,可证明 ,若反应产生气泡速率明显加快,可证明 作催化剂 作催化剂 |
C.每生成标准状况下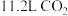 ,消耗 ,消耗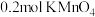 |
| D.加入某种试剂使Mn(Ⅵ)、Mn(Ⅳ)或Mn(Ⅲ)生成难溶物,若产生气泡速率减慢,则证明该猜想合理 |
您最近一年使用:0次
2022-05-20更新
|
306次组卷
|
2卷引用:山东省威海市2022届高三第二次模拟考试化学试题
4 . 钼系催化剂主要用于石油炼制和化学工业中。从废催化剂(主要成分为MoS、V2O5和Al2O3)中提取比较贵重的金属钒和钼,工艺流程如下:
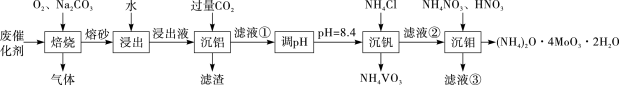
回答下列问题:
(1)“焙烧”时需对废催化剂进行粉碎,目的是_______ 。
(2)“焙烧”过程中MoS、V2O5和Al2O3均转化为对应的钠盐,写出MoS转化为Na2MoO4的化学方程式_______ 。
(3)“滤渣”的化学式为_______ 。滤液①的主要成分为Na2MoO4、_______ 。
(4)“沉钼”的离子方程式为_______ 。
(5)高温用 还原
还原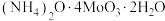 得金属钼,氧化剂与还原剂物质的量之比为
得金属钼,氧化剂与还原剂物质的量之比为_______ 。

回答下列问题:
(1)“焙烧”时需对废催化剂进行粉碎,目的是
(2)“焙烧”过程中MoS、V2O5和Al2O3均转化为对应的钠盐,写出MoS转化为Na2MoO4的化学方程式
(3)“滤渣”的化学式为
(4)“沉钼”的离子方程式为
(5)高温用
 还原
还原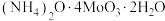 得金属钼,氧化剂与还原剂物质的量之比为
得金属钼,氧化剂与还原剂物质的量之比为
您最近一年使用:0次
2022-04-14更新
|
1667次组卷
|
4卷引用:山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题
山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题(已下线)微专题25 化学工艺流程题-----原料的预处理-备战2023年高考化学一轮复习考点微专题(已下线)微专题26 化学工艺流程题-----核心反应与条件控制-备战2023年高考化学一轮复习考点微专题辽宁省铁岭市六校协作体2022-2023学年高三上学期第一次联考化学试题
名校
5 . 溴乙烷是无色油状液体,是制造巴比妥的原料,工业上可用海水制备溴乙烷,部分工艺流程如图:

下列说法错误的是

下列说法错误的是
| A.粗盐提纯时,加入沉淀剂的顺序可以是BaCl2、NaOH和Na2CO3 |
| B.向“母液”中通入热空气,利用溴的易挥发性,将溴吹出 |
| C.“制备”时氧化剂和还原剂的物质的量之比为3:1 |
| D.“精制”时所用的玻璃仪器有分液漏斗、烧杯 |
您最近一年使用:0次
2022-03-22更新
|
1080次组卷
|
3卷引用:山东省济南市2022届高三3月高考模拟考试(一模)化学试题
山东省济南市2022届高三3月高考模拟考试(一模)化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题6-10)安徽省六安市第一中学2021-2022学年高一下学期期末考试化学试题
6 . 钼酸铵[(NH4)2MoO4]是生产高纯度钼制品、钼催化剂、钼颜料等的基本原料。一种以钼精矿(主要含MoS2,还含有少量SiO2、As、Sn、P、Cu、Pb、CaO)为原料制备钼酸铵的工艺流程如图所示:

已知:钼盐溶液中含钼物种之间的平衡关系为: 回答下列问题:
回答下列问题:
(1)(NH4)2MoO4中Mo元素的化合价为_______ 价。
(2)“氧化焙烧”时MoS2转化为MoO3,该反应中氧化剂与还原剂的物质的量之比为_______ ;气体A对环境的主要危害是_______ 。
(3)“除铜”时选择在60~80℃的条件下进行的原因为_______ 。
(4)“沉淀”过程中加入H2SO4调节溶液pH=2.1,则所得沉淀的化学式为_______ ,加入氨水后生成(NH4)2MoO4的化学方程式为_______ 。
(5)(NH4)6Mo7O24·4H2O的热重曲线如图所示:

已知A点失重的原因是生成H2O,则1 mol (NH4)6Mo7O24·4H2O在A点失去H2O的物质的量为_______ ,B点所得的物质为_______ (填化学式)。

已知:钼盐溶液中含钼物种之间的平衡关系为:
 回答下列问题:
回答下列问题:(1)(NH4)2MoO4中Mo元素的化合价为
(2)“氧化焙烧”时MoS2转化为MoO3,该反应中氧化剂与还原剂的物质的量之比为
(3)“除铜”时选择在60~80℃的条件下进行的原因为
(4)“沉淀”过程中加入H2SO4调节溶液pH=2.1,则所得沉淀的化学式为
(5)(NH4)6Mo7O24·4H2O的热重曲线如图所示:

已知A点失重的原因是生成H2O,则1 mol (NH4)6Mo7O24·4H2O在A点失去H2O的物质的量为
您最近一年使用:0次
2022-03-02更新
|
480次组卷
|
3卷引用:山东省菏泽市单县第二中学2022-2023学年高三下学期开学第一次模拟考试化学试题
山东省菏泽市单县第二中学2022-2023学年高三下学期开学第一次模拟考试化学试题广东省茂名市五校联盟2021-2022学年高三下学期第三次联考化学试卷(已下线)二轮专题强化练 大题突破3 无机化工流程题题型研究
解题方法
7 . 向 中加入足量硝酸,生成等量
中加入足量硝酸,生成等量 、
、 气体,其反应可表示为
气体,其反应可表示为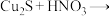
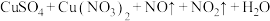 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 中加入足量硝酸,生成等量
中加入足量硝酸,生成等量 、
、 气体,其反应可表示为
气体,其反应可表示为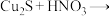
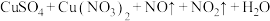 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是A. 晶体的熔点比 晶体的熔点比 晶体高 晶体高 |
B.消耗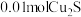 ,产生标准状况下 ,产生标准状况下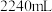 气体产物 气体产物 |
C.氧化剂和还原剂的物质的量之比为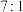 |
D.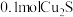 参与反应,产生的气体与一定量的 参与反应,产生的气体与一定量的 混合后通入水中完全反应生成硝酸,消耗 混合后通入水中完全反应生成硝酸,消耗 的质量为 的质量为 |
您最近一年使用:0次
名校
解题方法
8 . “价一类”二维图是研究物质性质的重要手段,下图是某常见元素的“价—类”二维图,已知Y中加入NaOH溶液,加热可生成X。据此回答下列问题:
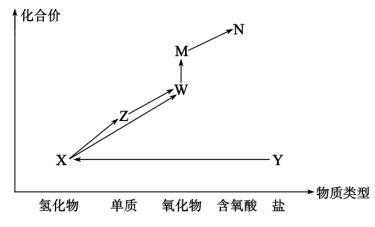
(1)实验室制取X的化学方程式为_______ ,其对应的制备装置为_______ 。
A.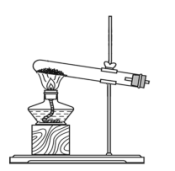 B.
B.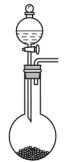 C.
C.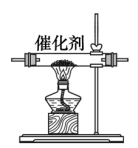
(2)下列试剂能用于干燥X的是___________。
(3)X→W反应中,氧化剂与还原剂的物质的量之比为___________ 。
(4)利用如图装置探究不同浓度的N溶液与金属反应的还原产物。
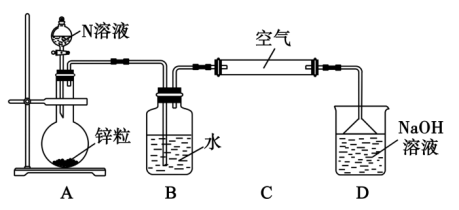
实验一:若N浓度为 时,其还原产物主要是M,则装置B中发生反应的化学方程式为
时,其还原产物主要是M,则装置B中发生反应的化学方程式为_____ 。
实验二:若N浓度为 时,其还原产物主要是W,则实验中能证明还原产物主要是W的现象是
时,其还原产物主要是W,则实验中能证明还原产物主要是W的现象是_______ 。
实验三:若N浓度为 时,过量锌粉与N反应产生H2,充分反应后所得溶液几乎无色。取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。则装置A中发生反应的离子方程式有:①
时,过量锌粉与N反应产生H2,充分反应后所得溶液几乎无色。取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。则装置A中发生反应的离子方程式有:①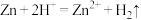 ;②
;②______ 。

(1)实验室制取X的化学方程式为
A.
 B.
B. C.
C.
(2)下列试剂能用于干燥X的是___________。
| A.无水氯化钙 | B.碱石灰 | C.氢氧化钠固体 | D.浓硫酸 |
(4)利用如图装置探究不同浓度的N溶液与金属反应的还原产物。

实验一:若N浓度为
 时,其还原产物主要是M,则装置B中发生反应的化学方程式为
时,其还原产物主要是M,则装置B中发生反应的化学方程式为实验二:若N浓度为
 时,其还原产物主要是W,则实验中能证明还原产物主要是W的现象是
时,其还原产物主要是W,则实验中能证明还原产物主要是W的现象是实验三:若N浓度为
 时,过量锌粉与N反应产生H2,充分反应后所得溶液几乎无色。取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。则装置A中发生反应的离子方程式有:①
时,过量锌粉与N反应产生H2,充分反应后所得溶液几乎无色。取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。则装置A中发生反应的离子方程式有:①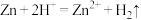 ;②
;②
您最近一年使用:0次
2022-02-20更新
|
587次组卷
|
3卷引用:山东省德州市2021-2022学年高一上学期期末考试化学试题
山东省德州市2021-2022学年高一上学期期末考试化学试题山东省枣庄滕州第第一中学2022-2023学年高一上学期期中(线上)考试化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
9 . 萨巴蒂尔反应可以将二氧化碳转化为甲烷和水,是氧气再生的一步重要反应,下图是氧气再生的流程图,下列说法错误的是


| A.富集二氧化碳可用碳酸钠的浓溶液 |
| B.装置I需要不断从外部补充水 |
| C.装置I是用铜作电极的电解装置 |
| D.萨巴蒂尔反应器中氧化剂和还原剂的物质的量之比为1:4 |
您最近一年使用:0次
解题方法
10 . 反应物相同,通过控制不同条件,可能得到不同的产物。某兴趣小组查阅资料发现: 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以 制备
制备 和
和 。已知:
。已知:

 。
。

回答下列问题:
(1)a中盛放浓盐酸的仪器名称为_______ ;若没有b装置,会导致c中产生大量的副产物_______ (填化学式)。
(2)a装置中发生反应的离子方程式为_______ 。
(3)资料显示:工业上制备“84”消毒液时,采用的是从吸收塔下部通入Cl2,从上部喷淋循环冷却的NaOH溶液(15~20%)。NaOH需要循环冷却的目的是_______ 。
(4)该兴趣小组在60℃条件下,将一定量的 通入600mL
通入600mL NaOH溶液中,NaOH恰好反应,得到产物中含有NaCl、NaClO和
NaOH溶液中,NaOH恰好反应,得到产物中含有NaCl、NaClO和 ,则参加反应
,则参加反应 的物质的量为
的物质的量为_______ mol。
 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以 制备
制备 和
和 。已知:
。已知:

 。
。
回答下列问题:
(1)a中盛放浓盐酸的仪器名称为
(2)a装置中发生反应的离子方程式为
(3)资料显示:工业上制备“84”消毒液时,采用的是从吸收塔下部通入Cl2,从上部喷淋循环冷却的NaOH溶液(15~20%)。NaOH需要循环冷却的目的是
(4)该兴趣小组在60℃条件下,将一定量的
 通入600mL
通入600mL NaOH溶液中,NaOH恰好反应,得到产物中含有NaCl、NaClO和
NaOH溶液中,NaOH恰好反应,得到产物中含有NaCl、NaClO和 ,则参加反应
,则参加反应 的物质的量为
的物质的量为
您最近一年使用:0次



