1 . 一水硫酸四氨合铜[Cu(NH3)4SO4·H2O]是一种易溶于水,难溶于乙醇的绛蓝色晶体,可作高效安全的广谱杀菌剂。成外某兴趣小组查阅资料后设计实验方案制备出该晶体并对制备出的晶体进行成分检验和性质探究。
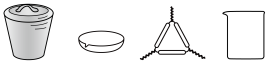
I.制备少量Cu(NH3)4SO4·H2O晶体:___________ (填仪器名称)。___________ 。
(3)步骤Ⅲ的离子方程式为___________ 。
(4)有同学查阅资料得知:(NH4)2SO4也难溶于乙醇。故对于制备出的晶体的成分,该同学提出如下假设:
假设一:只有(NH4)2SO4
假设二:只有Cu(NH3)4SO4·H2O
假设三:(NH4)2SO4和Cu(NH3)4SO4·H2O两种成分都有
已知产物晶体为蓝色,则无需实验即可排除___________ 。(填“假设一”、“假设二”、“假设三”)
Ⅱ.对制备出的晶体的成分进行检验和性质探究
(5)检验该晶体中阴离子的方法:___________ 。
(6)用所得晶体加水得到深蓝色溶液。取三份1L试样,分别加入一定量的水、稀硫酸、热的浓氢氧化钠溶液,实验现象记录如下:
结合化学用语,解释加入稀硫酸后出现的现象的原因___________ 。请补充完整加入热的浓氢氧化钠溶液后的现象:___________ 。
(7)晶体中N含量的测定
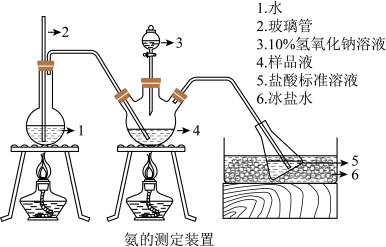
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,并用蒸馏水冲洗导管内壁,用V1mLc1mol/L的盐酸标准溶液完全吸收。取下接收瓶,用c2mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL溶液。___________ ,样品中N的质量分数的表达式为___________ ,最终通过N的质量分数确定了样品的成分。
I.制备少量Cu(NH3)4SO4·H2O晶体:
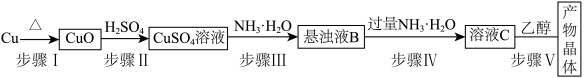
(3)步骤Ⅲ的离子方程式为
(4)有同学查阅资料得知:(NH4)2SO4也难溶于乙醇。故对于制备出的晶体的成分,该同学提出如下假设:
假设一:只有(NH4)2SO4
假设二:只有Cu(NH3)4SO4·H2O
假设三:(NH4)2SO4和Cu(NH3)4SO4·H2O两种成分都有
已知产物晶体为蓝色,则无需实验即可排除
Ⅱ.对制备出的晶体的成分进行检验和性质探究
(5)检验该晶体中阴离子的方法:
(6)用所得晶体加水得到深蓝色溶液。取三份1L试样,分别加入一定量的水、稀硫酸、热的浓氢氧化钠溶液,实验现象记录如下:
| 加入试剂 | 水 | 稀硫酸 | 热的氢氧化钠溶液 |
| 现象 | 深蓝色稍变浅 | 溶液颜色变成浅蓝色且与同浓度硫酸铜颜色相当 | 溶液最终变为无色 |
(7)晶体中N含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,并用蒸馏水冲洗导管内壁,用V1mLc1mol/L的盐酸标准溶液完全吸收。取下接收瓶,用c2mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL溶液。
您最近半年使用:0次
2 . 碱式碳酸铜 俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
Ⅰ.配制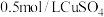 溶液和
溶液和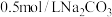 溶液各
溶液各 。
。
Ⅱ.取 所配
所配 溶液,按照
溶液,按照 和
和 的物质的量之比
的物质的量之比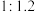 进行混合,在
进行混合,在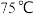 下搅拌反应产生蓝绿色沉淀。
下搅拌反应产生蓝绿色沉淀。
Ⅲ.待沉淀完全后减压过滤,用乙醇淋洗,干燥。
回答下列问题:
(1)步骤Ⅰ中,配制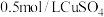 溶液时,不需要使用下列仪器中的
溶液时,不需要使用下列仪器中的___________ (填仪器名称)。___________ ,步骤Ⅲ中检验沉淀是否洗净的操作为___________ 。
(3)步骤Ⅲ中用乙醇淋洗的原因是___________ 。
Ⅳ.碱式碳酸铜纯度的测定:同学们设计了如图装置对制得的 蓝绿色固体进行实验。
蓝绿色固体进行实验。 装置加热前,需要首先打开活塞
装置加热前,需要首先打开活塞 ,用
,用 装置制取适量
装置制取适量 ,然后关闭
,然后关闭 ,点燃
,点燃 处酒精灯。装置A中发生反应的离子程式为
处酒精灯。装置A中发生反应的离子程式为___________ ,C中盛装的试剂应是___________ 。
(5)装置 的作用为
的作用为___________ 。
(6)待固体完全分解后,测得装置E增重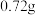 ,则该碱式碳酸铜的纯度为
,则该碱式碳酸铜的纯度为___________  (保留1位小数)。
(保留1位小数)。
 俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:Ⅰ.配制
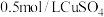 溶液和
溶液和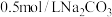 溶液各
溶液各 。
。Ⅱ.取
 所配
所配 溶液,按照
溶液,按照 和
和 的物质的量之比
的物质的量之比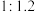 进行混合,在
进行混合,在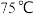 下搅拌反应产生蓝绿色沉淀。
下搅拌反应产生蓝绿色沉淀。Ⅲ.待沉淀完全后减压过滤,用乙醇淋洗,干燥。
回答下列问题:
(1)步骤Ⅰ中,配制
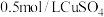 溶液时,不需要使用下列仪器中的
溶液时,不需要使用下列仪器中的
(3)步骤Ⅲ中用乙醇淋洗的原因是
Ⅳ.碱式碳酸铜纯度的测定:同学们设计了如图装置对制得的
 蓝绿色固体进行实验。
蓝绿色固体进行实验。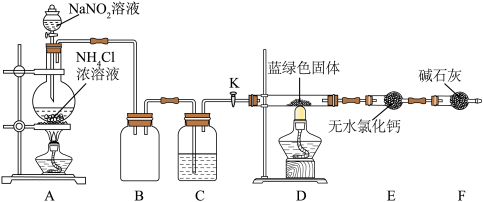
 装置加热前,需要首先打开活塞
装置加热前,需要首先打开活塞 ,用
,用 装置制取适量
装置制取适量 ,然后关闭
,然后关闭 ,点燃
,点燃 处酒精灯。装置A中发生反应的离子程式为
处酒精灯。装置A中发生反应的离子程式为(5)装置
 的作用为
的作用为(6)待固体完全分解后,测得装置E增重
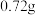 ,则该碱式碳酸铜的纯度为
,则该碱式碳酸铜的纯度为 (保留1位小数)。
(保留1位小数)。
您最近半年使用:0次
3 . 某工厂的固体废渣中主要含 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
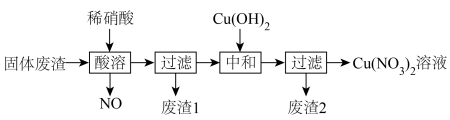
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知: 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。___________ 写出 与稀硝酸反应的离子反应方程式
与稀硝酸反应的离子反应方程式___________ 。
(2)酸溶时,反应温度不宜超过 ,其主要原因是
,其主要原因是___________ 。
(3)废渣1主要成分为___________ 。
(4)酸溶时产生的NO在一定条件下可以用氨气转化为对环境无害的物质,该反应中氧化剂和还原剂的物质的量之比为___________ 。
 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:已知:
 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。
 与稀硝酸反应的离子反应方程式
与稀硝酸反应的离子反应方程式(2)酸溶时,反应温度不宜超过
 ,其主要原因是
,其主要原因是(3)废渣1主要成分为
(4)酸溶时产生的NO在一定条件下可以用氨气转化为对环境无害的物质,该反应中氧化剂和还原剂的物质的量之比为
您最近半年使用:0次
4 . 中国三星堆出土了大量文物,如青铜面具、青铜大立人等。下列有关说法正确的是
| A.铜在空气中主要发生析氢腐蚀 |
| B.三星堆出土的青铜器上有大量铜锈,其主要成分为Cu2(OH)2CO3 |
| C.用硝酸清洗铜器可以除去铜锈,保护铜器 |
| D.青铜是铜中加入铅、锡制得的合金,其成分会加快铜的腐蚀 |
您最近半年使用:0次
名校
5 . 在中华文明的历史长河中,江西人才辈出,文化璀璨,下列说法正确的是
| A.“落木千山天远大,澄江一道月分明”,月亮倒映在江水中的现象属于丁达尔效应 |
B.白鹿洞书院建筑群易受酸雨腐蚀, 的雨水为酸雨 的雨水为酸雨 |
C.“庐山山南刷铜绿”,“铜绿”的主要成分为 |
| D.“白如玉,明如镜,薄如纸,声如馨”的景德镇白瓷的主要成分为无机硅酸盐材料 |
您最近半年使用:0次
名校
6 . 下列物质对应的化学式不正确的是
| A.干冰:CO2 | B.金刚砂:SiC |
| C.胆矾:CuSO4·5H2O | D.重晶石:CaSO4 |
您最近半年使用:0次
名校
7 . 硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主要成分为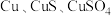 等,制备流程如图所示:
等,制备流程如图所示:
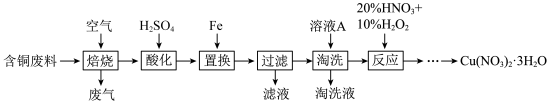
回答下列问题:
(1)焙烧时, 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“淘洗”所用的溶液A可以是___________ 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。
①理论上反应所消耗的 和
和 的物质的量之比为
的物质的量之比为___________ 。
②若不加10%的 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为___________ 。
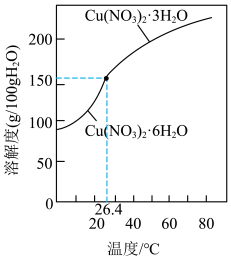
③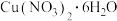 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是___________ 。
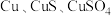 等,制备流程如图所示:
等,制备流程如图所示:
回答下列问题:
(1)焙烧时,
 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)“淘洗”所用的溶液A可以是
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的
 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。①理论上反应所消耗的
 和
和 的物质的量之比为
的物质的量之比为②若不加10%的
 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为③
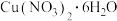 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是
您最近半年使用:0次
解题方法
8 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近半年使用:0次
9 . 红珊瑚栖息于200~2000米深的海域,它与琥珀、珍珠统称为有机宝石,红珊瑚是由无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,呈红色是因为在海底长期积淀某种元素的氧化物。该元素可能是
| A.Na | B.Fe | C.Si | D.Cu |
您最近半年使用:0次
解题方法
10 . 下列反应的离子方程式书写正确的是
A.碳酸钙与稀盐酸反应: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| B.金属钠加入硫酸铜溶液的反应中:2Na+CuSO4=Na2SO4+Cu |
| C.铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
| D.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
您最近半年使用:0次



