1 . 回答下列问题。
(1)如图是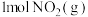 和
和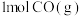 反应生成
反应生成 和
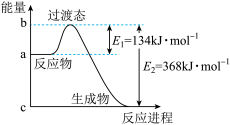
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式__________ 。
(2)用如图所示装置进行中和热的测定实验。
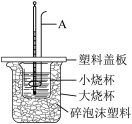
①仪器A的名称是__________ ,碎泡沫塑料的作用是__________ 。
②若实验过程中,未加塑料盖板,则实验测出的
__________ (填“偏大”或“偏小”或“无影响”)。
③理论上强酸强碱的中和热为 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式__________ 。
(3)甲醇是人们开发和利用的一种新能源。已知:


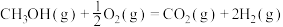
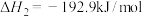
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为__________ ;
② 的燃烧热为
的燃烧热为__________ 。
(1)如图是
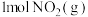 和
和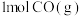 反应生成
反应生成 和
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式
(2)用如图所示装置进行中和热的测定实验。

①仪器A的名称是
②若实验过程中,未加塑料盖板,则实验测出的

③理论上强酸强碱的中和热为
 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式(3)甲醇是人们开发和利用的一种新能源。已知:


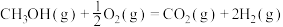
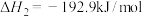
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为
②
 的燃烧热为
的燃烧热为
您最近半年使用:0次
2 . 下列说法正确的是
| A.锂电池使用时,能量只存在由化学能到电能的转化 |
| B.已知P4(白磷,s)=4P(红磷,s) ΔH=-18.4kJ·mol-1,故白磷比红磷稳定 |
| C.H2在Cl2中燃烧:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1,则H2的燃烧热ΔH=-184.6kJ·mol-1 |
| D.测定中和反应的反应热时,其他不变,用稀硫酸代替盐酸测得的反应热ΔH基本相同 |
您最近半年使用:0次
名校
3 . 能源是人类生存和发展的重要支柱。研究和有效地开发新能源有重要意义。已知CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的燃烧过程如图所示:

已知:H2O(g)=H2O(l) ΔH=-41kJ·mol-1.请根据以上信息,回答下列有关问题:
(1)图形中E表示CH3CH2CH2CH3(g)燃烧反应逆反应的___________ 。
(2)CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的热稳定性___________ 更高。
(3)表示CH3CH(CH3)CH3(g)燃烧热的热化学方程式为___________ 。
(4)CH3CH2CH2CH3(g)转化为CH3CH(CH3)CH3(g)的热化学反应方程式为___________ 。
(5)如表所示是部分化学键的键能参数:
合成气(CO和H2的混合气体)可以合成CH3CH2CH2CH3(g),同时生成H2O(g),则合成1molCH3CH2CH2CH3(g)的ΔH=___________ 。
(6)标准状况,CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的混合气体11.2L,充分燃烧后,生成H2O(g)和CO2(g),共放出1333.8kJ热量,则混合气体中CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的物质的量之比为___________ 。

已知:H2O(g)=H2O(l) ΔH=-41kJ·mol-1.请根据以上信息,回答下列有关问题:
(1)图形中E表示CH3CH2CH2CH3(g)燃烧反应逆反应的
(2)CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的热稳定性
(3)表示CH3CH(CH3)CH3(g)燃烧热的热化学方程式为
(4)CH3CH2CH2CH3(g)转化为CH3CH(CH3)CH3(g)的热化学反应方程式为
(5)如表所示是部分化学键的键能参数:
| 化学键 | C≡O | C—H | H—H | C—C | H—O |
| 键能/(kJ·mol-1) | a | b | d | e | f |
(6)标准状况,CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的混合气体11.2L,充分燃烧后,生成H2O(g)和CO2(g),共放出1333.8kJ热量,则混合气体中CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的物质的量之比为
您最近半年使用:0次
名校
4 . 依据如下反应可知某纯物质的燃烧热的是(燃烧热数值正确)
A.2C(s)+O2(g)=2CO(g)  =﹣221kJ•mol-1 =﹣221kJ•mol-1 |
B.CH4(g)+2O2(g)=2CO2(g)+2H2O(g)  =﹣890.3kJ•mol-1 =﹣890.3kJ•mol-1 |
C.4NH3(g)+3O2(g)=2N2(g)+6H2O(l)  =﹣1265.2kJ•mol-1 =﹣1265.2kJ•mol-1 |
D.2H2S(g)+O2(g)=2H2O(l)+2S(s)  =-632kJ•mol-1 =-632kJ•mol-1 |
您最近半年使用:0次
名校
解题方法
5 . 根据如下能量关系示意图,下列说法正确的是
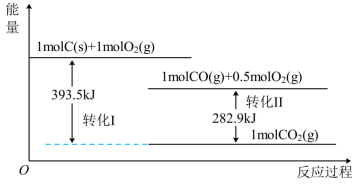
A.1mol 与1mol 与1mol  的能量之和为393.5kJ 的能量之和为393.5kJ |
| B.CO比CO2的能量高 |
C.C的燃烧热的热化学方程式为:C(s)+ O2(g)=CO(g) △H=110.6kJ·mol-1 O2(g)=CO(g) △H=110.6kJ·mol-1 |
D.CO气体燃烧的热化学方程式为: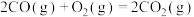  |
您最近半年使用:0次
2024-03-29更新
|
187次组卷
|
2卷引用:浙江省湖州市第二中学2023-2024学年高一下学期3月月考化学试卷
名校
解题方法
6 . 有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
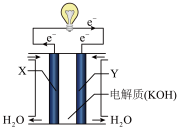
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近半年使用:0次
名校
解题方法
7 . 下列关于热化学反应的描述中正确的是
| A.在25℃、101 kPa、1 mol CH4(g)和2 molCH4(g)的燃烧热相等 |
| B.1 mol浓硫酸与1 mol NaOH溶液完全中和所放出的热量为中和热 |
C.已知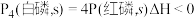 ,则白磷比红磷稳定 ,则白磷比红磷稳定 |
| D.△H越大,说明反应热量变化越大 |
您最近半年使用:0次
解题方法
8 . 下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
B.由 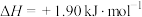 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
C.在101 kPa时,2 g  完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气摩尔燃烧焓的热化学方程式为 完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气摩尔燃烧焓的热化学方程式为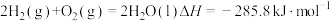 |
D.在稀溶液中, ,若将含0.5 mol ,若将含0.5 mol 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
您最近半年使用:0次
2024-03-26更新
|
148次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
解题方法
9 . 俄乌冲突爆发以来,许多西方国家宣布制裁俄罗斯,但俄罗斯的石油和天然气目前并不在制裁之列。天然气的主要成分是甲烷,已知甲烷的燃烧热为889.6kJ·mol-1,下列能正确表示甲烷燃烧热的热化学方程式是
A.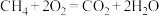 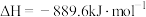 |
B. 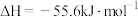 |
C. 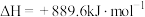 |
D. 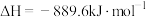 |
您最近半年使用:0次
10 . 能由下表所列的“依据”推导出后面的“结论”的是
| 依据 | 结论 | |
| A | 稀溶液中: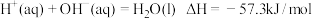 | 中和热为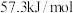 |
| B | C(s,石墨) C(s,金刚石) 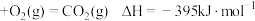 | 石墨转化为金刚石的过程中会放出热量 |
| C |  时, 时, ; ; | 非金属性: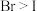 |
| D |  |  的燃烧热为 的燃烧热为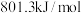 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



