解题方法
1 . 硫酸亚铁在工农业生产中有许多用途,如可用作农药,防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题。
(1)在 气氛中,
气氛中, (
( )的脱水热分解情况如表所示:
)的脱水热分解情况如表所示:
根据上述实验结果,可知
_______ 。
(2)已知下列热化学方程式:

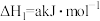

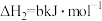


则 的
的
_______  。
。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: 。平衡时
。平衡时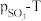 的关系如图所示。720K时,该反应的平衡总压
的关系如图所示。720K时,该反应的平衡总压
_______ kPa,平衡常数
_______ 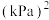 。
。 随反应温度升高而
随反应温度升高而_______ (填“增大”“减小”或“不变”)。

(4)提高温度,上述容器中进一步发生反应: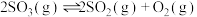 (Ⅱ),平衡时
(Ⅱ),平衡时
_______ (用 、
、 表示)。在929K时,
表示)。在929K时, ,
, ,则
,则
_______ kPa。
(1)在
 气氛中,
气氛中, (
( )的脱水热分解情况如表所示:
)的脱水热分解情况如表所示:| 加热温度/℃ | 失重比/% | 物质组成 |
| 100 | 19.4 |  |
| 200 | 38.8 |  |
| 300 | 45.3 |  |

(2)已知下列热化学方程式:

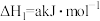

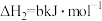


则
 的
的
 。
。(3)将
 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: 。平衡时
。平衡时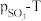 的关系如图所示。720K时,该反应的平衡总压
的关系如图所示。720K时,该反应的平衡总压

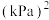 。
。 随反应温度升高而
随反应温度升高而
(4)提高温度,上述容器中进一步发生反应:
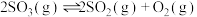 (Ⅱ),平衡时
(Ⅱ),平衡时
 、
、 表示)。在929K时,
表示)。在929K时, ,
, ,则
,则
您最近一年使用:0次
名校
解题方法
2 . CO2在自然界碳循环中起着重要作用,合理利用CO2是当今科学研究的前沿。
(1)蓝色碳汇技术:利用海洋生物吸收大气中的CO2,将其固定在海洋中。

①海水的CO295%以 形式存在,写出CO2溶于水产生
形式存在,写出CO2溶于水产生 的方程式
的方程式__________ 。
②珊瑚虫是海洋中的一种腔肠动物,经钙化作用可以形成石灰石外壳,示意图如上。写出钙化作用的离子方程式____________________ 。
(2)用CO2生产绿色燃料甲醇:
①用CO2生产绿色燃料甲醇时发生反应A:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
已知:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H=-1365.0kJ/mol
H2(g)+ O2(g)=H2O(g) △H=-241.8kJ/mol
O2(g)=H2O(g) △H=-241.8kJ/mol
则反应A的热化学方程式为___________________________ 。
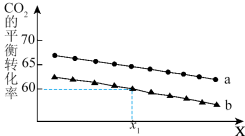
②在体积为1L的恒容密闭容器中发生反应A,下图为不同投料[n(CO2)和n(H2)分别为1mol,3mol;lmol,6mol]下,CO2平衡转化率随X(温度或压强)的变化曲线。
Ⅰ.曲线a对应的投料是___________ 。
Ⅱ.判断X代表的物理量是______ ,简述理由____________________ 。
Ⅲ.x1时,曲线b对应的化学平衡常数是______________ 。
Ⅳ.将CO2和H2按物质的量比1:3混合,以固定流速通过盛放Cu/Zn/Al/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如下图所示。
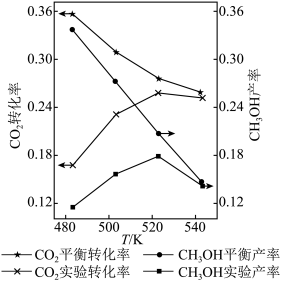
已知:CH3OH产率=
ⅰ.催化剂活性最好的温度为___ (填字母序号)。
a.483K b.503K c.523K d.543K
ⅱ.温度由523K升到543K,CO2的平衡转化率和CH3OH的实验产率均降低,解释原因:____________ 。
(1)蓝色碳汇技术:利用海洋生物吸收大气中的CO2,将其固定在海洋中。

①海水的CO295%以
 形式存在,写出CO2溶于水产生
形式存在,写出CO2溶于水产生 的方程式
的方程式②珊瑚虫是海洋中的一种腔肠动物,经钙化作用可以形成石灰石外壳,示意图如上。写出钙化作用的离子方程式
(2)用CO2生产绿色燃料甲醇:
①用CO2生产绿色燃料甲醇时发生反应A:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)已知:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) △H=-1365.0kJ/mol
H2(g)+
 O2(g)=H2O(g) △H=-241.8kJ/mol
O2(g)=H2O(g) △H=-241.8kJ/mol则反应A的热化学方程式为
②在体积为1L的恒容密闭容器中发生反应A,下图为不同投料[n(CO2)和n(H2)分别为1mol,3mol;lmol,6mol]下,CO2平衡转化率随X(温度或压强)的变化曲线。
Ⅰ.曲线a对应的投料是
Ⅱ.判断X代表的物理量是
Ⅲ.x1时,曲线b对应的化学平衡常数是

Ⅳ.将CO2和H2按物质的量比1:3混合,以固定流速通过盛放Cu/Zn/Al/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如下图所示。

已知:CH3OH产率=

ⅰ.催化剂活性最好的温度为
a.483K b.503K c.523K d.543K
ⅱ.温度由523K升到543K,CO2的平衡转化率和CH3OH的实验产率均降低,解释原因:
您最近一年使用:0次
名校
解题方法
3 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。资源化利用碳氧化合物能有效减少 排放,实现自然界中的碳循环。
排放,实现自然界中的碳循环。
(1) 的捕获是实现资源利用的重要途径。烟气中
的捕获是实现资源利用的重要途径。烟气中 的捕集可通过如下所示的物质转化实现。
的捕集可通过如下所示的物质转化实现。
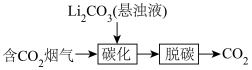
“碳化”的温度不能过高的原因是___________ 。
(2)以 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
Ⅰ.
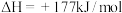 (主反应)
(主反应)
Ⅱ.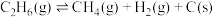
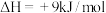 (副反应)
(副反应)
反应Ⅰ的反应历程可分为如下两步:
ⅰ.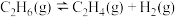

ⅱ.

①
___________ 。
②相比于提高 ,提高
,提高 对反应Ⅰ速率影响更大,原因是
对反应Ⅰ速率影响更大,原因是___________ 。
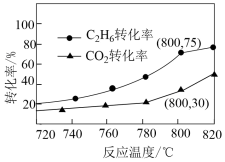
③ 时,向一恒容密闭容器中充入物质的量之比为2∶1的
时,向一恒容密闭容器中充入物质的量之比为2∶1的 和
和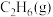 ,反应物转化率与反应温度的关系如图所示。在
,反应物转化率与反应温度的关系如图所示。在 下
下 的选择性
的选择性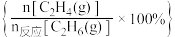 为
为________ 。
(3) 可制甲烷化,
可制甲烷化, 可制甲烷化过程中,
可制甲烷化过程中, 活化的可能途径如图所示。
活化的可能途径如图所示。 是
是 活化的优势中间体,可能的原因是
活化的优势中间体,可能的原因是___________ 。

(4) 和
和 催化合成
催化合成 。主要发生反应为
。主要发生反应为
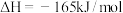 ,一定温度和压强下,将一定比例
,一定温度和压强下,将一定比例 和
和 分别通过装有两种不同。催化剂的反应器,反应相同时间,测得
分别通过装有两种不同。催化剂的反应器,反应相同时间,测得 转化率随温度变化情况下如图所示。
转化率随温度变化情况下如图所示。
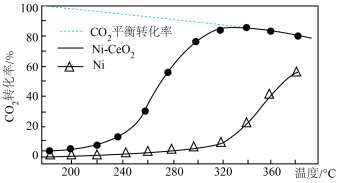
①高于 后,用
后,用 作催化剂,
作催化剂, 转化率明显上升,其可能原因是
转化率明显上升,其可能原因是___________
②高于 后,用
后,用 作催化剂,
作催化剂, 转化率略有下降,可能原因是
转化率略有下降,可能原因是___________ 。
 排放,实现自然界中的碳循环。
排放,实现自然界中的碳循环。(1)
 的捕获是实现资源利用的重要途径。烟气中
的捕获是实现资源利用的重要途径。烟气中 的捕集可通过如下所示的物质转化实现。
的捕集可通过如下所示的物质转化实现。
“碳化”的温度不能过高的原因是
(2)以
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:Ⅰ.

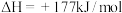 (主反应)
(主反应)Ⅱ.
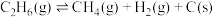
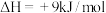 (副反应)
(副反应)反应Ⅰ的反应历程可分为如下两步:
ⅰ.
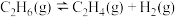

ⅱ.


①

②相比于提高
 ,提高
,提高 对反应Ⅰ速率影响更大,原因是
对反应Ⅰ速率影响更大,原因是③
 时,向一恒容密闭容器中充入物质的量之比为2∶1的
时,向一恒容密闭容器中充入物质的量之比为2∶1的 和
和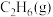 ,反应物转化率与反应温度的关系如图所示。在
,反应物转化率与反应温度的关系如图所示。在 下
下 的选择性
的选择性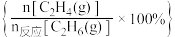 为
为
(3)
 可制甲烷化,
可制甲烷化, 可制甲烷化过程中,
可制甲烷化过程中, 活化的可能途径如图所示。
活化的可能途径如图所示。 是
是 活化的优势中间体,可能的原因是
活化的优势中间体,可能的原因是
(4)
 和
和 催化合成
催化合成 。主要发生反应为
。主要发生反应为
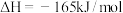 ,一定温度和压强下,将一定比例
,一定温度和压强下,将一定比例 和
和 分别通过装有两种不同。催化剂的反应器,反应相同时间,测得
分别通过装有两种不同。催化剂的反应器,反应相同时间,测得 转化率随温度变化情况下如图所示。
转化率随温度变化情况下如图所示。
①高于
 后,用
后,用 作催化剂,
作催化剂, 转化率明显上升,其可能原因是
转化率明显上升,其可能原因是②高于
 后,用
后,用 作催化剂,
作催化剂, 转化率略有下降,可能原因是
转化率略有下降,可能原因是
您最近一年使用:0次
4 . 烟道气中含 、
、 、
、 等多种有害气体,合理治理烟道气中具有重要意义。
等多种有害气体,合理治理烟道气中具有重要意义。
Ⅰ.烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:


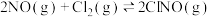

(1)则反应: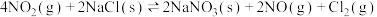

___________ (用含 、
、 的式子表示)。
的式子表示)。
Ⅱ.利用 可将
可将 转化为无害的
转化为无害的 ,其反应为:
,其反应为: 。在容积均为
。在容积均为 的甲、乙两个恒温(反应温度分别为℃、
的甲、乙两个恒温(反应温度分别为℃、 ℃)恒容密闭容器中,分别加入物质的量之比为
℃)恒容密闭容器中,分别加入物质的量之比为 的
的 和
和 ,测得各容器中
,测得各容器中 随反应时间
随反应时间 的变化情况如下表所示:
的变化情况如下表所示:
(2)
___________  ,该反应的
,该反应的
___________ 0。(填“>”或“<”)
(3) 时,该反应的平衡常数为
时,该反应的平衡常数为___________ ;若再加入 和
和 ,平衡向
,平衡向___________ (填“正反应方向”、“逆反应方向”或“不”)移动。
Ⅲ.对烟道气中的进行回收再利用具有较高的社会价值和经济价值,涉及到的主要反应是: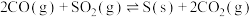
 。
。
(4)向三个体积相同的恒容密闭容器中通入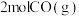 和
和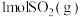 发生反应,反应体系的总压强随时间的变化如图所示。
发生反应,反应体系的总压强随时间的变化如图所示。
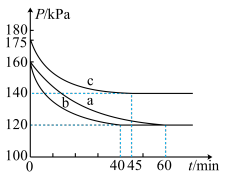
①实验 中,
中, 内
内 的平均反应速率为
的平均反应速率为___________  。
。
②与实验 相比,实验
相比,实验 改变的条件可能是
改变的条件可能是___________ 。
③实验 中
中 的平衡转化率为
的平衡转化率为___________ 。
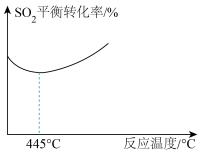
(5)其他条件不变时,随着温度的升高, 的平衡转化率随温度的变化曲线如图所示,温度高于445℃后
的平衡转化率随温度的变化曲线如图所示,温度高于445℃后 平衡转化率升高可能的原因
平衡转化率升高可能的原因___________ 。(已知硫的沸点约是445℃)
 、
、 、
、 等多种有害气体,合理治理烟道气中具有重要意义。
等多种有害气体,合理治理烟道气中具有重要意义。Ⅰ.烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:


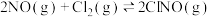

(1)则反应:
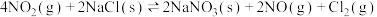

 、
、 的式子表示)。
的式子表示)。Ⅱ.利用
 可将
可将 转化为无害的
转化为无害的 ,其反应为:
,其反应为: 。在容积均为
。在容积均为 的甲、乙两个恒温(反应温度分别为℃、
的甲、乙两个恒温(反应温度分别为℃、 ℃)恒容密闭容器中,分别加入物质的量之比为
℃)恒容密闭容器中,分别加入物质的量之比为 的
的 和
和 ,测得各容器中
,测得各容器中 随反应时间
随反应时间 的变化情况如下表所示:
的变化情况如下表所示: 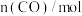 | 0 | 10 | 20 | 30 | 40 |
甲( ℃) ℃) | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙( ℃) ℃) | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
(2)

 ,该反应的
,该反应的
(3)
 时,该反应的平衡常数为
时,该反应的平衡常数为 和
和 ,平衡向
,平衡向Ⅲ.对烟道气中的进行回收再利用具有较高的社会价值和经济价值,涉及到的主要反应是:
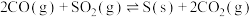
 。
。(4)向三个体积相同的恒容密闭容器中通入
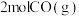 和
和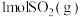 发生反应,反应体系的总压强随时间的变化如图所示。
发生反应,反应体系的总压强随时间的变化如图所示。
①实验
 中,
中, 内
内 的平均反应速率为
的平均反应速率为 。
。②与实验
 相比,实验
相比,实验 改变的条件可能是
改变的条件可能是③实验
 中
中 的平衡转化率为
的平衡转化率为(5)其他条件不变时,随着温度的升高,
 的平衡转化率随温度的变化曲线如图所示,温度高于445℃后
的平衡转化率随温度的变化曲线如图所示,温度高于445℃后 平衡转化率升高可能的原因
平衡转化率升高可能的原因
您最近一年使用:0次
名校
解题方法
5 . 氢能是一种理想的绿色能源,一种太阳能两步法甲烷蒸气重整制氢原理合成示意图如下:
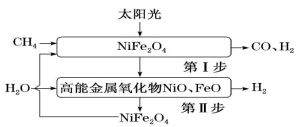
(1)第I步: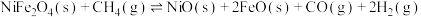
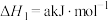 。总反应可表示为:
。总反应可表示为: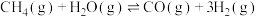
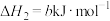 。写出第II步反应的热化学方程式:
。写出第II步反应的热化学方程式:___________ 。
(2)实验测得分步制氢比直接利用 和
和 反应具有更高的反应效率,原因是
反应具有更高的反应效率,原因是________ 。
(3)第I、II步反应的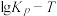 图像如下。
图像如下。
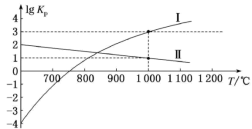
由图像可知a___________ b(填“大于”或“小于”), 时第I步反应平衡时
时第I步反应平衡时 的平衡分压
的平衡分压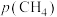
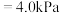 ,则平衡混合气体中
,则平衡混合气体中 的体积分数为
的体积分数为___________ (保留一位小数)。
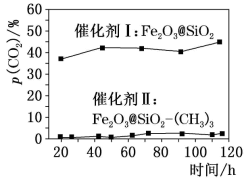
(4)第I步反应产生的合成气(CO和 的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应:
的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应: ,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内
,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内 的分数,据此应选择的催化剂是
的分数,据此应选择的催化剂是___________ (填“I”或“II”),选择的依据是___________ 。

(1)第I步:
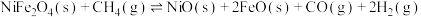
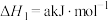 。总反应可表示为:
。总反应可表示为: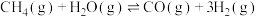
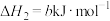 。写出第II步反应的热化学方程式:
。写出第II步反应的热化学方程式:(2)实验测得分步制氢比直接利用
 和
和 反应具有更高的反应效率,原因是
反应具有更高的反应效率,原因是(3)第I、II步反应的
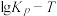 图像如下。
图像如下。
由图像可知a
 时第I步反应平衡时
时第I步反应平衡时 的平衡分压
的平衡分压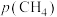
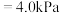 ,则平衡混合气体中
,则平衡混合气体中 的体积分数为
的体积分数为(4)第I步反应产生的合成气(CO和
 的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应:
的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应: ,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内
,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内 的分数,据此应选择的催化剂是
的分数,据此应选择的催化剂是
您最近一年使用:0次
名校
解题方法
6 . I. 可作大型船舶绿色燃科,可由CO或
可作大型船舶绿色燃科,可由CO或 制备。工业用
制备。工业用 制备
制备 原理如下:
原理如下:
反应1:
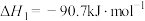
反应2:
 (副反应)
(副反应)
(1)反应3:
 ,该反应自发的条件
,该反应自发的条件________ (填“高温自发”、“低温自发”、“任意温度自发”或“任意温度不自发”)。
(2)不同压强下,按照 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
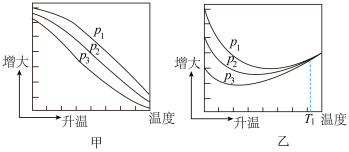
已知: 的平衡转化率
的平衡转化率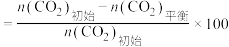 %
%
 的平衡产率
的平衡产率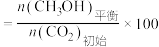 %
%
其中纵坐标表示 平衡转化率的是图
平衡转化率的是图___________ (填“甲”或“乙”);图乙中 温度时,三条曲线几乎交于一点且随温度升高而变大的原因是
温度时,三条曲线几乎交于一点且随温度升高而变大的原因是___________ 。
(3)在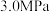 ,有催化剂的条件下,向密闭容器中充入
,有催化剂的条件下,向密闭容器中充入 和
和 ,
, 的平衡转化率与
的平衡转化率与 、CO的选择性随温度的变化如图所示,
、CO的选择性随温度的变化如图所示,
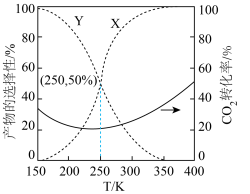
已知: (或CO)的选择性
(或CO)的选择性 %。
%。
若250℃反应达到平衡后, 的物质的量为
的物质的量为 ,则反应2的
,则反应2的
___________ 。
已知:对于气相反应,用组分B的平衡压强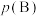 代替物质的量浓度
代替物质的量浓度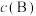 也可以表示平衡常数,记作
也可以表示平衡常数,记作 ,如
,如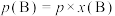 ,p为平衡压强,
,p为平衡压强,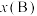 为平衡系统中B的物质的量分数。
为平衡系统中B的物质的量分数。
Ⅱ.已知水煤气反应:
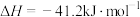 。
。
(4)以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,用两个化学方程式表示该催化反应历程(反应机理):
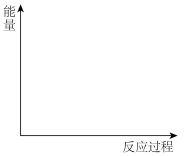
步骤I:___________ ;
步骤Ⅱ:___________ 。
(5)画出该反应无催化剂和有催化剂的能量与反应历程的关系图___________ 。
 可作大型船舶绿色燃科,可由CO或
可作大型船舶绿色燃科,可由CO或 制备。工业用
制备。工业用 制备
制备 原理如下:
原理如下:反应1:

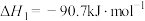
反应2:

 (副反应)
(副反应)(1)反应3:

 ,该反应自发的条件
,该反应自发的条件(2)不同压强下,按照
 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知:
 的平衡转化率
的平衡转化率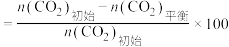 %
% 的平衡产率
的平衡产率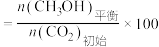 %
%其中纵坐标表示
 平衡转化率的是图
平衡转化率的是图 温度时,三条曲线几乎交于一点且随温度升高而变大的原因是
温度时,三条曲线几乎交于一点且随温度升高而变大的原因是(3)在
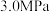 ,有催化剂的条件下,向密闭容器中充入
,有催化剂的条件下,向密闭容器中充入 和
和 ,
, 的平衡转化率与
的平衡转化率与 、CO的选择性随温度的变化如图所示,
、CO的选择性随温度的变化如图所示,
已知:
 (或CO)的选择性
(或CO)的选择性 %。
%。若250℃反应达到平衡后,
 的物质的量为
的物质的量为 ,则反应2的
,则反应2的
已知:对于气相反应,用组分B的平衡压强
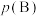 代替物质的量浓度
代替物质的量浓度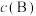 也可以表示平衡常数,记作
也可以表示平衡常数,记作 ,如
,如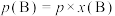 ,p为平衡压强,
,p为平衡压强,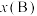 为平衡系统中B的物质的量分数。
为平衡系统中B的物质的量分数。Ⅱ.已知水煤气反应:

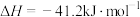 。
。(4)以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,用两个化学方程式表示该催化反应历程(反应机理):

步骤I:
步骤Ⅱ:
(5)画出该反应无催化剂和有催化剂的能量与反应历程的关系图
您最近一年使用:0次
2023-12-13更新
|
115次组卷
|
2卷引用:浙江省杭州第二中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 通过化学的方法实现 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径,由
减排途径,由 和
和 制备
制备 (二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:
(二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:
a.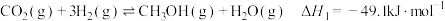
b.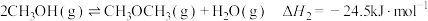
c.
已知: ,如:
,如: 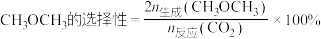 。
。
回答下列问题:
(1)写出 与
与 转化为
转化为 和
和 (反应d)的热化学方程式
(反应d)的热化学方程式______________________ 。
(2)反应a达到平衡时,若缩小体积增大压强,则 变
变____________ (填“大”或“小”)。
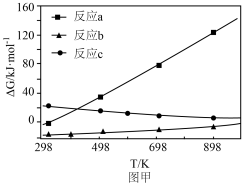
(3)反应a、b、c的吉布斯自由能随温度变化如图甲所示,298K时,能自发进行的反应有___________ ;反应c为熵______________ (填“增”或“减”)反应。
(4)向体积为 的恒压密闭容器中充入
的恒压密闭容器中充入 和
和 ,若仅考点上述反应,平衡时
,若仅考点上述反应,平衡时 和
和 的选择性及
的选择性及 的转化率随温度的变化如图乙实线所示。
的转化率随温度的变化如图乙实线所示。
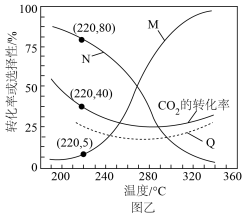
①图中曲线____________ (填“N”或“M”)表示 的选择性。
的选择性。
②平衡时 的转化率随温度的变化
的转化率随温度的变化____________ (填“可能”或“不可能”)如图中虚线Q所示。
③温度高于270℃,随着温度的升高, 的平衡转化率如图所示变化的原因是
的平衡转化率如图所示变化的原因是___________________ 。
④计算反应 在220℃下的平衡常数为
在220℃下的平衡常数为______________ (结果保留三位有效数字)。
 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径,由
减排途径,由 和
和 制备
制备 (二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:
(二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:a.
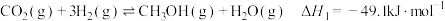
b.
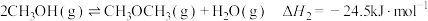
c.

已知:
 ,如:
,如: 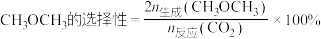 。
。回答下列问题:
(1)写出
 与
与 转化为
转化为 和
和 (反应d)的热化学方程式
(反应d)的热化学方程式(2)反应a达到平衡时,若缩小体积增大压强,则
 变
变(3)反应a、b、c的吉布斯自由能随温度变化如图甲所示,298K时,能自发进行的反应有

(4)向体积为
 的恒压密闭容器中充入
的恒压密闭容器中充入 和
和 ,若仅考点上述反应,平衡时
,若仅考点上述反应,平衡时 和
和 的选择性及
的选择性及 的转化率随温度的变化如图乙实线所示。
的转化率随温度的变化如图乙实线所示。
①图中曲线
 的选择性。
的选择性。②平衡时
 的转化率随温度的变化
的转化率随温度的变化③温度高于270℃,随着温度的升高,
 的平衡转化率如图所示变化的原因是
的平衡转化率如图所示变化的原因是④计算反应
 在220℃下的平衡常数为
在220℃下的平衡常数为
您最近一年使用:0次
2023-12-12更新
|
194次组卷
|
2卷引用:重庆市育才中学校、西南大学附中、万州中学2023-2024学年高二上学期12月联考化学试题
名校
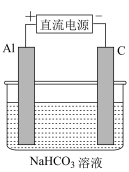
8 . I.氢叠氮酸( )和莫尔盐[
)和莫尔盐[ ]是两种常用原料。
]是两种常用原料。
(1)氢叠氮酸易溶于水,25℃时,该酸的电离常数为
①0.2mol/L的 溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,混合溶液中各离子和
溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,混合溶液中各离子和 分子浓度由大到小的顺序为
分子浓度由大到小的顺序为___________ 。
②已知T℃时,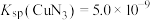 ,
,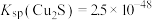 ,则相同温度下,
,则相同温度下, 该反应正反应方向
该反应正反应方向___________ (“能”或“不能”) 基本进行彻底,请通过计算说明___________ 。
(2)在 溶液中,加入
溶液中,加入 固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下:(已知莫尔盐的分子量为392)
固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下:(已知莫尔盐的分子量为392)
滴定终点的现象是___________ ,通过实验数据,计算该产品的纯度为___________ (用含字母a、c的式子表示)。上表第一次实验中记录数据明显大于后两次,其原因可能是___________ 。
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
II.锌及其化合物用途广泛。回答下列问题
(3)火法炼锌以闪锌矿(主要成分是ZnS)为主要原料,涉及的主要反应有:



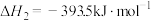

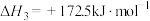

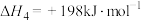
反应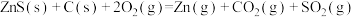 的
的
___________ kJ∙mol-1。
(4)银锌蓄电池工作原理为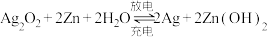 ,该蓄电池充电时,发生还原反应的物质是
,该蓄电池充电时,发生还原反应的物质是___________ ,正极反应分为两个阶段,第二阶段为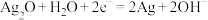 ,请写出第一阶段正极电极反应式
,请写出第一阶段正极电极反应式___________ 。
(5)以(4)中蓄电池作电源,用如图所示的装置在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是___________ (用相关的电极反应式和离子方程式表示)。
 )和莫尔盐[
)和莫尔盐[ ]是两种常用原料。
]是两种常用原料。(1)氢叠氮酸易溶于水,25℃时,该酸的电离常数为

①0.2mol/L的
 溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,混合溶液中各离子和
溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,混合溶液中各离子和 分子浓度由大到小的顺序为
分子浓度由大到小的顺序为②已知T℃时,
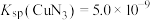 ,
,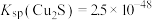 ,则相同温度下,
,则相同温度下, 该反应正反应方向
该反应正反应方向(2)在
 溶液中,加入
溶液中,加入 固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下:(已知莫尔盐的分子量为392)
固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下:(已知莫尔盐的分子量为392)| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液体积/mL 溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
II.锌及其化合物用途广泛。回答下列问题
(3)火法炼锌以闪锌矿(主要成分是ZnS)为主要原料,涉及的主要反应有:



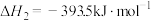

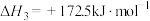

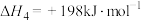
反应
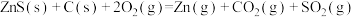 的
的
(4)银锌蓄电池工作原理为
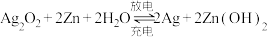 ,该蓄电池充电时,发生还原反应的物质是
,该蓄电池充电时,发生还原反应的物质是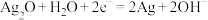 ,请写出第一阶段正极电极反应式
,请写出第一阶段正极电极反应式(5)以(4)中蓄电池作电源,用如图所示的装置在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是

您最近一年使用:0次
9 . 利用1-甲基萘(1-MN)制备四氢萘类物质(MTLs,包括1-MTL和5-MTL)。反应过程中伴有生成十氢萘(1-MD)的副反应,涉及反应如图:
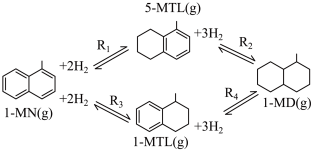
回答下列问题:
(1)1-甲基萘(1-MN)的组成元素电负性由小到大的顺序为___________ 。
(2)已知一定条件下反应 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则反应
,则反应 的焓变为
的焓变为___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(3)四个平衡体系的平衡常数与温度的关系如图甲所示。
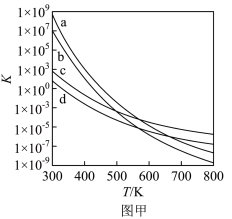
①c、d分别为反应 和
和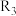 的平衡常数随温度变化的曲线,则表示反应
的平衡常数随温度变化的曲线,则表示反应 的平衡常数随温度变化曲线为
的平衡常数随温度变化曲线为___________ 。
②已知反应 的速率方程
的速率方程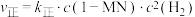 ,
,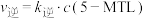 (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。温度
分别为正、逆反应速率常数,只与温度、催化剂有关)。温度 下反应达到平衡时
下反应达到平衡时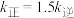 ,温度
,温度 下反应达到平衡时
下反应达到平衡时 。由此推知,
。由此推知,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③下列说法不正确的是___________ (填标号)。
A.四个反应均为放热反应
B.反应体系中1-MD最稳定
C.压强越大,温度越低越有利于生成四氢萘类物质
D.由上述信息可知,400K时反应 速率最快
速率最快
(4)1-MN在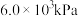 的高压
的高压 氛围下反应(
氛围下反应( 压强近似等于总压)。不同温度下达平衡时各产物的选择性
压强近似等于总压)。不同温度下达平衡时各产物的选择性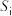 (某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数
(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数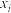 (
(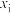 表示物种i与除
表示物种i与除 外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应
外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应 的平衡常数
的平衡常数
___________  (列出计算式)。
(列出计算式)。

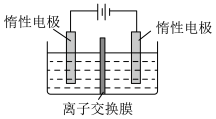
(5)利用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: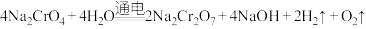 。则
。则 在
在___________ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为___________ 。

回答下列问题:
(1)1-甲基萘(1-MN)的组成元素电负性由小到大的顺序为
(2)已知一定条件下反应
 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则反应
,则反应 的焓变为
的焓变为 、
、 、
、 的代数式表示)。
的代数式表示)。(3)四个平衡体系的平衡常数与温度的关系如图甲所示。

①c、d分别为反应
 和
和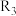 的平衡常数随温度变化的曲线,则表示反应
的平衡常数随温度变化的曲线,则表示反应 的平衡常数随温度变化曲线为
的平衡常数随温度变化曲线为②已知反应
 的速率方程
的速率方程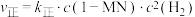 ,
,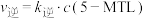 (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。温度
分别为正、逆反应速率常数,只与温度、催化剂有关)。温度 下反应达到平衡时
下反应达到平衡时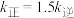 ,温度
,温度 下反应达到平衡时
下反应达到平衡时 。由此推知,
。由此推知,
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③下列说法不正确的是
A.四个反应均为放热反应
B.反应体系中1-MD最稳定
C.压强越大,温度越低越有利于生成四氢萘类物质
D.由上述信息可知,400K时反应
 速率最快
速率最快(4)1-MN在
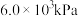 的高压
的高压 氛围下反应(
氛围下反应( 压强近似等于总压)。不同温度下达平衡时各产物的选择性
压强近似等于总压)。不同温度下达平衡时各产物的选择性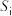 (某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数
(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数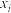 (
(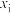 表示物种i与除
表示物种i与除 外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应
外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应 的平衡常数
的平衡常数
 (列出计算式)。
(列出计算式)。
(5)利用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: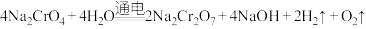 。则
。则 在
在
您最近一年使用:0次
解题方法
10 . 工业合成氨是20世纪的伟大成就之一,但化肥的过度使用、硝酸工业废气和机动车尾气的排放,给水体和大气带来了一定程度的污染,需要进行综合处理。
Ⅰ.含氮污染处理
(1)水体中氨氮处理:在微生物作用下,废水中 经两步反应被氧化成
经两步反应被氧化成
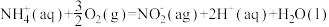 △H=-273kJ/mol
△H=-273kJ/mol
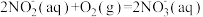 △H=-146kJ/mol
△H=-146kJ/mol
则 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(2)大气中NO处理:电解NaCl溶液(调节起始pH约为9)获得NaClO溶液,可用于去除大气中NO。其他条件相同,电解所得溶液中相关成分的浓度与电流强度的关系如图所示。

①用电解所得NaClO溶液氧化NO生成Cl-和 ,其离子方程式为:
,其离子方程式为:_______ 。
②电流强度大于4A,随着电流强度增大,电解所得溶液对NO去除率下降,其原因是:_______ 。
Ⅱ.合成氨:合成氨反应热化学方程式如下:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。
(3)关于合成氨的说法,正确的是_______ 。
A.合成氨反应的△H和△S都小于零
B.采用高温以提高反应的平衡转化率
C.将NH3液化后移去,利于反应速率提高和平衡正向移动
D.原料气须经过净化处理,以防止催化剂中毒和事故发生
E.采用高压以加快反应速率,提高的NH3产量
F.为提高H2转化率,可适当增大H2的浓度
(4)科学家发现,以H2O和N2为原料,熔融NaOH-KOH为电解质,纳米Fe2O3作催化剂,在250℃和常压下可实现电化学合成氨,阴极区发生的变化可按两步进行。已知第一步的反应为:Fe2O3+6e-+3H2O=2Fe+6OH-,则第二步的反应方程式为_______ 。
(5)若N2、H2 的初始投入量分别为0.1mol、0.3mol,在2L容器中反应,平衡后混合物中氨的体积分数(ψ)与温度、压强的关系如图所示。

①比较p2、p3的大小:p2_______ p3 (填“>”“<”或“=”),其原因是_______ 。
②比较平衡时A、B点对应的化学反应速率:vA(N2)_______ vB(N2) (填“>”“<”或“=”)。A、B点对应的化学平衡常数:KA_______ KB(填“>”“<”或“=”)。
③求出B点N2的转化率及KB的值(KB的值可以用分数表示),给出计算过程_______ 。
Ⅰ.含氮污染处理
(1)水体中氨氮处理:在微生物作用下,废水中
 经两步反应被氧化成
经两步反应被氧化成
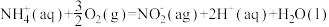 △H=-273kJ/mol
△H=-273kJ/mol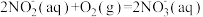 △H=-146kJ/mol
△H=-146kJ/mol则
 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是(2)大气中NO处理:电解NaCl溶液(调节起始pH约为9)获得NaClO溶液,可用于去除大气中NO。其他条件相同,电解所得溶液中相关成分的浓度与电流强度的关系如图所示。

①用电解所得NaClO溶液氧化NO生成Cl-和
 ,其离子方程式为:
,其离子方程式为:②电流强度大于4A,随着电流强度增大,电解所得溶液对NO去除率下降,其原因是:
Ⅱ.合成氨:合成氨反应热化学方程式如下:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。(3)关于合成氨的说法,正确的是
A.合成氨反应的△H和△S都小于零
B.采用高温以提高反应的平衡转化率
C.将NH3液化后移去,利于反应速率提高和平衡正向移动
D.原料气须经过净化处理,以防止催化剂中毒和事故发生
E.采用高压以加快反应速率,提高的NH3产量
F.为提高H2转化率,可适当增大H2的浓度
(4)科学家发现,以H2O和N2为原料,熔融NaOH-KOH为电解质,纳米Fe2O3作催化剂,在250℃和常压下可实现电化学合成氨,阴极区发生的变化可按两步进行。已知第一步的反应为:Fe2O3+6e-+3H2O=2Fe+6OH-,则第二步的反应方程式为
(5)若N2、H2 的初始投入量分别为0.1mol、0.3mol,在2L容器中反应,平衡后混合物中氨的体积分数(ψ)与温度、压强的关系如图所示。

①比较p2、p3的大小:p2
②比较平衡时A、B点对应的化学反应速率:vA(N2)
③求出B点N2的转化率及KB的值(KB的值可以用分数表示),给出计算过程
您最近一年使用:0次



