1 . 盐酸羟胺 是一种还原剂和显像剂,其化学性质与
是一种还原剂和显像剂,其化学性质与 类似。
类似。
(1) 被
被 取代可形成羟胺
取代可形成羟胺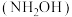 ,羟胺水溶液显碱性,用相关离子方程式解释原因
,羟胺水溶液显碱性,用相关离子方程式解释原因___________ 。
(2)已知氮原子上电子云密度越大则碱性越强,实验测得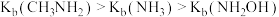 ,请解释原因:
,请解释原因:___________ 。
(3)采用原电池原理制备盐酸羟胺的装置如下图所示:

①含铁催化电极发生的电极反应式为___________ 。
②盐酸初始浓度相同,假设两侧溶液体积均为 且保持不变,理论上电路中通过
且保持不变,理论上电路中通过 电子时,左右两侧
电子时,左右两侧 浓度相差
浓度相差___________  。
。
 是一种还原剂和显像剂,其化学性质与
是一种还原剂和显像剂,其化学性质与 类似。
类似。(1)
 被
被 取代可形成羟胺
取代可形成羟胺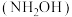 ,羟胺水溶液显碱性,用相关离子方程式解释原因
,羟胺水溶液显碱性,用相关离子方程式解释原因(2)已知氮原子上电子云密度越大则碱性越强,实验测得
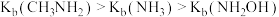 ,请解释原因:
,请解释原因:(3)采用原电池原理制备盐酸羟胺的装置如下图所示:

①含铁催化电极发生的电极反应式为
②盐酸初始浓度相同,假设两侧溶液体积均为
 且保持不变,理论上电路中通过
且保持不变,理论上电路中通过 电子时,左右两侧
电子时,左右两侧 浓度相差
浓度相差 。
。
您最近一年使用:0次
名校
2 . 已知 与2%的NaOH溶液反应:
与2%的NaOH溶液反应: 。下列叙述错误的是
。下列叙述错误的是
 与2%的NaOH溶液反应:
与2%的NaOH溶液反应: 。下列叙述错误的是
。下列叙述错误的是A. 分子是直线形非极性分子 分子是直线形非极性分子 | B.上述反应中涉及2种类型的晶体 |
C. 的键角大于 的键角大于 | D.NaOH的电子式为 |
您最近一年使用:0次
名校
解题方法
3 . 甲醛是家庭装修常见的污染物。一种催化氧化甲醛的反应:HCHO+O2 H2O+CO2.下列有关叙述正确的是
H2O+CO2.下列有关叙述正确的是
 H2O+CO2.下列有关叙述正确的是
H2O+CO2.下列有关叙述正确的是| A.HCHO分子中σ键和π键的数目之比为2:1 |
| B.HCHO分子中存在分子间氢键 |
| C.H2O是由极性键构成的非极性分子 |
| D.CO2中碳原子的杂化方式为sp |
您最近一年使用:0次
2024-03-08更新
|
261次组卷
|
4卷引用:江苏省盐城市响水县清源高级中学2023-2024学年高二上学期期中化学试卷(选修)
名校
4 . 对下列事实所给出的原因错误的是
| 选项 | 事实 | 原因 |
| A | 水中溶解性;苯<吡啶( ) ) | 吡啶能与水形成分子间氢键 |
| B | 物质的沸点: |  分子间存在氢键,而 分子间存在氢键,而 分子间不存在 分子间不存在 |
| C | 第一电离能: | 金属性: |
| D | 酸性: | 电负性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 硼元素在地壳中的含量仅为 ,但它却有着种类繁多的化合物。
,但它却有着种类繁多的化合物。
(1)基态 原子的电子排布式为
原子的电子排布式为___________ ;基态 原子的核外电子运动状态有
原子的核外电子运动状态有___________ 种。
(2)根据 的解离反应:
的解离反应: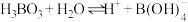 ,
,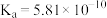 ,可判断
,可判断 是
是___________ 酸, 离子的VSEPR模型为
离子的VSEPR模型为___________ ,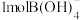 离子中含有
离子中含有___________  键。
键。
(3)分子式为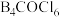 的化合物的结构如图,其中
的化合物的结构如图,其中 原子的杂化类型是
原子的杂化类型是___________ ,B-B-B键的键角___________ 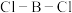 的键角(填“>”“<”或“=”)。
的键角(填“>”“<”或“=”)。

(4)在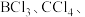 和
和 三种分子中,属于极性分子的是
三种分子中,属于极性分子的是___________ ,多原子分子中各原子若在同一平面,且有相互平行的 轨道,则
轨道,则 电子可在多个原子间运动,形成“离域
电子可在多个原子间运动,形成“离域 键”,上述三种分子中存在“离域
键”,上述三种分子中存在“离域 键”的是
键”的是___________ 。
 ,但它却有着种类繁多的化合物。
,但它却有着种类繁多的化合物。(1)基态
 原子的电子排布式为
原子的电子排布式为 原子的核外电子运动状态有
原子的核外电子运动状态有(2)根据
 的解离反应:
的解离反应: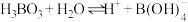 ,
,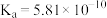 ,可判断
,可判断 是
是 离子的VSEPR模型为
离子的VSEPR模型为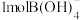 离子中含有
离子中含有 键。
键。(3)分子式为
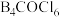 的化合物的结构如图,其中
的化合物的结构如图,其中 原子的杂化类型是
原子的杂化类型是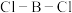 的键角(填“>”“<”或“=”)。
的键角(填“>”“<”或“=”)。
(4)在
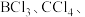 和
和 三种分子中,属于极性分子的是
三种分子中,属于极性分子的是 轨道,则
轨道,则 电子可在多个原子间运动,形成“离域
电子可在多个原子间运动,形成“离域 键”,上述三种分子中存在“离域
键”,上述三种分子中存在“离域 键”的是
键”的是
您最近一年使用:0次
名校
6 . 2023年9月23日第29届亚运会在杭州开幕,开幕式首次使用废碳(指 )再生的绿色甲醇作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
)再生的绿色甲醇作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
 )再生的绿色甲醇作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
)再生的绿色甲醇作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是| A.甲醇分子中最多有4个原子共平面 |
B.甲醇分子中C为 杂化,O为 杂化,O为 杂化 杂化 |
C. 为含极性键的非极性分子 为含极性键的非极性分子 |
D.“实现循环内的零排放”是指甲醇燃烧生成 , , 再转化为甲醇 再转化为甲醇 |
您最近一年使用:0次
2024-03-05更新
|
104次组卷
|
2卷引用:安徽省肥西宏图中学2023-2024学年高三上学期月考化学试卷
名校
7 . 下列对分子性质的解释中,不正确 的是

| A.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键 |
| B.碘易溶于四氯化碳、甲烷难溶于水都可用“相似相溶”规律解释 |
| C.过氧化氢是含有极性键和非极性键的极性分子 |
D.青蒿素的分子式为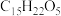 ,结构如图所示,该分子中包含7个手性碳原子 ,结构如图所示,该分子中包含7个手性碳原子 |
您最近一年使用:0次
2024-03-05更新
|
322次组卷
|
2卷引用:浙江省湖州市德清县求是高级中学有限公司2023-2024学年高二上学期期末考试化学试题
8 . 短周期元素X、Y、Z、W原子序数依次增大.基态X、Z、W原子均有两个未成对电子,W与Z同主族.下列说法错误的是
| A.第三电离能:Z>Y>X | B.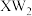 、 、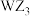 均为非极性分子 均为非极性分子 |
| C.Y、Z形成的化合物只有5种 | D.最高价含氧酸的酸性W大于X |
您最近一年使用:0次
23-24高二上·广东深圳·期末
名校
9 . 根据下列实验现象所得出的实验结论正确的是:
| 选项 | 实验现象 | 实验结论 |
| A | 将少量HA溶液加入Na2CO3溶液,未产生气泡。 | 酸性:HA<H2CO3 |
| B | 臭氧在CCl4中的溶解度高于在水中的溶解度 | O3为非极性分子 |
| C | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅。 | Na2CO3溶液中存在水解平衡 |
| D | 向10mLFeCl3溶液中滴加5mL等浓度的KI溶液,再滴加KSCN溶液,溶液最终变为血红色。 | FeCl3溶液与KI溶液的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列说法不正确的是
| A.熔点:金刚石>碳化硅>晶体硅>冰>干冰 |
| B.OF2分子的极性比水分子极性大 |
| C.等离子体具有良好的导电性,冠醚能识别碱金属离子 |
| D.某元素X气态基态原子的逐级电离能(kJ·mol-1)分别为738、1451、7733、10540、13630当它与氯气反应时可能生成的阳离子是X2+ |
您最近一年使用:0次



