解题方法
1 . 肉桂酸用在食品防腐保鲜上,是具有无公害的环保防腐剂。用在葡萄酒中,使其色泽光鲜。肉桂酸具有很强的兴奋作用,可直接添加于食品中。某小组设计实验制备肉桂酸并探究其性质。
【原理】

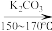
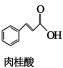
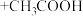
【性质】
【步骤】

【装置】利用图1装置完成步骤①,利用图2装置完成步骤②,抽滤操作用图3装置。(装置图中加热和固定装置省略)

回答下列问题:
(1)仪器A的名称是___________ 。完成步骤①选择合适的加热方式为___________ (填字母)。
a.热水浴(90℃以下) b.油浴(90~250℃) c.沙浴(250~350℃)
(2)完成步骤②,蒸馏的主要目的是___________ ,导管1与空气相通,其作用是___________ (答一条即可)。
(3)相对普通过滤,利用图3抽滤的主要优点有___________ (答一条即可)。
(4)第一次抽滤的滤渣主要成分是___________ 。
(5)证明步骤②中已达到实验目的主要现象是___________ 。
(6)探究肉桂酸的性质。取少量产品溶于水,并将溶液分成甲、乙两份进行如下实验:
上述实验结论正确的是___________ (填代号)。
【原理】

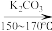

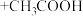
【性质】
| 物质 | 苯甲醛 | 肉桂酸 | 乙酸酐 | 乙酸 |
| 沸点 | 179℃ | 300℃ | 140℃ | 117.9℃ |
| 水溶性 | 微溶于水、无色油状液体 | 难溶于冷水、易溶于热水 | 与水反应生成乙酸 | 与水互溶 |

【装置】利用图1装置完成步骤①,利用图2装置完成步骤②,抽滤操作用图3装置。(装置图中加热和固定装置省略)

回答下列问题:
(1)仪器A的名称是
a.热水浴(90℃以下) b.油浴(90~250℃) c.沙浴(250~350℃)
(2)完成步骤②,蒸馏的主要目的是
(3)相对普通过滤,利用图3抽滤的主要优点有
(4)第一次抽滤的滤渣主要成分是
(5)证明步骤②中已达到实验目的主要现象是
(6)探究肉桂酸的性质。取少量产品溶于水,并将溶液分成甲、乙两份进行如下实验:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| a | 向甲中滴加少量的酸性 溶液 溶液 | 紫色变为无色 | 肉桂酸含碳碳双键 |
| b | 向乙中滴加少量的 溶液 溶液 | 产生气泡 | 肉桂酸的酸性比碳酸强 |
您最近一年使用:0次
2023-06-01更新
|
83次组卷
|
2卷引用:江西省2022-2023学年高二下学期5月统一调研测试化学试题
2 . 如图实验装置和方法进行相应实验,装置和现象均正确且能达到实验目的的是
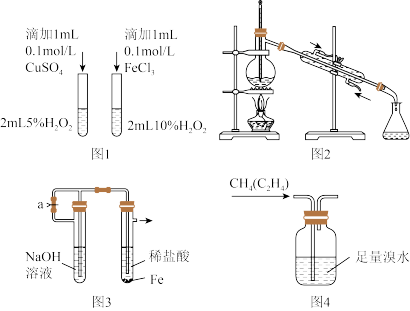

| A.图1比较Cu2+、Fe3+对反应速率的影响 |
| B.图2蒸馏海水得到淡水 |
| C.图3制备少量Fe(OH)2沉淀 |
| D.图4除甲烷中的乙烯 |
您最近一年使用:0次
3 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
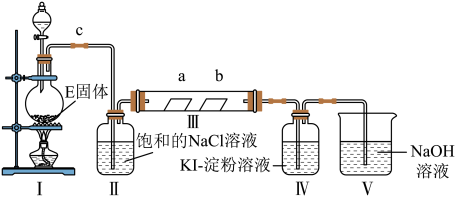
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)实验过程中,装置IV中的实验现象为___________ ;发生反应的化学方程式为___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的___________ 装置(填序号),
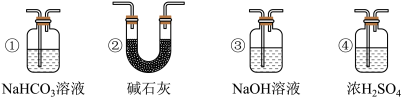
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式___________ 。

(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是
(2)装置Ⅱ的作用是
(3)实验过程中,装置IV中的实验现象为
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的

(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式
您最近一年使用:0次
名校
解题方法
4 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
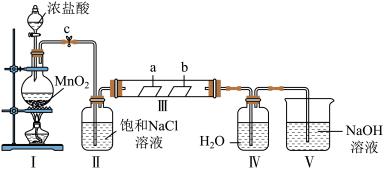
回答下列问题:
(1)加入药品前,必须先___________ 。
(2)装置Ⅰ中发生反应的化学方程式为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在___________ 和___________ (填装置序号)之间添加洗气装置,该装置的作用是___________ 。
(4)装置Ⅴ中NaOH溶液的作用是___________ ,相关反应的化学方程式为___________ 。
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有___________ 。

回答下列问题:
(1)加入药品前,必须先
(2)装置Ⅰ中发生反应的化学方程式为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在
(4)装置Ⅴ中NaOH溶液的作用是
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有
您最近一年使用:0次
2023·全国·模拟预测
解题方法
5 . 为完成各组实验,下列所选试剂、实验操作方法和实验现象的描述均正确的是
| 选项 | 实验目的 | 试剂 | 操作方法 | 实验现象 |
| A | 制备 并检验其性质 并检验其性质 | 浓氨水、蒸馏水、pH试纸 | 加热浓氨水,用湿润的pH试纸检验逸出的气体 | 浓氮水冒气泡,pH试纸变蓝 |
| B | 检验溴乙烷中含溴元素 | 溴乙烷、KOH溶液、 溶液 溶液 | 加热溴乙烷与KOH的混合液,然后滴加 溶液 溶液 | 有淡黄色沉淀生成 |
| C | 钠盐的焰色试验 |  溶液、稀硫酸 溶液、稀硫酸 | 用铂丝蘸取稀硫酸,并在酒精灯火焰上灼烧,然后再蘸取 溶液灼烧 溶液灼烧 | 焰色为黄色 |
| D | 探究金属腐蚀类型 | NaCl溶液、铁钉 | 将铁钉用NaCl溶液浸泡,然后放入气密性良好的下列装置中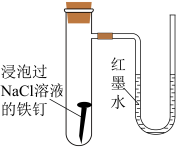 | U形管中红墨水右端高、左端低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
22-23高二下·全国·课时练习
解题方法
6 . 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
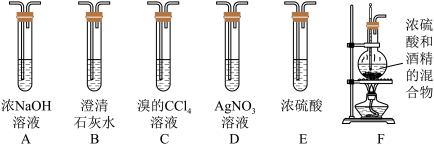
(1)实验中,混合浓硫酸与乙醇的方法是将_______ 慢慢加入另一种物质中;加热F装置时必须使液体温度_______ 。
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:_______ 。
(3)为实现上述实验目的,装置的连接顺序为F→_______ →D(各装置限用一次)。
(4)当C中观察到_______ 时,表明单质溴能与乙烯反应;当D中_______ 时,表明C中发生的是取代反应;若D中没有出现前面所描述的现象时,表明C中发生的是_______ 反应。
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有_______ 个。
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体

(1)实验中,混合浓硫酸与乙醇的方法是将
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:
(3)为实现上述实验目的,装置的连接顺序为F→
(4)当C中观察到
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体
您最近一年使用:0次
名校
7 . Ⅰ.某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
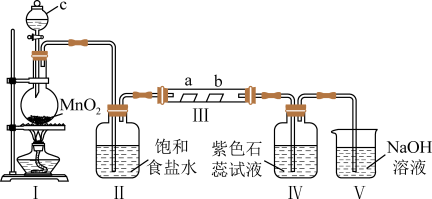
(1)装置Ⅰ中仪器c的名称是_______ ,写出装置Ⅰ中制备Cl2的化学方程式为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的_______ 装置(填序号)。

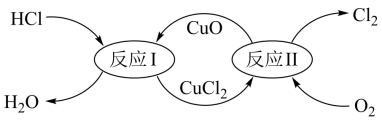
(4)“地康法”制取Cl2的反应原理如图所示,在450℃条件下,反应Ⅱ的化学方程式为_______ 。
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组设计了如下实验方案。
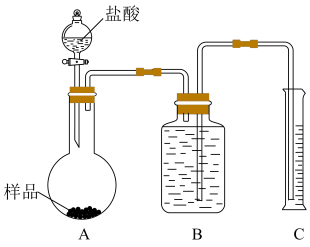
(5)把一定质量的样品与足量盐酸反应后,用如图所示装置测定产生CO2气体的体积,为了使测量结果准确,B中溶液选用_______ ,但选用该溶液后实验结果仍然不够准确,可能的原因是_______ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(4)“地康法”制取Cl2的反应原理如图所示,在450℃条件下,反应Ⅱ的化学方程式为

Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组设计了如下实验方案。
(5)把一定质量的样品与足量盐酸反应后,用如图所示装置测定产生CO2气体的体积,为了使测量结果准确,B中溶液选用

您最近一年使用:0次
2023-01-19更新
|
339次组卷
|
2卷引用: 湖北省武汉市新洲区第一中学2022--2023学年高一上学期阶段检测化学试题
名校
8 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。
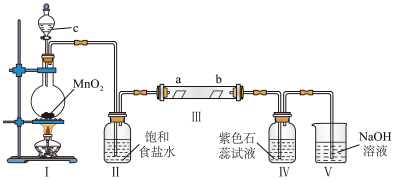
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象___________ 。
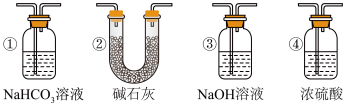
(4)实验结束后,该组同学在装置Ⅲ中视察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(5)有一种“地康法”制取氯气的反应原理如图所示:
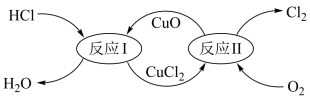
①反应Ⅰ属于___________ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为 ,请用单线桥表示该反应中电子转移的方向和数目:
,请用单线桥表示该反应中电子转移的方向和数目:___________ 。
③工业生产中常用氨气检查输送氯气的管道是否有 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中视察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
 ,请用单线桥表示该反应中电子转移的方向和数目:
,请用单线桥表示该反应中电子转移的方向和数目:③工业生产中常用氨气检查输送氯气的管道是否有
 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
您最近一年使用:0次
2022-12-06更新
|
251次组卷
|
2卷引用:天津市天津中学2022-2023学年高一上学期期中考试化学试题
名校
解题方法
9 . 某课外活动小组设计如图装置验证“二氧化碳与水接触时才能和过氧化钠反应”,已知盐酸具有挥发性且易挥发出HCl气体。
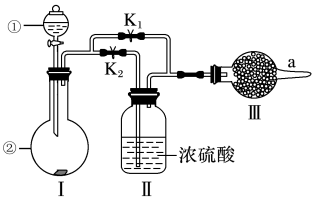
(1)过氧化钠与二氧化碳反应的化学方程式是_________ 。
(2)装置Ⅰ是制备纯净的_________ (写化学式),则仪器①和②中最适宜的药品组合是_________ (填字母)。
a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)装置Ⅲ中盛装的是过氧化钠,具体实验时操作步骤如下:
第一步:打开分液漏斗活塞,再打开弹簧夹 (
( 此时处于关闭状态),将带火星的木条置于a口。
此时处于关闭状态),将带火星的木条置于a口。
第二步:关闭 ,打开
,打开 ,再将带火星的木条置于a口。
,再将带火星的木条置于a口。
现象:第一步观察到带火星的木条始终不复燃。第二步观察到带火星的木条也始终不复燃。
①为了观察到木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是_________ 。
②乙采纳甲的建议在Ⅲ后安装一个盛有碱石灰的干燥管,再将带火星的木条置于盛有碱石灰的干燥管管口。改进后本实验预期现象是_________ 。这也不能证明实验结论,原因是_________ (用化学方程式表示)。
(4)为进一步达到实验目的,应补充的实验是:取第二步反应后的Ⅲ中所得固体少量于试管中,_________ (写出实验操作、现象及结论)。

(1)过氧化钠与二氧化碳反应的化学方程式是
(2)装置Ⅰ是制备纯净的
a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)装置Ⅲ中盛装的是过氧化钠,具体实验时操作步骤如下:
第一步:打开分液漏斗活塞,再打开弹簧夹
 (
( 此时处于关闭状态),将带火星的木条置于a口。
此时处于关闭状态),将带火星的木条置于a口。第二步:关闭
 ,打开
,打开 ,再将带火星的木条置于a口。
,再将带火星的木条置于a口。现象:第一步观察到带火星的木条始终不复燃。第二步观察到带火星的木条也始终不复燃。
①为了观察到木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是
②乙采纳甲的建议在Ⅲ后安装一个盛有碱石灰的干燥管,再将带火星的木条置于盛有碱石灰的干燥管管口。改进后本实验预期现象是
(4)为进一步达到实验目的,应补充的实验是:取第二步反应后的Ⅲ中所得固体少量于试管中,
您最近一年使用:0次
名校
10 . 某校化学兴趣小组为探究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)装置Ⅰ中仪器c的名称是________ ,实验室以二氧化锰和浓盐酸共热制备氯气的化学方程式为__________________ 。
(2)装置Ⅱ的作用是__________________________________________ 。
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是__________________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的________ 装置(填序号)。
① ②
② ③
③ ④
④
(5)工业生产中常用NH3检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟(NH4Cl固体)生成,同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:____________ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①
 ②
② ③
③ ④
④
(5)工业生产中常用NH3检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟(NH4Cl固体)生成,同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
2022-12-01更新
|
117次组卷
|
4卷引用:云南省澄江市第一中学2022-2023学年高一上学期期中考试化学试题



