名校
解题方法
1 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
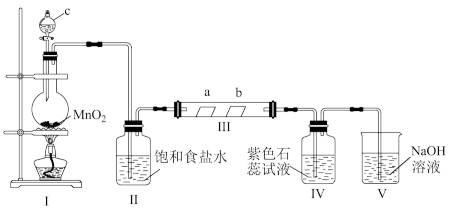
(1)装置Ⅰ中仪器c的名称是___ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___ 。
(2)装置Ⅱ的作用是___
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___ 。
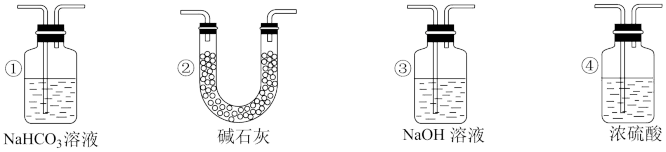
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___ 装置(填序号)。
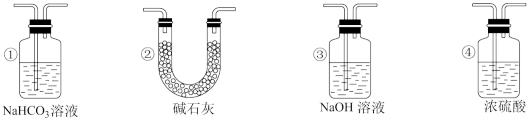
(5)有一种“地康法”制取氯气的反应原理如图所示:
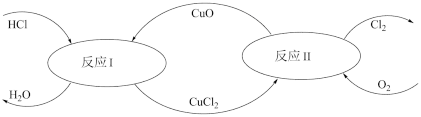
①反应Ⅰ属于___ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为____ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:___ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
2021-09-24更新
|
796次组卷
|
6卷引用:福建省泉州市第五中学2020-2021学年高一上学期期中考化学试题
福建省泉州市第五中学2020-2021学年高一上学期期中考化学试题辽宁省营口市第二高级中学2021-2022学年高三上学期第一次月考化学试题(已下线)必考点09 氯气的制取 氯离子的检验-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)广东省佛山市第一中学2021-2022学年高一上学期期中考试化学试题(已下线)衔接点16 氯气的性质-2022年初升高化学无忧衔接?陕西省榆林市府谷县第一中学2023-2024学年高一上学期12月月考化学试题
2 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置III中a为干燥的红色纸,b为湿润的红色纸。
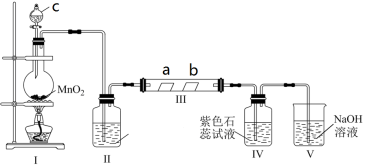
(1)装置I中仪器c的名称是_______ ,装置II盛放的药品是_______ 。
(2)实验室以二氧化锰和浓盐酸制备氯气的化学方程式为______ 。
(3)实验过程中装置IV中的实验现象______ 。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,还需在装置II与III之间添加下列______ 装置(填序号)。

(5)有一种“地康法”制取氯气的反应原理如图所示:
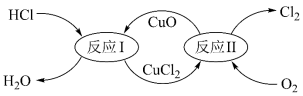
①反应II属于___________ (填四种基本反应类型之一)。
②若要制得0.5molCl2则消耗O2(标准状况)的体积约______ L,转移的电子数目是_______ 。

(1)装置I中仪器c的名称是
(2)实验室以二氧化锰和浓盐酸制备氯气的化学方程式为
(3)实验过程中装置IV中的实验现象
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,还需在装置II与III之间添加下列

(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应II属于
②若要制得0.5molCl2则消耗O2(标准状况)的体积约
您最近一年使用:0次
2022-02-24更新
|
276次组卷
|
2卷引用:广东省东莞市东华高级中学2021-2022学年高一上学期期末考试化学试题
名校
3 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。 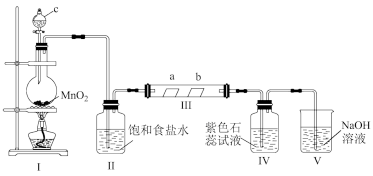
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式为___________ ,HCl在反应中体现的性质为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
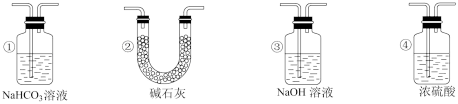
(5)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:___________ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
4 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
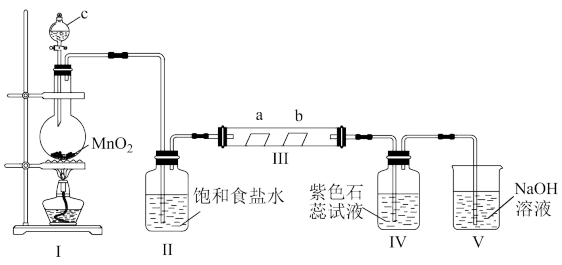
(1)装置Ⅰ中仪器c的名称是___________ ,实验室用二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅴ中发生反应的离子方程式是___________ 。
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象是___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
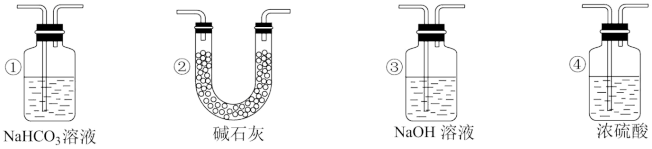
(5)有一种“地康法”制取氯气的反应原理如图所示:
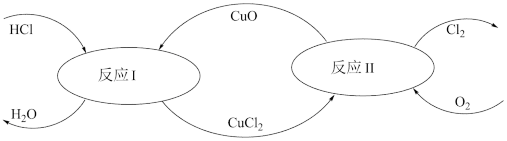
在450℃条件下,反应Ⅱ的化学方程式为___________ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅴ中发生反应的离子方程式是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
名校
5 . (1)根据下列实验装置图,回答有关问题:
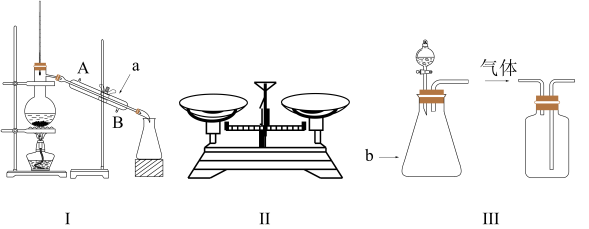
①实验室用I装置制取蒸馏水,仪器a的名称是___________ ,冷水应从___________ 进___________ 出。
②装置II是实验室经常用于固体药品称量使用的托盘天平。称量时,应将称量物放在___________ (选填“左盘”或“右盘”);如果称量时使用了游码,且将称量物放反,则所称得样品质量的数据比实际值___________ (选填“大”、“不变”、“小”)。
③装置III是实验室制备气体的常用气体发生装置和收集装置,仪器b的名称是___________ ;若用MnO2与H2O2制氧气,MnO2在反应中的作用是___________ ;___________ (选填“能”或“不能”)用此收集装置的收集方法收集CO2。
(2)扎西同学在化学兴趣小组中提出一个猜想:“根据学习过的化学反应CaCO3+CO2+H2O=Ca(HCO3)2可以知道,Na2CO3溶液也能与CO2发生反应”。为了确定扎西同学猜想是否正确,兴趣小组在老师的指导下,通过实验探究的方法,完成了对该猜想的判断。请你完成兴趣小组在实验探究活动中的部分实验报告。
【实验目的】探究Na2CO3溶液与CO2的反应
【实验药品】Na2CO3溶液、饱和的NaHCO3溶液、大理石、CaCl2、CaO、稀盐酸、稀硫酸、浓硫酸、澄清石灰水
【查阅资料】NaHCO3能与Ca(OH)2发生反应:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O。Ca(HCO3)2易溶于水
【实验装置】

【实验操作步骤与现象】
①制取二氧化碳时应选用上述的___________ (填药品名称)。
②将制得的CO2通过饱和NaHCO3溶液洗气瓶的目的是___________ 。
③使过量CO2通入装置 Ⅲ,充分反应后,将其中所得的溶液取出3mL于试管中,然后向试管中加入___________ 试剂(请从以上给出的药品中选择):
a.当试管中___________ 现象时,Na2CO3溶液与CO2没有发生反应;
b.当试管中___________ 现象时,Na2CO3溶液与CO2发生了化学反应,其反应的化学方程式为:___________ 。
【结论】通过实验探究,扎西同学的猜想是正确的。
【应用】你能否依据此化学反应的规律,再写出一个类似的化学反应方程式(写上述已有的两个反应不得分):___________ 。

①实验室用I装置制取蒸馏水,仪器a的名称是
②装置II是实验室经常用于固体药品称量使用的托盘天平。称量时,应将称量物放在
③装置III是实验室制备气体的常用气体发生装置和收集装置,仪器b的名称是
(2)扎西同学在化学兴趣小组中提出一个猜想:“根据学习过的化学反应CaCO3+CO2+H2O=Ca(HCO3)2可以知道,Na2CO3溶液也能与CO2发生反应”。为了确定扎西同学猜想是否正确,兴趣小组在老师的指导下,通过实验探究的方法,完成了对该猜想的判断。请你完成兴趣小组在实验探究活动中的部分实验报告。
【实验目的】探究Na2CO3溶液与CO2的反应
【实验药品】Na2CO3溶液、饱和的NaHCO3溶液、大理石、CaCl2、CaO、稀盐酸、稀硫酸、浓硫酸、澄清石灰水
【查阅资料】NaHCO3能与Ca(OH)2发生反应:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O。Ca(HCO3)2易溶于水
【实验装置】

【实验操作步骤与现象】
①制取二氧化碳时应选用上述的
②将制得的CO2通过饱和NaHCO3溶液洗气瓶的目的是
③使过量CO2通入装置 Ⅲ,充分反应后,将其中所得的溶液取出3mL于试管中,然后向试管中加入
a.当试管中
b.当试管中
【结论】通过实验探究,扎西同学的猜想是正确的。
【应用】你能否依据此化学反应的规律,再写出一个类似的化学反应方程式(写上述已有的两个反应不得分):
您最近一年使用:0次
名校
6 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
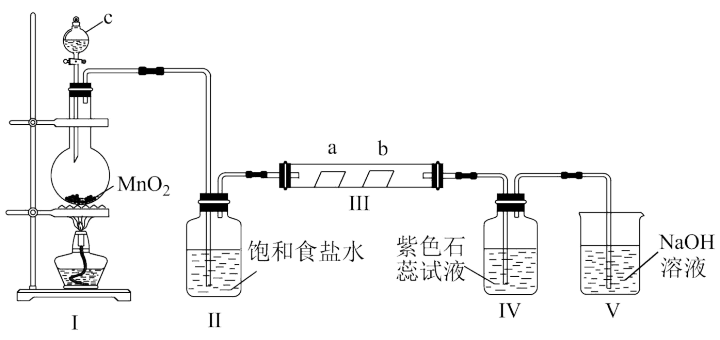
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式___________ ,每生成1mol该气体,K2FeO4转移的电子数目为___________ NA。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式
您最近一年使用:0次
2021-12-18更新
|
293次组卷
|
2卷引用:贵州省黔南州都匀市都匀第一中学2021-2022学年高一上学期期中化学试题
名校
7 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
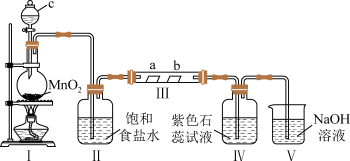
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置V的作用是___________ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
① ②
②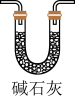 ③
③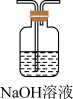 ④
④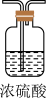
(5)有一种“地康法”制取氯气的反应原理如图所示:
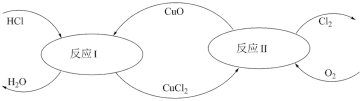
在450℃条件下,反应Ⅱ的化学方程式为___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置V的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①
 ②
② ③
③ ④
④
(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
2021-11-10更新
|
155次组卷
|
2卷引用:安徽师范大学附属中学2021-2022学年高一上学期期中考查化学试题
8 . 氯化铁可用作金属蚀刻、有机合成的催化剂,研究其制备及性质是一个重要的课题。

(1)氯化铁晶体的制备:
①实验过程中装置乙发生反应的离子方程式有___________ 、___________ ,仪器丙的作用为___________ 。
②为顺利达成实验目的,上述装置中弹簧夹打开和关闭的顺序为___________ 。
③反应结束后,将乙中溶液边加入___________ ,边进行加热浓缩、冷却结晶、过滤、洗涤、干燥即得到产品。
(2)氯化铁的性质探究:
某兴趣小组将饱和FeCl3溶液进行加热蒸发、蒸干灼烧,在试管底部没有得到预期的红棕色固体。为进一步探究该固体的成分设计了如下实验。(查阅文献知:①FeCl3溶液浓度越大,水解程度越小②氯化铁的熔点为306 ℃、沸点为315 ℃,易升华,气态FeCl3会分解成FeCl2和Cl2 ③FeCl2熔点为670 ℃)


(1)氯化铁晶体的制备:
①实验过程中装置乙发生反应的离子方程式有
②为顺利达成实验目的,上述装置中弹簧夹打开和关闭的顺序为
③反应结束后,将乙中溶液边加入
(2)氯化铁的性质探究:
某兴趣小组将饱和FeCl3溶液进行加热蒸发、蒸干灼烧,在试管底部没有得到预期的红棕色固体。为进一步探究该固体的成分设计了如下实验。(查阅文献知:①FeCl3溶液浓度越大,水解程度越小②氯化铁的熔点为306 ℃、沸点为315 ℃,易升华,气态FeCl3会分解成FeCl2和Cl2 ③FeCl2熔点为670 ℃)

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K,充入氮气 | D中有气泡产生 | ①充入N2的原因 |
| 关闭K,加热至600 ℃,充分灼烧固体 | B中出现棕黄色固体 | ②产生现象的原因 |
| 实验结束,振荡C静置 | ③ | ④2FeCl3 2FeCl2+Cl2 2FeCl2+Cl2 |
| ⑤结合以上实验和文献资料,该未知固体可以确定的成分有 | ||
您最近一年使用:0次
名校
9 . KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。
(一)KMnO4的制备,分步骤I、II两步进行。
步骤I:先利用如图所示装置制备K2MnO4


(1)装置A应选用______ (填a、b或c)。
(2)装置B中所盛试剂的名称为______ 。
(3)装置C处反应生成K2MnO4的化学方程式为______ 。
步骤II:由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③再将滤液进行一系列处理,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为______ ;
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录]
(5)为完成实验目的,H2C2O4溶液的物质的量浓度不低于______ 。
(6)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=______ 。
(一)KMnO4的制备,分步骤I、II两步进行。
步骤I:先利用如图所示装置制备K2MnO4


(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成K2MnO4的化学方程式为
步骤II:由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③再将滤液进行一系列处理,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录]
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 一定浓度mol·L-1 H2C2O4溶液 | H2O | 0.05 mol·L-1 KMnO4溶液 | 3 mol·L-1稀硫酸 | ||
| 1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
| 2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
| 3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
(6)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=
您最近一年使用:0次
10 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
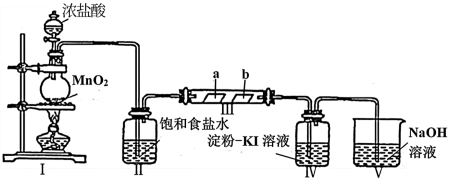
(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为___________ 。
(2)实验过程中装置Ⅳ中的实验现象为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图中的___________ (填序号)装置。
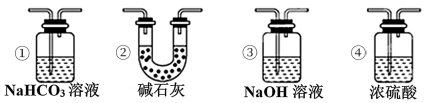
(4)装置V的作用___________ ,写出装置V中发生反应的化学方程式___________

(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为
(2)实验过程中装置Ⅳ中的实验现象为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图中的

(4)装置V的作用
您最近一年使用:0次



