真题
解题方法
1 . 明矾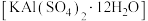 可用作净水剂。下列说法正确的是
可用作净水剂。下列说法正确的是
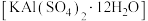 可用作净水剂。下列说法正确的是
可用作净水剂。下列说法正确的是A.半径: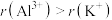 | B.电负性: |
C.沸点: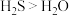 | D.碱性: |
您最近一年使用:0次
名校
2 .  参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是
①催化剂是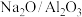 复合催化剂,如果催化剂是
复合催化剂,如果催化剂是 则主要发生乙苯的直接脱氢生成苯乙烯和氢气
则主要发生乙苯的直接脱氢生成苯乙烯和氢气
 参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是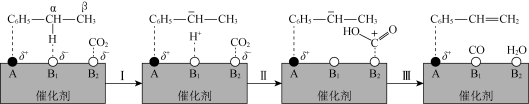
①催化剂是
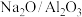 复合催化剂,如果催化剂是
复合催化剂,如果催化剂是 则主要发生乙苯的直接脱氢生成苯乙烯和氢气
则主要发生乙苯的直接脱氢生成苯乙烯和氢气②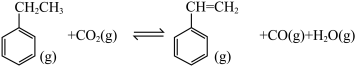

| A.反应过程中需要控制催化剂表面的酸碱性,不能太高或太低 |
B.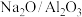 复合催化剂使 复合催化剂使 位点带较多负电荷,活化C-H发生耦合脱氢 位点带较多负电荷,活化C-H发生耦合脱氢 |
C.恒温恒容,其他条件不变时,适当提高 分压,可能使反应速率加快 分压,可能使反应速率加快 |
D.恒温恒压, 能提高乙苯的平衡转化率是降低了气体分压并消耗了 能提高乙苯的平衡转化率是降低了气体分压并消耗了 ,使平衡正向移动 ,使平衡正向移动 |
您最近一年使用:0次
真题
解题方法
3 . 实验室进行铁钉镀锌实验。下列相关原理、装置及操作不正确的是
| A | B | C | D |
|
|
|
|
配制 溶液 溶液 | 铁钉除油污 | 铁钉除锈 | 铁钉镀锌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . K是一种抗病毒药物的重要中间体,K的一种合成路线如下(部分试剂和条件略去)。
(1)A中官能团的名称为___________ 。
(2)B中碳原子的轨道杂化类型为___________ 。
(3)由C生成E的化学方程式为___________ 。
(4)E→F的反应类型为___________ 。
(5)H的结构简式为___________ 。
(6)K分子中具有孤电子对的原子数目有___________ 个。
(7)在H的同分异构体中,同时满足下列条件的共有___________ 种(不考虑立体异构)。
①含有苯环且苯环上只有一个取代基;
②能与金属钠反应产生 。
。
其中,不含手性碳原子的同分异构体的结构简式为___________ (任写一种)。
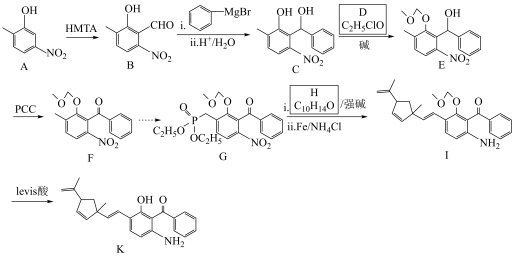
已知:.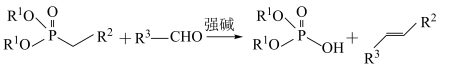
(1)A中官能团的名称为
(2)B中碳原子的轨道杂化类型为
(3)由C生成E的化学方程式为
(4)E→F的反应类型为
(5)H的结构简式为
(6)K分子中具有孤电子对的原子数目有
(7)在H的同分异构体中,同时满足下列条件的共有
①含有苯环且苯环上只有一个取代基;
②能与金属钠反应产生
 。
。其中,不含手性碳原子的同分异构体的结构简式为
您最近一年使用:0次
5 . 卡维地洛类药物(丁)可用于治疗原发性高血压、有症状的充血性心力衰竭。以甲为原料合成丁的方法如下图所示。下列说法正确的是

| A.试剂X可以是足量的NaOH溶液 |
| B.乙、丙、丁均能与盐酸反应 |
| C.丙、丁互为同系物 |
| D.戊的同分异构体有3种 |
您最近一年使用:0次
名校
6 . 葡萄糖酸钙是一种重要的补钙剂,工业上以葡萄糖、碳酸钙为原料,在溴化钠溶液中采用间接电氧化反应制备葡萄糖酸钙,其阳极区反应过程如下:
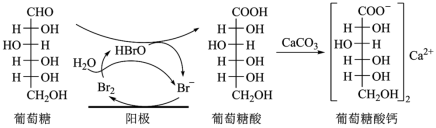
| A.溴化钠起催化和导电作用 |
B.每生成 葡萄糖酸钙,理论上电路中转移了0.1NA电子 葡萄糖酸钙,理论上电路中转移了0.1NA电子 |
| C.葡萄糖酸能通过分子内反应生成含有六元环状结构的产物 |
| D.葡萄糖能发生氧化、还原、取代、加成和消去反应 |
您最近一年使用:0次
7日内更新
|
75次组卷
|
2卷引用:2024届宁夏回族自治区银川一中高三下学期第四次模拟考试理科综合试卷-高中化学
名校
解题方法
7 . 下列离子方程式书写正确的是
A.乙酰胺与盐酸混合共热:CH3CONH2+H2O+H+ CH3COOH+NH CH3COOH+NH |
| B.向硝酸银溶液中滴入少量氨水:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O |
C.向Na2S2O3溶液中加入足量稀硝酸:S2O +2H+=S↓+SO2↑+H2O +2H+=S↓+SO2↑+H2O |
D.一定条件下,由乳酸[CH3CH(OH)COOH]合成聚乳酸的化学方程式: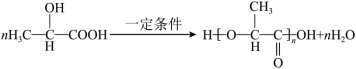 |
您最近一年使用:0次
7日内更新
|
195次组卷
|
2卷引用:安徽省合肥一六八中学 (东校区)2024届高三下学期最后一卷(三模)化学试卷
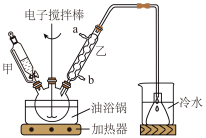
8 . 清凉茶酸乙酯(CH2CH=CHCH=CHCOOCH2CH3)是一种消毒杀菌剂,对细菌霉菌等有灭活作用。通过酯化反应制备清凉茶酸乙酯的方法如图,实验装置(部分夹持装置省略)如图所示。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X。
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如表:
(1)仪器甲的名称为______ 。
(2)写出实验中三颈烧瓶中发生的主要反应______ ,其中环己烷的作用是______ 。
(3)加热搅拌过程中忘加沸石,正确的操作是______ 。
(4)下列有关该实验过程,正确的是______ 。
(5)计算该制备实验的产率:______ (保留三位有效数字)。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X。
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如表:
| 沸点/℃ | 密度/(g•cm-3) | 水溶性 | 备注 | |
| 乙醇 | 78 | 0.789 | 混溶 | |
| 清凉茶酸 | 228 | 1.204 | 易溶 | |
| 清凉茶酸乙酯 | 195 | 0.926 | 难溶 | |
| 环己烷 | 80.7 | 0.780 | 难溶 | 挥发过程中可带出较多的水 |
(2)写出实验中三颈烧瓶中发生的主要反应
(3)加热搅拌过程中忘加沸石,正确的操作是
(4)下列有关该实验过程,正确的是
| A.乙中的进水口为a |
| B.操作X使用的玻璃仪器有玻璃棒,漏斗,烧杯 |
| C.加入小苏打是为了中和混合物中的酸性物质 |
| D.分液后的有机层加入碱石灰干燥 |
您最近一年使用:0次
真题
解题方法
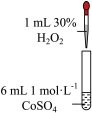
9 . 学习小组为探究 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。
已知: 为粉红色、
为粉红色、 为蓝色、
为蓝色、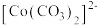 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:
(1)配制 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的_______ (填标号)。
_______ (填“能”或“不能”)催化 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是_______ 。实验Ⅲ初步表明 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式_______ 、_______ 。
(3)实验I表明,反应 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因_______ 。_______ 、_______ 。
 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
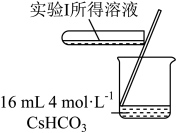
的分解及相关性质,室温下进行了实验I~Ⅳ。| 实验I | 实验Ⅱ | 实验Ⅲ |
|
|
|
| 无明显变化 | 溶液变为红色,伴有气泡产生 | 溶液变为墨绿色,并持续产生能使带火星木条复燃的气体 |
 为粉红色、
为粉红色、 为蓝色、
为蓝色、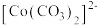 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:(1)配制
 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的a.  b.
b.  c.
c.  d.
d.

 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式(3)实验I表明,反应
 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因实验Ⅳ:
您最近一年使用:0次
真题
解题方法
10 . 过量 与以下
与以下 的溶液反应,下列总反应方程式错误的是
的溶液反应,下列总反应方程式错误的是
 与以下
与以下 的溶液反应,下列总反应方程式错误的是
的溶液反应,下列总反应方程式错误的是| 溶液 | 现象 | 化学方程式 | |
| A |  | 产生淡黄色沉淀 |  |
| B |  | 溶液由棕黄色变浅绿色 | 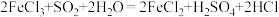 |
| C |  | 溶液褪色,产生白色沉淀 | 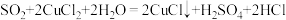 |
| D |  (含酚酞) (含酚酞) | 溶液由红色变无色 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次