名校
1 . 油条是我国传统食品,其做法是将明矾[KAl(SO4)2•12H2O]、纯碱、食盐按比例加入温水中,再加入面粉,搅拌成面团,放置,使面团产生气体,形成孔洞,放置过程发生反应:3Na2CO3+KAl(SO4)2•12H2O=3Na2SO4+K2SO4+3CO2↑+2Al(OH)3↓+21H2O。下列有关判断正确的是
| A.明矾属于混合物 |
| B.放置过程发生的反应中,反应物和生成物均为电解质 |
C.KAl(SO4)2在水溶液中的电离方程式为KAl(SO4)2=K++Al3++SO |
D.该反应说明Al3+与CO 不能大量共存 不能大量共存 |
您最近一年使用:0次
名校
2 . 短周期主族元素X、Y、A、B、C在元素周期表的相对位置如图所示,A是电负最大的元素,下列说法不正确的是
| X | A | ||
| Y | C | B |
| A.原子半径由小到大的顺序为 A<B<C<Y |
| B.A、B的氢化物的稳定性强弱为HA<HB |
| C.X、Y最高价氧化物对应水化物的酸性由弱到强的顺序为H2YO3<H2XO3 |
| D.B、C简单离子的还原性由弱到强的顺序为B<C |
您最近一年使用:0次
名校
解题方法
3 . 某同学在实验室选用下列装置,验证碳和浓硫酸的反应产物,回答下列问题:
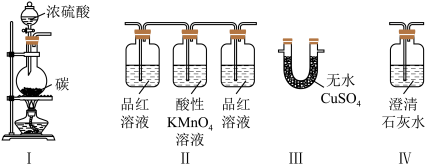
(1)盛放浓硫酸的仪器名称为______ ;写出碳与浓硫酸反应的化学方程式_______ 。
(2)验证产物的正确连接顺序为________ 。
(3)装置Ⅱ中左侧和右侧品红溶液的作用分别是________ 、________ 。
(4)装置Ⅲ的现象是_______ 。

(1)盛放浓硫酸的仪器名称为
(2)验证产物的正确连接顺序为
(3)装置Ⅱ中左侧和右侧品红溶液的作用分别是
(4)装置Ⅲ的现象是
您最近一年使用:0次
名校
4 . Ⅰ.在一定条件下A与B反应可生成C和D,其能量变化如图:

(1)若E1>E2,反应体系的总能量_______ (填“升高”或“降低”),为_______ (填“吸热”或“放热”)反应。原因是_______ 。
Ⅱ.2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(2)原电池反应能够提供电能而不产生CO2气体,如图是某原电池装置图。

①Zn棒是原电池的_______ 极,发生_______ (填“氧化”或“还原”)反应。
②Cu棒上发生的电极反应式为_______ 。
③溶液中H+向_______ (填“Zn”或“Cu”)电极定向移动。
(3)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是_______ (填“Zn”或“Cu”),正极的电极反应式为_______ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=_______ mol。
(4)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。该原电池电解质是KOH溶液,写出正极的电极反应_______ 。

(1)若E1>E2,反应体系的总能量
Ⅱ.2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(2)原电池反应能够提供电能而不产生CO2气体,如图是某原电池装置图。

①Zn棒是原电池的
②Cu棒上发生的电极反应式为
③溶液中H+向
(3)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(4)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。该原电池电解质是KOH溶液,写出正极的电极反应
您最近一年使用:0次
名校
5 . 有关如图流程的判断中正确的是
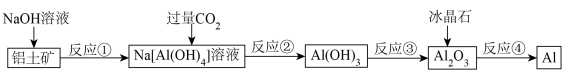

| A.流程中涉及的反应均为非氧化还原反应 |
B.反应②产生的阴离子主要为CO |
| C.实验室中完成反应③应在蒸发皿中进行 |
| D.反应①的离子方程式为Al2O3+2OH-+3H2O=2[Al(OH)4]- |
您最近一年使用:0次
6 . 把b中三个碎纸片补充到a中,可得到一个完整的离子方程式(未配平)。b中补充到a中的反应物是
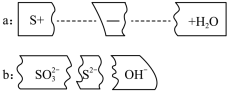

| A.S2- | B.SO | C.OH- | D.无法确定 |
您最近一年使用:0次
7 . Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为


A.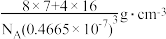 | B.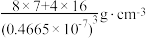 |
C.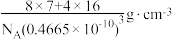 | D.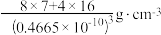 |
您最近一年使用:0次
名校
8 . 铜是人类最早发现并广泛使用的一种金属。黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)Cu的价电子排布式为___________ ,CuFeS2中三种元素的电负性从大到小的顺序为___________ (用元素符号表示)。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是___________ ,中心原子杂化类型为___________ 。
②X的沸点比水的沸点低,主要原因是___________ 。
(3)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有___________ (填标号)
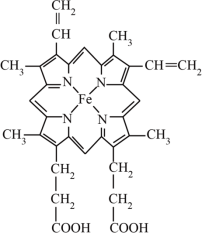
A.范德华力 B. 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键
(4)某镍白铜合金的立方晶胞结构如图所示:
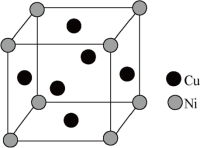
①晶胞中铜原子与镍原子的数目之比为___________ 。
②若该合金的晶胞边长为a nm,则该合金的密度为___________ g·cm-3(设NA为阿伏加德罗常数的值)
(1)Cu的价电子排布式为
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水的沸点低,主要原因是
(3)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有

A.范德华力 B.
 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键(4)某镍白铜合金的立方晶胞结构如图所示:

①晶胞中铜原子与镍原子的数目之比为
②若该合金的晶胞边长为a nm,则该合金的密度为
您最近一年使用:0次
名校
解题方法
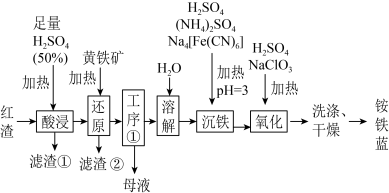
9 . 以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料生产制备铵铁蓝Fe(NH4)[Fe(CN)6]颜料的工艺流程如图:_______ (填化学式),滤渣①的主要成分是_______ (填化学式)。
(2)黄铁矿研细的目的是_______ 。
(3)工序①经过_______ 、过滤、洗涤得到一种含7个结晶水的晶体,该晶体为_______ (填化学式)。
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:_______ 。
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:_______ 。6Fe(NH4)2[Fe(CN)6]+ClO +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
(2)黄铁矿研细的目的是
(3)工序①经过
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:
 +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
您最近一年使用:0次
2024-03-01更新
|
92次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高一下学期化学试题
名校
解题方法
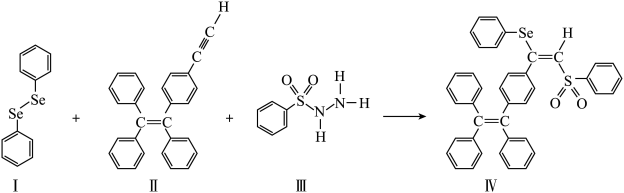
10 . 硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子N的合成路线如下:
(1)H2Se的沸点低于H2O,其原因是___________ 。
(2)关于I~Ⅲ三种反应物,下列说法正确的有___________ 。
A. I中仅有σ键 B. I中的 Se-Se为非极性共价键
C. Ⅱ易溶于水 D. Ⅱ中原子的杂化轨道类型只有sp与sp2
E. I~Ⅲ含有的元素中,O电负性最大
(3)Ⅳ中具有孤电子对的原子有___________ 。
(4)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为___________ 。
(5)吡啶(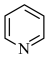 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大
大 键,则吡啶中N原子的价层孤电子对占据___________(填标号)。
键,则吡啶中N原子的价层孤电子对占据___________(填标号)。
(6)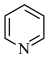 、
、 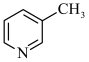 、
、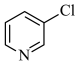 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是___________ 。

(1)H2Se的沸点低于H2O,其原因是
(2)关于I~Ⅲ三种反应物,下列说法正确的有
A. I中仅有σ键 B. I中的 Se-Se为非极性共价键
C. Ⅱ易溶于水 D. Ⅱ中原子的杂化轨道类型只有sp与sp2
E. I~Ⅲ含有的元素中,O电负性最大
(3)Ⅳ中具有孤电子对的原子有
(4)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒。
 的空间结构为
的空间结构为(5)吡啶(
 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大
大 键,则吡啶中N原子的价层孤电子对占据___________(填标号)。
键,则吡啶中N原子的价层孤电子对占据___________(填标号)。| A.2s轨道 | B.2p轨道 | C.sp杂化轨道 | D.sp2杂化轨道 |
(6)
 、
、  、
、 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
您最近一年使用:0次



