1 . 由下列实验操作和现象所得结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将亚硫酸钠样品溶于水,加入盐酸酸化的Ba(NO3)2溶液有白色沉淀产生 | 样品已变质 |
| B | 将盐酸滴入某溶液,产生能使澄清石灰水变浑浊的气体 | 溶液中有 |
| C | 铁投入冷的浓硝酸中无明显现象,投入稀硝酸中有气泡冒出 | 氧化性:稀硝酸>浓硝酸 |
| D | 向Na2SO3溶液中滴入稀盐酸,产生刺激性气味的气体可使品红溶液褪色 | 酸性:HCl>H2SO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-09更新
|
212次组卷
|
3卷引用:上海市复旦大学附属中学2022-2023学年高一下学期阶段测试化学试题
2 . 矾是一类含硫化合物,一般都含有氢、氧、硫等元素,在生活和生产中有着重要应用。
(1)硫元素在周期表中的位置是___________ ,与硫原子占有相同轨道数目的阳离子有___________ (用微粒符号表示)。
(2)从原子结构的角度解释硫元素的非金属性比氧弱的原因:___________ 。
(3)蓝矾(CuSO4•5H2O)常用于冶金、制农药等。实验室常用蓝矾溶液检验H2S气体,该反应的离子方程式为___________ 。
(4)绿矾(FeSO4•7H2O)水溶液显酸性,在空气中久置出现红褐色的Fe(OH)3沉淀,且溶液的酸性增强,该反应的离子方程式为___________ 。因此绿矾水溶液保存时防止变质可加入试剂为___________ (填化学式)。
(5)已知黄矾[FexS2O9•yH2O]中Fe、S的化合价分别为+3、+6,则x=___________ 。将2.500g样品加热到110℃时,样品失掉部分结晶水,恒重后的固体质量为2.320g;将样品继续高温加热至恒重,得到氧化铁0.800g。黄矾的化学式为___________ 。
(1)硫元素在周期表中的位置是
(2)从原子结构的角度解释硫元素的非金属性比氧弱的原因:
(3)蓝矾(CuSO4•5H2O)常用于冶金、制农药等。实验室常用蓝矾溶液检验H2S气体,该反应的离子方程式为
(4)绿矾(FeSO4•7H2O)水溶液显酸性,在空气中久置出现红褐色的Fe(OH)3沉淀,且溶液的酸性增强,该反应的离子方程式为
(5)已知黄矾[FexS2O9•yH2O]中Fe、S的化合价分别为+3、+6,则x=
您最近一年使用:0次
名校
3 . 有一 固体样品因保存时间较长,部分被氧化而变质了。
固体样品因保存时间较长,部分被氧化而变质了。
(1) 溶液呈
溶液呈_____ 性(选填“酸”“碱”“中”),在 溶液中加少量
溶液中加少量_____ 可以使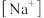 与
与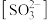 比值接近
比值接近 ;
;
(2)在 的
的 溶液中,下列关系式正确的有
溶液中,下列关系式正确的有_____
a.
b.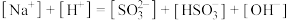
c.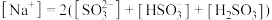
d.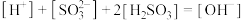
(3) 在空气中变质的原因是
在空气中变质的原因是_____ (用化学术语表示)。
为测定样品纯度,甲、乙两位同学分别分别进行了设计和思考:
【甲同学】:称取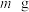 样品溶于水,加入过量稀盐酸,再加入过量的
样品溶于水,加入过量稀盐酸,再加入过量的 溶液。过滤,将滤渣洗涤后进行烘干,冷却后称得质量为
溶液。过滤,将滤渣洗涤后进行烘干,冷却后称得质量为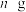 。
。
(4) 溶液必须过量的原因是
溶液必须过量的原因是_____ 。检验 溶液足量的方法是
溶液足量的方法是_____ 。
(5)甲同学实验测得亚硫酸钠的纯度是_____ 。
【乙同学】查阅资料发现,亚硫酸钠溶液与高锰酸钾溶液可以快速反应:
 (未配平)
(未配平)
乙同学计划称取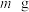 样品于锥形瓶中加适量水溶解,配成溶液,将浓度为
样品于锥形瓶中加适量水溶解,配成溶液,将浓度为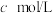 的酸性高锰酸钾溶液滴入到该试液至恰好反应时,消耗高锰酸钾溶液
的酸性高锰酸钾溶液滴入到该试液至恰好反应时,消耗高锰酸钾溶液 。
。
(6)滴入最后一滴 溶液时,锥形瓶中
溶液时,锥形瓶中_____ (现象)表示恰好完全反应。
(7)乙同学实验测得亚硫酸钠的纯度是_____ 。
 固体样品因保存时间较长,部分被氧化而变质了。
固体样品因保存时间较长,部分被氧化而变质了。(1)
 溶液呈
溶液呈 溶液中加少量
溶液中加少量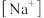 与
与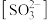 比值接近
比值接近 ;
;(2)在
 的
的 溶液中,下列关系式正确的有
溶液中,下列关系式正确的有a.

b.
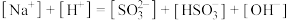
c.
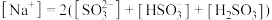
d.
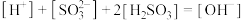
(3)
 在空气中变质的原因是
在空气中变质的原因是为测定样品纯度,甲、乙两位同学分别分别进行了设计和思考:
【甲同学】:称取
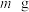 样品溶于水,加入过量稀盐酸,再加入过量的
样品溶于水,加入过量稀盐酸,再加入过量的 溶液。过滤,将滤渣洗涤后进行烘干,冷却后称得质量为
溶液。过滤,将滤渣洗涤后进行烘干,冷却后称得质量为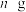 。
。(4)
 溶液必须过量的原因是
溶液必须过量的原因是 溶液足量的方法是
溶液足量的方法是(5)甲同学实验测得亚硫酸钠的纯度是
【乙同学】查阅资料发现,亚硫酸钠溶液与高锰酸钾溶液可以快速反应:
 (未配平)
(未配平)乙同学计划称取
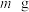 样品于锥形瓶中加适量水溶解,配成溶液,将浓度为
样品于锥形瓶中加适量水溶解,配成溶液,将浓度为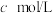 的酸性高锰酸钾溶液滴入到该试液至恰好反应时,消耗高锰酸钾溶液
的酸性高锰酸钾溶液滴入到该试液至恰好反应时,消耗高锰酸钾溶液 。
。(6)滴入最后一滴
 溶液时,锥形瓶中
溶液时,锥形瓶中(7)乙同学实验测得亚硫酸钠的纯度是
您最近一年使用:0次
名校
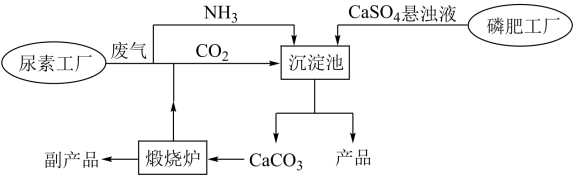
4 . “绿色化学”是化工生产中的重要理念。下图为利用尿素工厂废气以及磷肥工厂废渣(液)联合生产硫酸铵的工艺流程。
完成下列填空:
(1)沉淀池中发生反应的化学方程式为___________ 。已知硫酸铵溶解度变化趋势与氯化钠相似,则从沉淀池中获得产品的操作包含___________ 、___________ 、洗涤、烘干等。
(2)流程中体现“绿色化学”理念的设计有___________ 、___________ 等。
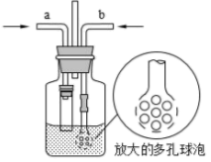
(3)为在实验室模拟沉淀池中的反应,设计了如图所示的装置,导管a下端连接粗管的目的是___________ ;导管b下端使用多孔球泡的目的是___________ 。
可用甲醛法测定所得 样品中氮的质量分数。其反应原理可以表示为:
样品中氮的质量分数。其反应原理可以表示为:
 [已知:
[已知: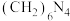 不与NaOH反应]
不与NaOH反应]
实验过程:称取样品1.500g,溶解配制成250mL溶液,取25.00mL样品溶液于锥形瓶中,加入过量的甲醛溶液,摇匀、静置5min后,加入1~2滴甲基橙试液,用NaOH标准溶液滴定至终点。
(4)终点的判断依据是___________ 。
(5)已知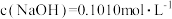 ,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为
,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为___________ 。(保留4位小数),实验测得硫酸铵样品中氮的质量分数略高,原因可能是___________ 。
a.甲醛被氧化 b.没有进行平行实验
c.氢氧化钠溶液久置变质 d.锥形瓶没有用待测液润洗

完成下列填空:
(1)沉淀池中发生反应的化学方程式为
(2)流程中体现“绿色化学”理念的设计有
(3)为在实验室模拟沉淀池中的反应,设计了如图所示的装置,导管a下端连接粗管的目的是

可用甲醛法测定所得
 样品中氮的质量分数。其反应原理可以表示为:
样品中氮的质量分数。其反应原理可以表示为: [已知:
[已知: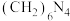 不与NaOH反应]
不与NaOH反应]实验过程:称取样品1.500g,溶解配制成250mL溶液,取25.00mL样品溶液于锥形瓶中,加入过量的甲醛溶液,摇匀、静置5min后,加入1~2滴甲基橙试液,用NaOH标准溶液滴定至终点。
(4)终点的判断依据是
(5)已知
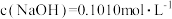 ,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为
,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为a.甲醛被氧化 b.没有进行平行实验
c.氢氧化钠溶液久置变质 d.锥形瓶没有用待测液润洗
您最近一年使用:0次
2021-04-20更新
|
352次组卷
|
4卷引用:上海市浦东新区2021届高三二模化学试题
上海市浦东新区2021届高三二模化学试题上海市宝山区行知中学-2021-2022学年高三下学期3月月考化学试题(已下线)化学-2022年高考押题预测卷02(上海卷)(含考试版、全解全析、参考答案、答题卡)(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)
名校
解题方法
5 . 有一Na2SO3固体样品因保存时间较长,部分被氧化而变质了。
(1)Na2SO3溶液呈________ 性(选填“酸”、“碱”、“中”),在Na2SO3溶液中加少量________ 可以使[Na+]与[ ]比值接近2:1。
]比值接近2:1。
(2)在0.1mol/L的Na2SO3溶液中,下列关系式正确的有___________ 。
a.[Na+]>[ ]>[
]>[ ]>[OH-]>[H+] b.[Na+]+[H+]=[
]>[OH-]>[H+] b.[Na+]+[H+]=[ ]+[
]+[ ]+[OH-]
]+[OH-]
c.[Na+]= [ ]+[
]+[ ]+[H2SO3] d.[H+]+[
]+[H2SO3] d.[H+]+[ ]=[
]=[ ]+[OH-]
]+[OH-]
(3)Na2SO3在空气中变质的原因是________ (用化学方程式表示)。
为测定样品纯度,甲、乙两位同学分别分别进行了设计和思考:
【甲同学】:称取m g样品溶于水,加入过量稀盐酸,再加入过量的BaCl2溶液。过滤,将滤渣洗涤后进行烘干,冷却后称得质量为n g。
(4)BaCl2溶液必须过量的原因是_______ 。检验BaCl2溶液足量的方法是______ 。
(5)甲同学实验测得亚硫酸钠的纯度是______ 。
【乙同学】:称取a g样品溶于250mL水中,并取出25mL,用浓度为b mol/L的酸性高锰酸钾溶液滴定至终点,消耗酸性高锰酸钾溶液V mL。
(6)滴定终点的现象是______ 。
(7)乙同学实验测得亚硫酸钠的纯度是______ 。
(1)Na2SO3溶液呈
 ]比值接近2:1。
]比值接近2:1。(2)在0.1mol/L的Na2SO3溶液中,下列关系式正确的有
a.[Na+]>[
 ]>[
]>[ ]>[OH-]>[H+] b.[Na+]+[H+]=[
]>[OH-]>[H+] b.[Na+]+[H+]=[ ]+[
]+[ ]+[OH-]
]+[OH-]c.[Na+]= [
 ]+[
]+[ ]+[H2SO3] d.[H+]+[
]+[H2SO3] d.[H+]+[ ]=[
]=[ ]+[OH-]
]+[OH-](3)Na2SO3在空气中变质的原因是
为测定样品纯度,甲、乙两位同学分别分别进行了设计和思考:
【甲同学】:称取m g样品溶于水,加入过量稀盐酸,再加入过量的BaCl2溶液。过滤,将滤渣洗涤后进行烘干,冷却后称得质量为n g。
(4)BaCl2溶液必须过量的原因是
(5)甲同学实验测得亚硫酸钠的纯度是
【乙同学】:称取a g样品溶于250mL水中,并取出25mL,用浓度为b mol/L的酸性高锰酸钾溶液滴定至终点,消耗酸性高锰酸钾溶液V mL。
(6)滴定终点的现象是
(7)乙同学实验测得亚硫酸钠的纯度是
您最近一年使用:0次
6 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由实验现象可推知:____________ 。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①将补全下列实验操作步骤正确排序da_____ e(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
②缓缓通入N2的目的是_________ 。
③根据实验记录,计算绿矾化学式中结晶水数目x=_________ (列式表示)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A(取出a g后)接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为BaCl2、品红。C、D中可观察到的现象分别为________ 、________ 。
②写出硫酸亚铁高温分解反应的化学方程式________ 。
(4)为了测定A中样品的纯度,将取出a g样品溶于水,配制成500 mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00 mL,实验结果记录如下:
上表中第一次实验中记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由实验现象可推知:
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①将补全下列实验操作步骤正确排序da
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
②缓缓通入N2的目的是
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A(取出a g后)接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为BaCl2、品红。C、D中可观察到的现象分别为
②写出硫酸亚铁高温分解反应的化学方程式
(4)为了测定A中样品的纯度,将取出a g样品溶于水,配制成500 mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00 mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
您最近一年使用:0次
2020-12-29更新
|
429次组卷
|
2卷引用:上海市嘉定区2021届高三一模化学试题
12-13高三上·上海浦东新·期中
名校
7 . 有一Na2SO3固体因部分被氧化而变质。为测定样品纯度,甲、乙两位同学分别设计了如下实验方案:
【甲同学】称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是_________________________________ 。
(2)洗涤残留固体的方法是_________________________________________ 。
(3)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是__________________________________ 。
【乙同学】称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+(未配平)
(4)配制样品溶液时,不一定需要的实验仪器是_________ (错选扣分)。
A.容量瓶 B.玻璃棒 C.滴定管 D.烧杯
(5)滴定终点的判断依据是____________________________________ 。
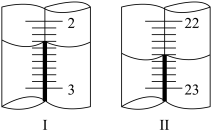
(6)滴定管液面变化如图所示,图Ⅰ显示初读数为___________ mL,根据图Ⅱ所示末读数,可得样品纯度计算式为___________________ 。(缺少的数据用A代替,数量级与本题一致)
【甲同学】称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是
(2)洗涤残留固体的方法是
(3)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是
【乙同学】称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+(未配平)
(4)配制样品溶液时,不一定需要的实验仪器是
A.容量瓶 B.玻璃棒 C.滴定管 D.烧杯
(5)滴定终点的判断依据是

(6)滴定管液面变化如图所示,图Ⅰ显示初读数为
您最近一年使用:0次
8 . 亚硫酸钠固体久置变质,部分生成硫酸钠。取a g亚硫酸钠样品,依照如图装置实验,分析样品纯度(质量分数)。
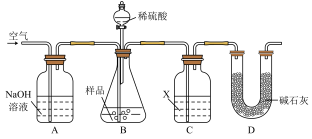
(1)在C瓶试剂X的选择上,甲同学认为使用足量的Ba(OH)2溶液比足量的Ca(OH)2溶液更合适,理由是______________________ 。
(2)实验操作步骤如下:(X采用甲同学意见)。
①先在A、B中通一段时间空气,再接上C、D;
②加稀硫酸反应;
③反应结束,通空气足够时间。该操作的目的是________________ ;
④将C中物质过滤、洗涤、干燥、称重,得b g固体。以此计算,亚硫酸钠样品纯度为_____________ 。
(3)乙同学指出,上述操作实验结果偏大,原因是(用化学反应方程式表示)_____ ;改进的措施是__________________ 。
(4)依据乙同学意见改进方案后,乙同学又提出也可以通过称量C装置前后的质量差来分析结果。丙同学指出如此操作,实验结果将偏小,原因是_______________ 。
(5)丙同学认为若以称重前后差量来分析,可称量D装置,并从以下3方面调整:
①将C瓶试剂X换为______________ 。
②在D装置后可以接________ (填选项编号)。
a. 装有无水氯化钙的干燥管 b. 装有碱石灰的干燥管
c. 装有浓硫酸的洗气瓶 d. 装有氢氧化钠溶液的洗气瓶
③先在C之前(含C)的装置中通一段时间气体,再接上D及之后的装置。

(1)在C瓶试剂X的选择上,甲同学认为使用足量的Ba(OH)2溶液比足量的Ca(OH)2溶液更合适,理由是
(2)实验操作步骤如下:(X采用甲同学意见)。
①先在A、B中通一段时间空气,再接上C、D;
②加稀硫酸反应;
③反应结束,通空气足够时间。该操作的目的是
④将C中物质过滤、洗涤、干燥、称重,得b g固体。以此计算,亚硫酸钠样品纯度为
(3)乙同学指出,上述操作实验结果偏大,原因是(用化学反应方程式表示)
(4)依据乙同学意见改进方案后,乙同学又提出也可以通过称量C装置前后的质量差来分析结果。丙同学指出如此操作,实验结果将偏小,原因是
(5)丙同学认为若以称重前后差量来分析,可称量D装置,并从以下3方面调整:
①将C瓶试剂X换为
②在D装置后可以接
a. 装有无水氯化钙的干燥管 b. 装有碱石灰的干燥管
c. 装有浓硫酸的洗气瓶 d. 装有氢氧化钠溶液的洗气瓶
③先在C之前(含C)的装置中通一段时间气体,再接上D及之后的装置。
您最近一年使用:0次
解题方法
9 . 有一Na2SO3固体因部分被氧化而变质。为测定样品纯度,甲、乙两位同学分别设计了如下实验方案:
【甲同学】称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是___________________________________________ 。在滤液中滴加____________ 溶液,若没有白色沉淀生成,则证明BaCl2溶液不足,还需继续在滤液中加入BaCl2溶液后进行过滤。洗涤残留固体的方法是__________________________________________________ ;在洗出液中滴加_______________ 溶液,可以判断残留固体是否洗涤干净。
(2)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是_________________________________________________________ 。
【乙同学】称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+ (未配平)
(3)配制样品溶液时,不一定 需要的实验仪器是__________ (选填答案编号)。
a.容量瓶 b.玻璃棒 c.滴定管 d.烧杯
(4)滴定终点的判断依据是___________________________________________________ 。
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用__________________________________________ 。滴定管液面变化如图所示,从图Ⅰ图Ⅱ显示消耗的高锰酸钾溶液体积为__________________ 。
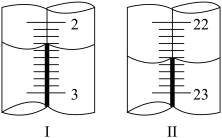
【甲同学】称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是
(2)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是
【乙同学】称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+ (未配平)
(3)配制样品溶液时,
a.容量瓶 b.玻璃棒 c.滴定管 d.烧杯
(4)滴定终点的判断依据是
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用

您最近一年使用:0次
10-11高三上·上海浦东新·期末
10 . 已知NaHCO3在潮湿的空气中会缓慢分解。取没有妥善保管已部分变质的NaHCO3样品a g,溶于水配成溶液,慢慢滴入0.200mol/L稀盐酸并不停地搅拌,反应过程中测得溶液中NaHCO3的质量与加入盐酸的体积之间的关系如图所示。
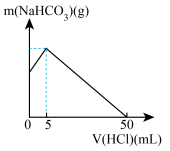
(1)a g样品中含Na2CO3的质量为____________ g。
(2)a g样品未变质前NaHCO3的质量为________ g。
(3)若另取样品b g,充分加热以后得到固体质量为5.300g,则b=_____________ g。

(1)a g样品中含Na2CO3的质量为
(2)a g样品未变质前NaHCO3的质量为
(3)若另取样品b g,充分加热以后得到固体质量为5.300g,则b=
您最近一年使用:0次



