解题方法
1 . 一种用 浴液浸取黄铁矿(主要含
浴液浸取黄铁矿(主要含 和少量难溶杂质)的流程如图所示。下列说法正确的是
和少量难溶杂质)的流程如图所示。下列说法正确的是

 浴液浸取黄铁矿(主要含
浴液浸取黄铁矿(主要含 和少量难溶杂质)的流程如图所示。下列说法正确的是
和少量难溶杂质)的流程如图所示。下列说法正确的是
A. 晶体中含有离子键和共价键,阴阳离子个数比为 晶体中含有离子键和共价键,阴阳离子个数比为 |
B.浸取时,若生成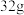 硫,则转移电子数为 硫,则转移电子数为 |
C.配制 溶液需要用到硫酸溶液和蒸馏水 溶液需要用到硫酸溶液和蒸馏水 |
D.向溶液X中先通 再滴加 再滴加 溶液,可检验是否有 溶液,可检验是否有 |
您最近一年使用:0次
名校
2 . 完成下列问题。
(1)将下列化学方程式配平___________ 。
_______KI+_______H2SO4=_______I2+______H2S+______KHSO4+______H2O
(2)反应8NH3+3Cl2=6NH4Cl+N2中氧化剂与还原剂的质量之比为___________ 。
(3)已知:酸性环境中,Fe2+被 氧化,生成Fe3+和NO气体,请写出对应的离子方程式:
氧化,生成Fe3+和NO气体,请写出对应的离子方程式:_______ ;
(4)R2O 离子在一定条件下可以把Mn2+离子氧化为
离子在一定条件下可以把Mn2+离子氧化为 若反应后R2O
若反应后R2O 离子变为RO
离子变为RO 离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为
离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为___________ ,R2O 中R的化合价是
中R的化合价是___________ 价。
(5)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有300gFeS2参加反应时,被氧化的硫元素的质量为___________ g。
(1)将下列化学方程式配平
_______KI+_______H2SO4=_______I2+______H2S+______KHSO4+______H2O
(2)反应8NH3+3Cl2=6NH4Cl+N2中氧化剂与还原剂的质量之比为
(3)已知:酸性环境中,Fe2+被
 氧化,生成Fe3+和NO气体,请写出对应的离子方程式:
氧化,生成Fe3+和NO气体,请写出对应的离子方程式:(4)R2O
 离子在一定条件下可以把Mn2+离子氧化为
离子在一定条件下可以把Mn2+离子氧化为 若反应后R2O
若反应后R2O 离子变为RO
离子变为RO 离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为
离子,又知反应中氧化剂和还原剂的个数之比为5:2,则n值为 中R的化合价是
中R的化合价是(5)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有300gFeS2参加反应时,被氧化的硫元素的质量为
您最近一年使用:0次
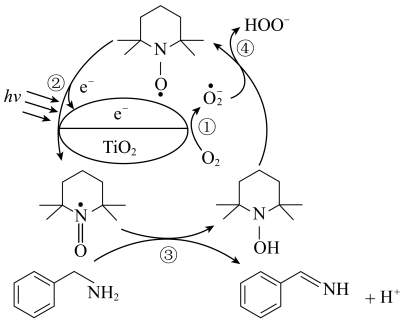
3 . 纳米TiO2是一种重要的光催化剂,其催化苯甲胺(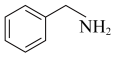 )生成苯甲亚胺(
)生成苯甲亚胺(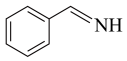 )的机理如图所示。下列说法不正确的是
)的机理如图所示。下列说法不正确的是
 )生成苯甲亚胺(
)生成苯甲亚胺( )的机理如图所示。下列说法不正确的是
)的机理如图所示。下列说法不正确的是
| A.HOO-具有氧化性 |
| B.O2在TiO2表面捕获电子 |
| C.反应③涉及π键的断裂和生成 |
D.总反应为2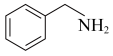 +O2→2 +O2→2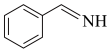 +2H2O +2H2O |
您最近一年使用:0次
2023-09-14更新
|
188次组卷
|
2卷引用:湖北省高中名校联盟2024届高三第一次联合测评化学试题
名校
4 . 废SCR催化剂(含TO2、V2O5、WO3等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
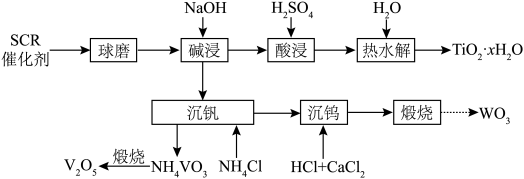
已知:①TO2、V2O5和WO3都能与NaOH溶液反应生成可溶性的NaVO3、Na2WO4和不溶性的Na2TiO3;
②Ksp(CaWO4)=9×10-9。
回答下列问题:
(1)基态23V原子的价层电子轨道表示式为___________ 。
(2)“球磨”的目的是___________ 。
(3)“碱浸”后通过___________ (填操作名称)可以实现钛与钒、钨分离。
(4)“酸浸”后钛主要以TO2+形式存在,“热水解”反应的离子方程式为___________ 。
(5)“煅烧”NH4VO3的化学方程式为___________ 。
(6)“沉钨”中析出CaWO4时,需要加入过量CaCl2,其目的是___________ 。
(7)向20mL0.3mol/LNa2WO4的滤液中加入等体积的CaCl2溶液(忽略混合过程中的体积变化),欲使WO 浓度小于1×10-6mol/L,则CaCl2溶液的最小浓度为
浓度小于1×10-6mol/L,则CaCl2溶液的最小浓度为___________ mol/L。

已知:①TO2、V2O5和WO3都能与NaOH溶液反应生成可溶性的NaVO3、Na2WO4和不溶性的Na2TiO3;
②Ksp(CaWO4)=9×10-9。
回答下列问题:
(1)基态23V原子的价层电子轨道表示式为
(2)“球磨”的目的是
(3)“碱浸”后通过
(4)“酸浸”后钛主要以TO2+形式存在,“热水解”反应的离子方程式为
(5)“煅烧”NH4VO3的化学方程式为
(6)“沉钨”中析出CaWO4时,需要加入过量CaCl2,其目的是
(7)向20mL0.3mol/LNa2WO4的滤液中加入等体积的CaCl2溶液(忽略混合过程中的体积变化),欲使WO
 浓度小于1×10-6mol/L,则CaCl2溶液的最小浓度为
浓度小于1×10-6mol/L,则CaCl2溶液的最小浓度为
您最近一年使用:0次
5 . 乙醇在一定条件下可以转化为乙醛,乙醛可进一步被氧化成乙酸。某兴趣小组进行两组实验探究,实验装置如下图所示(装置气密性已检查)。
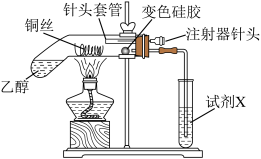
已知:变色硅胶吸收水分后会由蓝色变成粉红色。
实验Ⅰ:通过注射器针头鼓入空气的条件下进行实验。
(1)乙醛中官能团的结构简式为_______ ,下列可用于检验该官能团的试剂是_______ (填字母选项)。
a.银氨溶液 b. 溶液 c.
溶液 c. -淀粉溶液
-淀粉溶液
(2)开始实验时先加热铜网,再通过注射器针头缓慢鼓入空气,该过程中铜丝产生实验现象为_______ ,同时变色硅胶由蓝色变成粉红色,写出乙醇催化氧化的化学反应方程式_______ 。
(3)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是_______ (填“吸热”或“放热”)反应。
(4)为检验上述实验收集的产物,该小组同学继续进行如下实验并得出相应结论。
实验①~③中的结论不合理的是_______ (填序号),原因是_______ 。
实验Ⅱ:在没有鼓入空气的条件下进行实验。
(5)乙醇蒸气能发生催化氧化生成乙醛,变色硅胶不变色,则该反应的化学方程式为_______ 。

已知:变色硅胶吸收水分后会由蓝色变成粉红色。
实验Ⅰ:通过注射器针头鼓入空气的条件下进行实验。
(1)乙醛中官能团的结构简式为
a.银氨溶液 b.
 溶液 c.
溶液 c. -淀粉溶液
-淀粉溶液(2)开始实验时先加热铜网,再通过注射器针头缓慢鼓入空气,该过程中铜丝产生实验现象为
(3)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是
(4)为检验上述实验收集的产物,该小组同学继续进行如下实验并得出相应结论。
| 实验序号 | 试剂 和反应条件 和反应条件 | 现象 | 结论 |
| ① | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| ② | 新制氢氧化铜悬浊液,加热 | 生成砖红色沉淀 | 产物含有乙醛 |
| ③ | 含酚酞的 溶液 溶液 | 浅红色褪去 | 产物可能含有乙酸 |
实验Ⅱ:在没有鼓入空气的条件下进行实验。
(5)乙醇蒸气能发生催化氧化生成乙醛,变色硅胶不变色,则该反应的化学方程式为
您最近一年使用:0次
名校
6 .  催化剂能催化
催化剂能催化 脱除烟气中的
脱除烟气中的 ,反应为
,反应为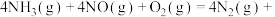
 ,其机理如图所示。下列说法正确的是
,其机理如图所示。下列说法正确的是

 催化剂能催化
催化剂能催化 脱除烟气中的
脱除烟气中的 ,反应为
,反应为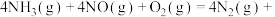
 ,其机理如图所示。下列说法正确的是
,其机理如图所示。下列说法正确的是
A.该反应 |
B.该反应的平衡常数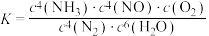 |
C.步骤Ⅰ可描述为 吸附到 吸附到 表面与表面吸附氧反应生成 表面与表面吸附氧反应生成 和 和 ,同时 ,同时 被还原为 被还原为 ;烟气中的 ;烟气中的 和 和 反应生成 反应生成 和 和 |
D.该反应中每消耗1  ,转移电子的数目约为 ,转移电子的数目约为 |
您最近一年使用:0次
2023-09-02更新
|
270次组卷
|
3卷引用:选择题1-5
23-24高三上·北京西城·开学考试
名校
解题方法
7 . 已知:A、B、C为中学常见的单质,A为淡黄色固体;D、E、F为中学常见的氧化物,E是具有磁性的黑色晶体;H、K为中学常见的盐;M为一种常见的无色液体。各物质间的转化关系如图所示(某些条件已略去)。

请回答:
(1)生成F的化学方程式_________ 。
(2)物质K的化学式为________ 。
(3)D可使酸性KMnO4溶液褪色,体现了D物质的________ (填字母序号)。
A.氧化性 B.还原性 C.漂白性
(4)C与M在一定条件下反应的化学方程式为_________ 。
(5)先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为________ 。
(6)H溶液在空气中长期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因:________ 。

请回答:
(1)生成F的化学方程式
(2)物质K的化学式为
(3)D可使酸性KMnO4溶液褪色,体现了D物质的
A.氧化性 B.还原性 C.漂白性
(4)C与M在一定条件下反应的化学方程式为
(5)先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为
(6)H溶液在空气中长期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因:
您最近一年使用:0次
名校
8 . 镍铼高温合金可用于制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴。NH4ReO4是制备高纯度Re的原料。实验室制备NH4ReO4的装置如图所示。
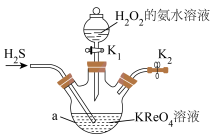
已知: Ⅰ.KReO4、与H2S反应生成Re2Sn7;
Ⅱ.2NH4ReO4+7H2=2Re+ 2NH3 + 8H2O。
有关物质的溶解度S见下表:
回答下列问题:
(1)金属铼具有良好的导电、导热性和延展性,可用于解释这--现象的理论是_______________ 。
(2)仪器a的名称是__________ 。
(3)反应开始前先向仪器a中加入一定量的KReO4溶液,再通入一定量的H2S,反应一段时间,仪器a内生成Re2S7,然后滴入足量的H2O2的氨水溶液,生成NH4ReO4,同时有硫酸铵生成;写出生成NH4ReO4的化学方程式:_____ ,反应结束后从溶液中分离出NH4ReO4的方法是_______ 。
(4)氢气还原NH4ReO4制备金属铼时,在加热前,需先通入一段时间的氢气,其目的是_____ 。实验室制取氢气时,常用粗锌粒而不用纯锌,其原因是___ 。

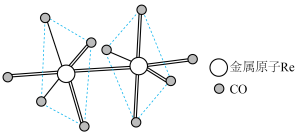
(5)铼可形成多种配位化合物, Re2 (CO)10就是其中的一种,其结构如图,其中配位原子为_______ (填“C"或“O")。

已知: Ⅰ.KReO4、与H2S反应生成Re2Sn7;
Ⅱ.2NH4ReO4+7H2=2Re+ 2NH3 + 8H2O。
有关物质的溶解度S见下表:
| 温度/℃ | S[(NH4)2SO4]/g | S[NH4ReO4]/g |
| 20 | 75.4 | 6.1 |
| 30 | 78.0 | 32.3 |
(1)金属铼具有良好的导电、导热性和延展性,可用于解释这--现象的理论是
(2)仪器a的名称是
(3)反应开始前先向仪器a中加入一定量的KReO4溶液,再通入一定量的H2S,反应一段时间,仪器a内生成Re2S7,然后滴入足量的H2O2的氨水溶液,生成NH4ReO4,同时有硫酸铵生成;写出生成NH4ReO4的化学方程式:
(4)氢气还原NH4ReO4制备金属铼时,在加热前,需先通入一段时间的氢气,其目的是

(5)铼可形成多种配位化合物, Re2 (CO)10就是其中的一种,其结构如图,其中配位原子为

您最近一年使用:0次
2023-08-20更新
|
161次组卷
|
2卷引用:湖北省部分学校2024届高三上学期8月起点考试化学试题
真题
解题方法
9 . 铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱石(主要化学成分为( ,还含有一定量的FeO和
,还含有一定量的FeO和 )生产BeO的一种工艺流程如下。
)生产BeO的一种工艺流程如下。
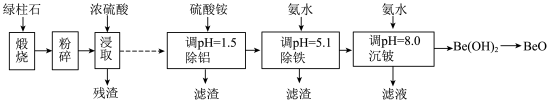
回答问题:
(1) 中Be的化合价为
中Be的化合价为_______ 。
(2)粉碎的目的是_______ ;残渣主要成分是_______ (填化学式)。
(3)该流程中能循环使用的物质是_______ (填化学式)。
(4)无水 可用作聚合反应的催化剂。BeO、
可用作聚合反应的催化剂。BeO、 与足量C在600~800℃制备
与足量C在600~800℃制备 的化学方程式为
的化学方程式为_______ 。
(5)沉铍时,将pH从8.0提高到8.5,则铍的损失降低至原来的_______ %。
 ,还含有一定量的FeO和
,还含有一定量的FeO和 )生产BeO的一种工艺流程如下。
)生产BeO的一种工艺流程如下。
回答问题:
(1)
 中Be的化合价为
中Be的化合价为(2)粉碎的目的是
(3)该流程中能循环使用的物质是
(4)无水
 可用作聚合反应的催化剂。BeO、
可用作聚合反应的催化剂。BeO、 与足量C在600~800℃制备
与足量C在600~800℃制备 的化学方程式为
的化学方程式为(5)沉铍时,将pH从8.0提高到8.5,则铍的损失降低至原来的
您最近一年使用:0次
解题方法
10 . 采用水合肼( )还原法制取碘化钠固体,其制备流程如图所示,已知:“合成”步骤中生成的副产物为
)还原法制取碘化钠固体,其制备流程如图所示,已知:“合成”步骤中生成的副产物为 。
。

下列说法中不正确的是
 )还原法制取碘化钠固体,其制备流程如图所示,已知:“合成”步骤中生成的副产物为
)还原法制取碘化钠固体,其制备流程如图所示,已知:“合成”步骤中生成的副产物为 。
。
下列说法中不正确的是
A.“合成”过程所得溶液中主要含有 、 、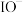 、 、 和 和 |
B.“还原”过程消耗 的离子方程式为 的离子方程式为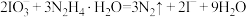 |
C.“水合肼还原法”的优点是 被氧化后的产物为 被氧化后的产物为 和 和 ,不引入杂质 ,不引入杂质 |
D.工业上常用铁屑还原 制备NaI,理论上该反应中氧化剂与还原剂的物质的量之比为1:2 制备NaI,理论上该反应中氧化剂与还原剂的物质的量之比为1:2 |
您最近一年使用:0次



