名校
1 . 氧化还原反应在日常生活、工农业生产和科学技术中应用广泛。
(1)对于反应 +3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+,其中被还原的元素是
+3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+,其中被还原的元素是___________ ,还原剂是___________ ,还原产物是___________ 。
(2)某实验兴趣小组根据氧化还原反应相关知识。探究 、
、 、
、 三者的氧化性强弱,设计实验装置如图。
三者的氧化性强弱,设计实验装置如图。

①实验Ⅰ的现象是___________ ;实验Ⅱ的现象是 ___________ 。
②实验Ⅱ发生反应的离子方程式为___________ 。
③综合实验Ⅰ和实验Ⅱ的现象及氧化还原反应的理论知识,可推测出 、
、 、
、 三者的氧化性由强到弱的顺序为
三者的氧化性由强到弱的顺序为 ___________ 。
(3)水是生命之源,是工业的血液,是农业的命脉。在下列反应中,水的作用是什么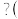 若水是反应物,则从
若水是反应物,则从 、
、 、
、 、
、 中选择
中选择 若水是生成物,则从
若水是生成物,则从 、
、 、
、 、
、 中选择
中选择
A.氧化剂 B.还原剂 C.既是氧化剂,又是还原剂 D.既不是氧化剂又不是还原剂
E.氧化产物 F.还原产物 G.既是氧化产物,又是还原产物
H.既不是氧化产物,又不是还原产物
①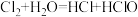 水的作用是
水的作用是___________ ;
②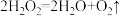 水的作用是
水的作用是___________
③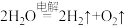 水的作用是
水的作用是___________ ;
④ 水的作用是
水的作用是___________ ;
⑤ 水的作用是
水的作用是___________ 。
(1)对于反应
 +3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+,其中被还原的元素是
+3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+,其中被还原的元素是(2)某实验兴趣小组根据氧化还原反应相关知识。探究
 、
、 、
、 三者的氧化性强弱,设计实验装置如图。
三者的氧化性强弱,设计实验装置如图。
①实验Ⅰ的现象是
②实验Ⅱ发生反应的离子方程式为
③综合实验Ⅰ和实验Ⅱ的现象及氧化还原反应的理论知识,可推测出
 、
、 、
、 三者的氧化性由强到弱的顺序为
三者的氧化性由强到弱的顺序为 (3)水是生命之源,是工业的血液,是农业的命脉。在下列反应中,水的作用是什么
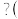 若水是反应物,则从
若水是反应物,则从 、
、 、
、 、
、 中选择
中选择 若水是生成物,则从
若水是生成物,则从 、
、 、
、 、
、 中选择
中选择
A.氧化剂 B.还原剂 C.既是氧化剂,又是还原剂 D.既不是氧化剂又不是还原剂
E.氧化产物 F.还原产物 G.既是氧化产物,又是还原产物
H.既不是氧化产物,又不是还原产物
①
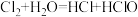 水的作用是
水的作用是②
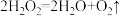 水的作用是
水的作用是③
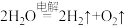 水的作用是
水的作用是④
 水的作用是
水的作用是⑤
 水的作用是
水的作用是
您最近一年使用:0次
名校
2 . 我国学者制备了一种介孔二氧化锰负载的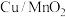 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是

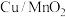 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
,BZA)的无污染降解中,催化机理如下图(部分产物已省略):下列说法错误的是
| A.BZA中既含有极性键又含有非极性键 |
B.反应中氧化剂为 ,氧化产物为 ,氧化产物为 和 和 |
C.直接降解BZA的活性氧物种的化学式为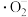 和 和 |
D.据机理图可知氧化性: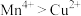 |
您最近一年使用:0次
2023-10-25更新
|
124次组卷
|
2卷引用:云南省昆明市云南民族大学附属高级中学2023-2024学年高三上学期第一次月考理综化学试题
3 . 氧化还原反应原理在生产、生活中应用广泛.
(1)下列反应中不涉及氧化还原反应的是____________(填序号).
(2)缺铁性贫血患者在服用补铁药片时,与维生素C同服效果更佳,因为维生素C可以将不易吸收的 转化为
转化为 .该过程中维生素C表现出的性质与下列____________(填序号)反应中
.该过程中维生素C表现出的性质与下列____________(填序号)反应中 表现出的性质相同.
表现出的性质相同.
(3)已知实验室制取 的反应:
的反应: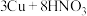 (稀)
(稀) ,该反应的离子方程式为
,该反应的离子方程式为____________________________________________________ ,硝酸在该反应中体现氧化性和酸性的个数比是____________ .
(4)以下3个未配平的化学反应方程式中:① ;②
;②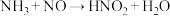 ;③
;③ ,一定不可能发生的是
,一定不可能发生的是____________ .
(5)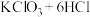 (浓)
(浓) 可以用来制氯气,在该反应中氧化剂和还原剂的个数比为
可以用来制氯气,在该反应中氧化剂和还原剂的个数比为____________ ,生成6个 分子,转移的电子数为
分子,转移的电子数为____________ .
(6)高铁酸钾 是一种环保、高效饮水处理剂,通过图流程可以制备
是一种环保、高效饮水处理剂,通过图流程可以制备 ,相关反应的化学方程式:
,相关反应的化学方程式: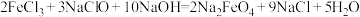 .
.
请用双线桥表示其电子转移的方向和数目:______________________________________________ .

(1)下列反应中不涉及氧化还原反应的是____________(填序号).
| A.蜡炬成灰 | B.水滴石穿 | C.食物腐败 | D.钟乳石的形成 | E.醋酸清洗水垢 |
(2)缺铁性贫血患者在服用补铁药片时,与维生素C同服效果更佳,因为维生素C可以将不易吸收的
 转化为
转化为 .该过程中维生素C表现出的性质与下列____________(填序号)反应中
.该过程中维生素C表现出的性质与下列____________(填序号)反应中 表现出的性质相同.
表现出的性质相同.A. |
B.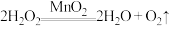 |
C.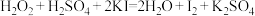 |
D. |
(3)已知实验室制取
 的反应:
的反应: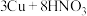 (稀)
(稀) ,该反应的离子方程式为
,该反应的离子方程式为(4)以下3个未配平的化学反应方程式中:①
 ;②
;②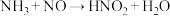 ;③
;③ ,一定不可能发生的是
,一定不可能发生的是(5)
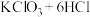 (浓)
(浓) 可以用来制氯气,在该反应中氧化剂和还原剂的个数比为
可以用来制氯气,在该反应中氧化剂和还原剂的个数比为 分子,转移的电子数为
分子,转移的电子数为(6)高铁酸钾
 是一种环保、高效饮水处理剂,通过图流程可以制备
是一种环保、高效饮水处理剂,通过图流程可以制备 ,相关反应的化学方程式:
,相关反应的化学方程式: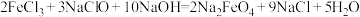 .
.请用双线桥表示其电子转移的方向和数目:

您最近一年使用:0次
解题方法
4 . 以辉铜矿(主要成分是 Cu2S。含少量 FeS2、FeS、SiO2等)为原料制备胆矾、硫代硫酸钠(Na2S2O3·5H2O)。流程如图所示。 回答下列问题:
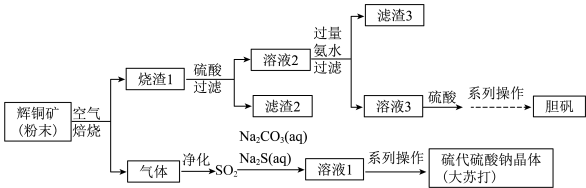
已知:Cu(OH)2+4NH3·H2O═[Cu(NH3)4](OH)2+4H2O,[Cu(NH3)4](OH)2与硫酸反应生成CuSO4。
(1)焙烧时,粉碎矿石的目的是___________ ;滤渣2的主要成分是___________ (填化学式)。
(2)向Na2S和 Na2CO3的混合溶液中通入SO2制备硫代硫酸钠的化学方程式为___________ 。
(3)某小组探究外界条件对 Na2S2O3相关反应的反应速率的影响,实验方案如下:
已知:① (慢),②
(慢),② (快)。
(快)。
上述反应中,活化能较大的反应是___________ (填“①”或“②”)。下列叙述错误的是___________ (填标号)。
A.在KI-淀粉溶液中滴加过量 Na2S2O3溶液,溶液始终不会变蓝
B.上述方案可以探究浓度对反应速率的影响
C.当n(Na2S2O3):n(K2S2O8)的值小于2时会出现蓝色
(4)检验溶液2中含 Fe2+的试剂可能是___________(填标号)。
(5)25.0 g CuSO4·5H2O受热分解。残留固体的质量与温度的关系如图所示。

①1300 ℃时,固体的成分是___________ (填化学式)。
②已知580~1000℃之间产生了两种气体和一种固体,写出发生反应的化学方程式:___________ 。

已知:Cu(OH)2+4NH3·H2O═[Cu(NH3)4](OH)2+4H2O,[Cu(NH3)4](OH)2与硫酸反应生成CuSO4。
(1)焙烧时,粉碎矿石的目的是
(2)向Na2S和 Na2CO3的混合溶液中通入SO2制备硫代硫酸钠的化学方程式为
(3)某小组探究外界条件对 Na2S2O3相关反应的反应速率的影响,实验方案如下:
已知:①
 (慢),②
(慢),② (快)。
(快)。| 体积/mL | ||||
| 实验序号 | K2S2O8溶液 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 |
| 1 | 10.0 | 4.0 | 5.0 | 2.0 |
| 2 | 5.0 | 4.0 | 5.0 | 2.0 |
A.在KI-淀粉溶液中滴加过量 Na2S2O3溶液,溶液始终不会变蓝
B.上述方案可以探究浓度对反应速率的影响
C.当n(Na2S2O3):n(K2S2O8)的值小于2时会出现蓝色
(4)检验溶液2中含 Fe2+的试剂可能是___________(填标号)。
| A.KSCN溶液 | B.K3Fe(CN)6溶液 | C.酸性 KMnO4溶液 | D.NaOH 溶液 |

①1300 ℃时,固体的成分是
②已知580~1000℃之间产生了两种气体和一种固体,写出发生反应的化学方程式:
您最近一年使用:0次
5 . 化学与生产和生活密切相关,下列分析正确的是
| A.用氯化钙作钢箱梁大桥融雪剂对钢箱梁大桥无影响 |
| B.“日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华的现象 |
| C.过氧碳酸钠(2Na2CO3•3H2O2)具有碳酸钠和H2O2的双重性质,可作去污剂、消毒剂 |
| D.“碳纳米泡沫”与石墨烯互为同分异构体 |
您最近一年使用:0次
6 . Ⅰ.硅在元素周期表中,处于金属和非金属的交界处,是良好的半导体材料,单晶硅是生产芯片的重要材料。工业冶炼纯硅的原理是:① ;②
;② ;③
;③ 。化学反应与能量变化如图所示,回答下列问题:
。化学反应与能量变化如图所示,回答下列问题:
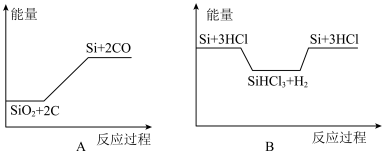
(1)反应①属于_______ 反应(填“吸热”或“放热”)。反应②破坏反应物中的化学键所吸收的能量_______ (填“>”或“<”)形成生成物中化学键所放出的能量。
Ⅱ.化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用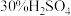 溶液作电解质溶液,其简易装置如图所示。
溶液作电解质溶液,其简易装置如图所示。
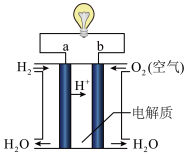
(2)在这个燃料电池中,正极的电极反应式为_______ 。若在标况下,消耗了33.6L的氢气,此时电路中转移的电子数目为_______ (用阿伏加德罗常数表示)。
Ⅲ.1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图所示(反应温度为450℃):

(3)用地康法制备氯气时总反应的方程式为_______ ,其中氧化剂与还原剂的物质的量之比为_______ 。
(4)在该过程中,氧化铜的作用是_______ 。
 ;②
;② ;③
;③ 。化学反应与能量变化如图所示,回答下列问题:
。化学反应与能量变化如图所示,回答下列问题:
(1)反应①属于
Ⅱ.化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用
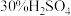 溶液作电解质溶液,其简易装置如图所示。
溶液作电解质溶液,其简易装置如图所示。
(2)在这个燃料电池中,正极的电极反应式为
Ⅲ.1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图所示(反应温度为450℃):

(3)用地康法制备氯气时总反应的方程式为
(4)在该过程中,氧化铜的作用是
您最近一年使用:0次
名校
7 . 胆矾(CuSO4·5H2O,相对式量为250)受热会先失去结晶水,完全脱水的化学方程式为: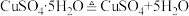 ,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
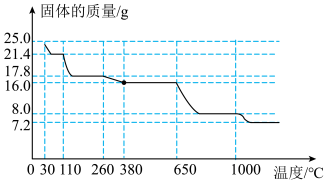
(1)胆矾失水的温度范围为30℃~380C
(2)开始加热至完全脱水,胆矾经历5次脱水过程
(3)650℃后CuSO4分解得到CuO和SO2两种物质
(4)1000℃时,得到固体物质的化学式为CuO
(5)1000℃之后,可能发生了以下的化学变化: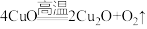
(6)整个变化过程中没有元素化合价发生改变
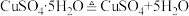 ,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
(1)胆矾失水的温度范围为30℃~380C
(2)开始加热至完全脱水,胆矾经历5次脱水过程
(3)650℃后CuSO4分解得到CuO和SO2两种物质
(4)1000℃时,得到固体物质的化学式为CuO
(5)1000℃之后,可能发生了以下的化学变化:
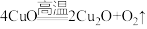
(6)整个变化过程中没有元素化合价发生改变
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
8 . 已知: 易溶于水,
易溶于水, 微溶于水。以含锂的电解铝废渣(主要含
微溶于水。以含锂的电解铝废渣(主要含 、
、 、
、 、
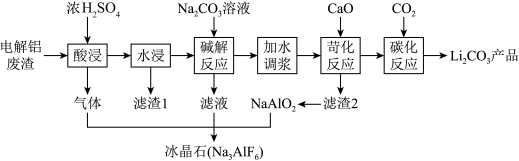
、 )和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
)和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
 易溶于水,
易溶于水, 微溶于水。以含锂的电解铝废渣(主要含
微溶于水。以含锂的电解铝废渣(主要含 、
、 、
、 、
、 )和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
)和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
A.第一步酸浸时产生气体的化学式为 |
B.滤渣1的成分为 |
C.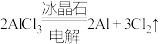 |
D.碳化反应后的溶液得到 的具体实验操作是蒸发浓缩,冷却结晶,过滤,洗涤,干燥 的具体实验操作是蒸发浓缩,冷却结晶,过滤,洗涤,干燥 |
您最近一年使用:0次
解题方法
9 . 化学与生产、生活密切相关。下列说法不正确的是
A.《美国陶瓷学会会刊》发表我国故宫研究院的考古成果:乾隆时期紫金釉中发现特殊晶体-亚稳相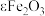 晶体,该样品溶于盐酸,滴加KSCN溶液,可验证 晶体,该样品溶于盐酸,滴加KSCN溶液,可验证 |
| B.利用酸性重铬酸钾检测酒驾利用了酸性重铬酸钾的强氧化性和酒精的还原性、挥发性 |
| C.石油的分馏,煤的气化、液化均属于物理变化 |
| D.采取“汽车尾气催化净化”“静电除尘”“燃煤固硫”等方法,可提高空气质量 |
您最近一年使用:0次
10 . 利用下图可从不同角度研究含氯物质的性质及其转化关系。回答下列问题:
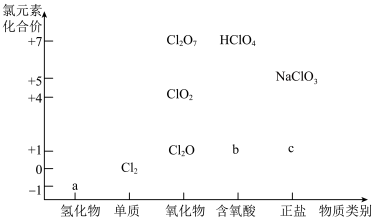
(1)图中a物质是否为电解质___________ (填“是”或“否”),b物质的化学式为___________ 。
(2)实验室用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的离子方程式:___________ 。
(3)“84消毒液”是常用含氯消毒剂,其有效成分是图中c物质,“84消毒液”不可与洁厕灵(主要成分稀盐酸)混合使用的原因是___________ 。(用离子方程式说明)
(4)工业漂白粉中的有效成分 能与空气中的水蒸气和二氧化碳发生如下反应:
能与空气中的水蒸气和二氧化碳发生如下反应: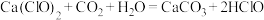 ,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:
,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:___________ 。
(5)高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理,工业上制备 有多种方法,其中一种制备的化学原理是在碱性条件下用
有多种方法,其中一种制备的化学原理是在碱性条件下用 氧化氯化铁,请完成离子方程式的配平:
氧化氯化铁,请完成离子方程式的配平:
__ ____
____ ____
____ —___
—___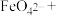 ___
___ ___
___ ,
,______________ 。反应中消耗 数与转移的电子数之比是
数与转移的电子数之比是___________ 。

(1)图中a物质是否为电解质
(2)实验室用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的离子方程式:
(3)“84消毒液”是常用含氯消毒剂,其有效成分是图中c物质,“84消毒液”不可与洁厕灵(主要成分稀盐酸)混合使用的原因是
(4)工业漂白粉中的有效成分
 能与空气中的水蒸气和二氧化碳发生如下反应:
能与空气中的水蒸气和二氧化碳发生如下反应: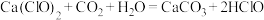 ,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:
,久置于空气中的漂白粉易失效,请用化学方程式解释漂白粉失效的原因:(5)高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理,工业上制备
 有多种方法,其中一种制备的化学原理是在碱性条件下用
有多种方法,其中一种制备的化学原理是在碱性条件下用 氧化氯化铁,请完成离子方程式的配平:
氧化氯化铁,请完成离子方程式的配平:__
 ____
____ ____
____ —___
—___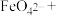 ___
___ ___
___ ,
, 数与转移的电子数之比是
数与转移的电子数之比是
您最近一年使用:0次
2023-07-28更新
|
283次组卷
|
2卷引用:云南师大附中、官渡一中、迪庆一中三校2023-2024学年高一上学期11月期中考试化学试题



