解题方法
1 . 某制酸工厂产生的废酸液主要成分为HF、 、
、 、
、 、
、 ,一种处理工艺如下:
,一种处理工艺如下: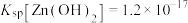
回答下列问题:
(1)基态As原子的价层电子排布图为__________________ ,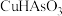 中As的化合价为
中As的化合价为_________ 。
(2)原废水中含有的 浓度为52.0
浓度为52.0 ,则
,则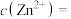
_____  ,常温下,有B离子的去除量、“调pH”为6.0后,
,常温下,有B离子的去除量、“调pH”为6.0后, 的去除率为
的去除率为_______ 。(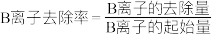 )
)
(3)强碱(AOH)的化学式为_____________ 。
(4)写出“还原”过程中 发生反应的化学方程式
发生反应的化学方程式_______________ 。
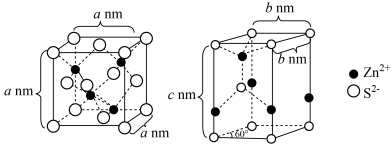
(5)产品结构分析。晶体W的晶胞结构如图所示:__________ 。
②W的化学式为_____________ 。
(6)产品纯度分析。称取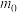 g
g  样品,用碱溶解,加入淀粉作指示剂,用浓度为
样品,用碱溶解,加入淀粉作指示剂,用浓度为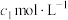 的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为
的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为 mL,则制得的产品纯度为
mL,则制得的产品纯度为___________ 。(用含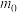 、
、 、
、 的代数式表示)
的代数式表示)
 、
、 、
、 、
、 ,一种处理工艺如下:
,一种处理工艺如下: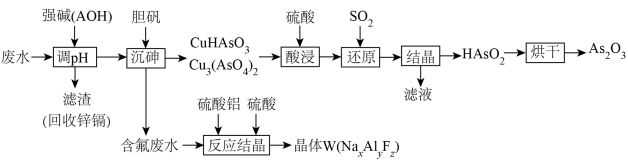
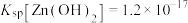
回答下列问题:
(1)基态As原子的价层电子排布图为
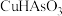 中As的化合价为
中As的化合价为(2)原废水中含有的
 浓度为52.0
浓度为52.0 ,则
,则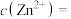
 ,常温下,有B离子的去除量、“调pH”为6.0后,
,常温下,有B离子的去除量、“调pH”为6.0后, 的去除率为
的去除率为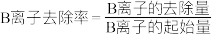 )
)(3)强碱(AOH)的化学式为
(4)写出“还原”过程中
 发生反应的化学方程式
发生反应的化学方程式(5)产品结构分析。晶体W的晶胞结构如图所示:

②W的化学式为
(6)产品纯度分析。称取
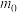 g
g  样品,用碱溶解,加入淀粉作指示剂,用浓度为
样品,用碱溶解,加入淀粉作指示剂,用浓度为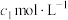 的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为
的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为 mL,则制得的产品纯度为
mL,则制得的产品纯度为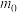 、
、 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
名校
解题方法
2 . 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
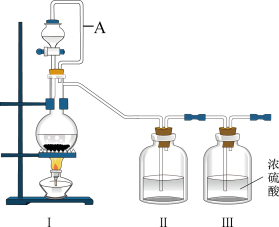
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和
_______ 。写出该装置制备氯气的离子方程式:_______ 。
(2)乙组同学利用甲组制得的NO和 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:________ 。
②装置连接顺序为a→________ (按气流自左向右方向,用小写字母表示)。
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为_______ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为______ 。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为________ (用代数式表示即可)。
(1)甲组同学拟用同一装置Ⅰ、Ⅱ、Ⅲ分别制备纯净干燥的NO和

(2)乙组同学利用甲组制得的NO和
 制备NOCl,装置如图所示:
制备NOCl,装置如图所示: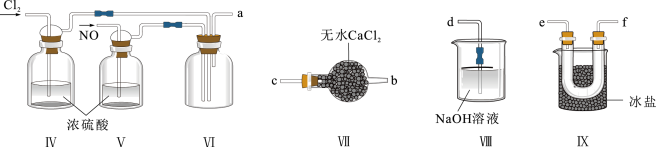
②装置连接顺序为a→
③装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00 mL,用c mol/L
 溶液反应,消耗
溶液反应,消耗 溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的环境问题也日益受到关注。回答以下问题:
(1)与氮氧化物有关的全球性大气环境问题有_____。
(2)以下是氮循环的一部分: 的方法与其不同,写出实验室中固体物质加热制取氨气的化学方程式
的方法与其不同,写出实验室中固体物质加热制取氨气的化学方程式________ 。
②反应⑥的离子方程式是_______ 。
③催化剂存在下, 也可用来消除
也可用来消除 的污染,生成两种对环境无害的物质,请写出
的污染,生成两种对环境无害的物质,请写出 与
与 反应的化学方程式为
反应的化学方程式为_______ 。
Ⅱ.二氧化硫性质探究
(3)实验小组甲同学向:5 mL 1 mol⋅L
 溶液中通入足量的
溶液中通入足量的 ,检验该反应中产物含有
,检验该反应中产物含有 的方法是
的方法是_______ 。
(4)实验小组乙同学将 通入少量酸性
通入少量酸性 溶液,酸性
溶液,酸性 溶液褪色,请写出此反应的离子方程式:
溶液褪色,请写出此反应的离子方程式:_______ 。
Ⅲ.中华人民共和国国家标准规定葡萄酒中最大使用量为0.25 g/L。某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中,并对其含量进行定性测定。 全部逸出并与C中
全部逸出并与C中 完全反应,除去C中过量的
完全反应,除去C中过量的 ,然后用0.1 mol/L NaOH溶液进行反应,恰好反应时,消耗NaOH溶液25.00 mL,该葡萄酒中
,然后用0.1 mol/L NaOH溶液进行反应,恰好反应时,消耗NaOH溶液25.00 mL,该葡萄酒中 含量为
含量为_____ g/L。
(1)与氮氧化物有关的全球性大气环境问题有_____。
| A.酸雨 | B.沙尘暴 | C.光化学烟雾 | D.白色污染 |
(2)以下是氮循环的一部分:
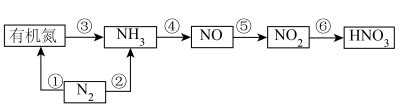
 的方法与其不同,写出实验室中固体物质加热制取氨气的化学方程式
的方法与其不同,写出实验室中固体物质加热制取氨气的化学方程式②反应⑥的离子方程式是
③催化剂存在下,
 也可用来消除
也可用来消除 的污染,生成两种对环境无害的物质,请写出
的污染,生成两种对环境无害的物质,请写出 与
与 反应的化学方程式为
反应的化学方程式为Ⅱ.二氧化硫性质探究
(3)实验小组甲同学向:5 mL 1 mol⋅L

 溶液中通入足量的
溶液中通入足量的 ,检验该反应中产物含有
,检验该反应中产物含有 的方法是
的方法是(4)实验小组乙同学将
 通入少量酸性
通入少量酸性 溶液,酸性
溶液,酸性 溶液褪色,请写出此反应的离子方程式:
溶液褪色,请写出此反应的离子方程式:Ⅲ.中华人民共和国国家标准规定葡萄酒中最大使用量为0.25 g/L。某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中,并对其含量进行定性测定。
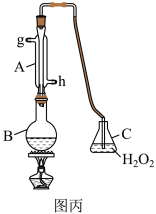
 全部逸出并与C中
全部逸出并与C中 完全反应,除去C中过量的
完全反应,除去C中过量的 ,然后用0.1 mol/L NaOH溶液进行反应,恰好反应时,消耗NaOH溶液25.00 mL,该葡萄酒中
,然后用0.1 mol/L NaOH溶液进行反应,恰好反应时,消耗NaOH溶液25.00 mL,该葡萄酒中 含量为
含量为
您最近一年使用:0次
解题方法
4 . Ⅰ.铁及其化合物在生产生活中有极其重要的用途。 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
(1)由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:______ 。
Ⅱ.高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和 胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
(2)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠: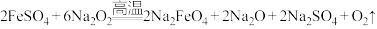 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。上述反应在熔融状态下进行,而不在水溶液中进行的原因是
。上述反应在熔融状态下进行,而不在水溶液中进行的原因是______ 。
(3)高铁酸钾可通过次氯酸钾氧化 溶液来制备。次氯酸钾的制备装置如图所示。
溶液来制备。次氯酸钾的制备装置如图所示。
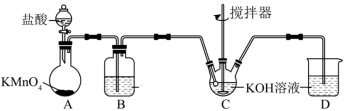
回答下列问题:
①装置A中 与盐酸反应生成
与盐酸反应生成 和
和 ,其化学方程式为
,其化学方程式为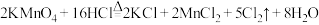 。
。
a.请用双线桥法标出电子转移方向与数目_______ 。
b.上述反应中的HCl体现了什么性质?_______ 。
②将制备的 通过装置B可除去杂质HCl,B中的溶液为
通过装置B可除去杂质HCl,B中的溶液为_____ 。
③ 和KOH溶液在较高温度下反应生成
和KOH溶液在较高温度下反应生成 。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是
。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是______ 。
④若实验制得的次氯酸钾溶液中 (N代表微粒个数),则
(N代表微粒个数),则
_______ 。
⑤装置D的作用是_______ 。
⑥次氯酸盐氧化法是在碱性条件下,KClO饱和溶液可将 转化为
转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:________ 。
 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
(1)由上述实验能否得出“维生素C可将
 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:Ⅱ.高铁酸钾(
 )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和 胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。(2)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:
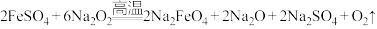 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。上述反应在熔融状态下进行,而不在水溶液中进行的原因是
。上述反应在熔融状态下进行,而不在水溶液中进行的原因是(3)高铁酸钾可通过次氯酸钾氧化
 溶液来制备。次氯酸钾的制备装置如图所示。
溶液来制备。次氯酸钾的制备装置如图所示。
回答下列问题:
①装置A中
 与盐酸反应生成
与盐酸反应生成 和
和 ,其化学方程式为
,其化学方程式为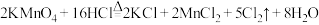 。
。a.请用双线桥法标出电子转移方向与数目
b.上述反应中的HCl体现了什么性质?
②将制备的
 通过装置B可除去杂质HCl,B中的溶液为
通过装置B可除去杂质HCl,B中的溶液为③
 和KOH溶液在较高温度下反应生成
和KOH溶液在较高温度下反应生成 。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是
。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是④若实验制得的次氯酸钾溶液中
 (N代表微粒个数),则
(N代表微粒个数),则
⑤装置D的作用是
⑥次氯酸盐氧化法是在碱性条件下,KClO饱和溶液可将
 转化为
转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
名校
5 . 下表是某城市某日空气质量报告:
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行探究。
实验一:用下图所示装置进行实验。

(1)A装置的作用是____________________ 。
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变成________ 色,说明SO2与水反应生成一种酸。
(3)D装置的作用是_____________ ,写出反应的化学方程式________________ 。
实验二:
(4)往盛有水的烧杯中通入SO2气体,然后每隔1 h测定其pH,发现pH逐渐变小,直至恒定。说明烧杯中溶液被空气中的氧气最终氧化成(写化学式)________ 。
(5)查阅资料:SO2形成酸雨的另一途径:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4。在此过程中飘尘作________________ 。
探究结论:SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(6)若将D中的溶液换成酸性Na2FeO4溶液,一会儿后发现溶液呈黄色,写出此时溶液中所发生的离子反应的方程式_____________ 。
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
55 | SO2 | Ⅱ | 良 |
实验一:用下图所示装置进行实验。

(1)A装置的作用是
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变成
(3)D装置的作用是
实验二:
(4)往盛有水的烧杯中通入SO2气体,然后每隔1 h测定其pH,发现pH逐渐变小,直至恒定。说明烧杯中溶液被空气中的氧气最终氧化成(写化学式)
(5)查阅资料:SO2形成酸雨的另一途径:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4。在此过程中飘尘作
探究结论:SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(6)若将D中的溶液换成酸性Na2FeO4溶液,一会儿后发现溶液呈黄色,写出此时溶液中所发生的离子反应的方程式
您最近一年使用:0次
解题方法
6 .  是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为
是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为 ,还含有少量:
,还含有少量: 、
、 、
、 、
、 、
、 、PbO,
、PbO, 、CdO和
、CdO和 )制备
)制备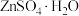 流程如下:
流程如下:
回答下列问题:
(1)加硫酸浸取后再调节pH=5,过滤获得的滤渣①的主要成分为 、
、 、
、 、
、___________ 和___________ 。
(2)加入 溶液后过滤可以得到
溶液后过滤可以得到 和
和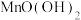 两种沉淀,
两种沉淀, 发生反应的离子方程式为
发生反应的离子方程式为___________ ,常温下,此时溶液pH仍为5,则溶液残留的微量 的浓度约为
的浓度约为___________ mol/L⋅,根据“转化过滤”过程,推测若Zn、稀硫酸、Cd形成原电池,则电势较高的一极为___________ 。
(3)“脱钙镁”后“过滤”所得的滤渣还可以和浓硫酸反应制备HF以循环使用,则该反应可以发生的原因是___________ 。
(4)脱完钙和镁之后的 滤液中含有少量的
滤液中含有少量的 ,
, 的溶解度曲线如图。由滤液④获得
的溶解度曲线如图。由滤液④获得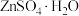 的具体操作为
的具体操作为___________ 。___________ (用含a、b、c的代数式表示)。
 是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为
是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为 ,还含有少量:
,还含有少量: 、
、 、
、 、
、 、
、 、PbO,
、PbO, 、CdO和
、CdO和 )制备
)制备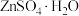 流程如下:
流程如下: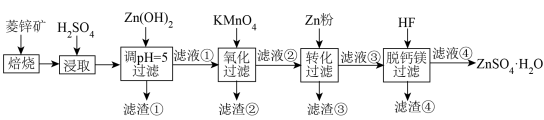
| 金属阳离子 |  |  |  | 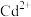 |  |  |  |
| 开始沉淀pH | 6.2 | 7.4 | 2.2 | 7.7 | 9.1 | 8.1 | 3.4 |
| 沉淀完全pH | 8.2 | 8.9 | 3.2 | 9.7 | 11.1 | 10.1 | 4.7 |
(1)加硫酸浸取后再调节pH=5,过滤获得的滤渣①的主要成分为
 、
、 、
、 、
、(2)加入
 溶液后过滤可以得到
溶液后过滤可以得到 和
和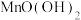 两种沉淀,
两种沉淀, 发生反应的离子方程式为
发生反应的离子方程式为 的浓度约为
的浓度约为(3)“脱钙镁”后“过滤”所得的滤渣还可以和浓硫酸反应制备HF以循环使用,则该反应可以发生的原因是
(4)脱完钙和镁之后的
 滤液中含有少量的
滤液中含有少量的 ,
, 的溶解度曲线如图。由滤液④获得
的溶解度曲线如图。由滤液④获得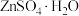 的具体操作为
的具体操作为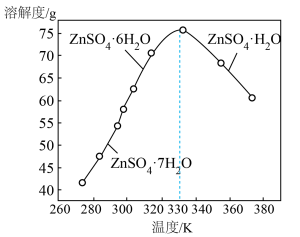
您最近一年使用:0次
名校
解题方法
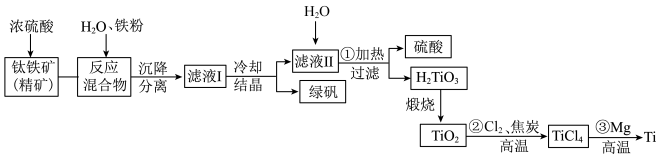
7 . 金属钛硬度大、熔点高、耐腐蚀,易被氧化,被誉为“未来金属”。以钛铁矿(主要成分 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如图,其中钛铁矿与浓硫酸发生反应的化学方程式为:
,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如图,其中钛铁矿与浓硫酸发生反应的化学方程式为: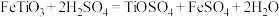 。已知
。已知 熔点为1850℃,回答下列问题:
熔点为1850℃,回答下列问题:
(1)生产时将钛铁矿精矿粉碎后再与浓硫酸反应,其目的是_______ ,钛酸亚铁( )中钛元素的化合价为
)中钛元素的化合价为_______ 价。
(2)滤液Ⅱ中主要物质是 ,反应①的化学方程式是
,反应①的化学方程式是_______ 。
(3)反应②生成 和一种可燃性气体,其化学反应方程式为
和一种可燃性气体,其化学反应方程式为_______ 。
(4)反应③需要在氩气氛围中进行,原因是_______ 。
(5)CO与 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池总反应为
构成的质子交换膜燃料电池总反应为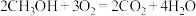 ,负极的电极反应式为
,负极的电极反应式为_______ 。若外电路中转移2mol电子,则上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L
 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如图,其中钛铁矿与浓硫酸发生反应的化学方程式为:
,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如图,其中钛铁矿与浓硫酸发生反应的化学方程式为: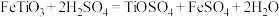 。已知
。已知 熔点为1850℃,回答下列问题:
熔点为1850℃,回答下列问题:
(1)生产时将钛铁矿精矿粉碎后再与浓硫酸反应,其目的是
 )中钛元素的化合价为
)中钛元素的化合价为(2)滤液Ⅱ中主要物质是
 ,反应①的化学方程式是
,反应①的化学方程式是(3)反应②生成
 和一种可燃性气体,其化学反应方程式为
和一种可燃性气体,其化学反应方程式为(4)反应③需要在氩气氛围中进行,原因是
(5)CO与
 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池总反应为
构成的质子交换膜燃料电池总反应为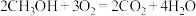 ,负极的电极反应式为
,负极的电极反应式为 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
8 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
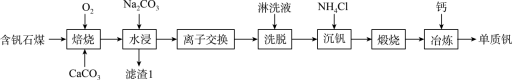
已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
②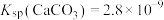 ,
,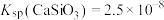 ,
,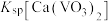 远大于
远大于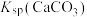 。
。
回答下列问题:
(1)基态Fe3+的价电子轨道表示式为______ 。
(2)“焙烧”时,V2O3、V2O4都转化为 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:____________ 。
(3)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有______ :“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是______ 。(列式计算平衡常数分析该反应进行的趋势,一般认为, 时反应进行较完全,
时反应进行较完全,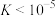 时反应难以进行)
时反应难以进行)
(4)“离子交换”与“洗脱”可表示为 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用______ 。
(5)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是____________ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是______(填字母)。

已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
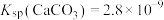 ,
,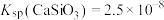 ,
,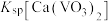 远大于
远大于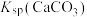 。
。回答下列问题:
(1)基态Fe3+的价电子轨道表示式为
(2)“焙烧”时,V2O3、V2O4都转化为
 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:(3)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
 时反应进行较完全,
时反应进行较完全,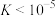 时反应难以进行)
时反应难以进行)(4)“离子交换”与“洗脱”可表示为
 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(5)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是______(填字母)。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
9 . 利用下图,可以从不同角度研究含硫物质的性质及其转化关系,图中物质甲~己中均含有硫元素.回答下列问题:
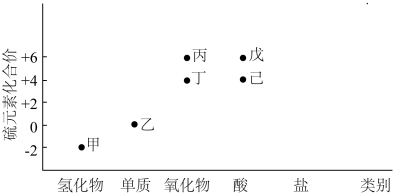
(1)写出甲的电子式:_______ ,该物质中的硫元素可表现出___________ (填“氧化性”或“还原性”);利用高温热分解甲可以获得乙,该方法的优点是______________ ,缺点是_____________ .
(2)黄铁矿(主要成分为 )在沸腾炉中与氧气反应,主要生成的含硫元素的物质是
)在沸腾炉中与氧气反应,主要生成的含硫元素的物质是__________ (填“丙”或“丁”),该物质与水化合生成___________ (填化学名称).
(3)① 溶液与戊溶液反应的离子方程式为
溶液与戊溶液反应的离子方程式为_______________________________ .
②同位素示踪实验可证实 中两个S原子的化学环境不同,实验过程为
中两个S原子的化学环境不同,实验过程为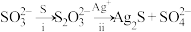 .过程ii中,
.过程ii中, 断裂的只有硫硫键,若过程i所用试剂为
断裂的只有硫硫键,若过程i所用试剂为 和
和 ,过程ii含硫产物是
,过程ii含硫产物是_____________ (标记出同位素原子).

(1)写出甲的电子式:
(2)黄铁矿(主要成分为
 )在沸腾炉中与氧气反应,主要生成的含硫元素的物质是
)在沸腾炉中与氧气反应,主要生成的含硫元素的物质是(3)①
 溶液与戊溶液反应的离子方程式为
溶液与戊溶液反应的离子方程式为②同位素示踪实验可证实
 中两个S原子的化学环境不同,实验过程为
中两个S原子的化学环境不同,实验过程为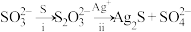 .过程ii中,
.过程ii中, 断裂的只有硫硫键,若过程i所用试剂为
断裂的只有硫硫键,若过程i所用试剂为 和
和 ,过程ii含硫产物是
,过程ii含硫产物是
您最近一年使用:0次
名校
解题方法
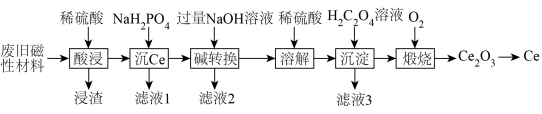
10 . 稀土金属(RE)属于战略性金属,我国的稀土提炼技术位于世界领先地位。一种从废旧磁性材料[主要成分为铈(Ce)、Al、Fe和少量不溶于酸的杂质]中回收稀土金属Ce的工艺流程如图所示。
(1)为提高酸浸的速率,可采取的措施为___________ (写一条即可)。
(2)常温下,“酸浸”后测得溶液中c(Fe2+)=1.0mol/L,c(Ce3+)=0.01mol/L,则“沉Ce”时,为了使Al3+完全沉淀,但不引人Fe(OH)2和Ce(OH)3,需要调节溶液的pH范围为___________ 。
(3)“碱转换”过程中Ce(H2PO4)所发生反应的离子方程式为___________ ,“滤液2”中铝元素的存在形式为___________ (填化学式)。
(4)“沉淀”后所得的固体为Ce2(C2O4)3·10H2O,将其煅烧可得Ce2O3和一种无毒的气体,发生反应的化学方程式为___________ 。
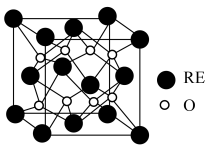
(5)某稀土金属氧化物的立方晶胞如图所示,则该氧化物的化学式为___________ ,距离RE原子最近的O原子有___________ 个。若M(晶胞)=Mg/mol,晶胞边长为anm,NA为阿伏加德罗常数的值,则晶胞的密度为___________ g/cm3(列出计算式)。
(1)为提高酸浸的速率,可采取的措施为
(2)常温下,“酸浸”后测得溶液中c(Fe2+)=1.0mol/L,c(Ce3+)=0.01mol/L,则“沉Ce”时,为了使Al3+完全沉淀,但不引人Fe(OH)2和Ce(OH)3,需要调节溶液的pH范围为
(3)“碱转换”过程中Ce(H2PO4)所发生反应的离子方程式为
(4)“沉淀”后所得的固体为Ce2(C2O4)3·10H2O,将其煅烧可得Ce2O3和一种无毒的气体,发生反应的化学方程式为
(5)某稀土金属氧化物的立方晶胞如图所示,则该氧化物的化学式为
您最近一年使用:0次
2024-03-31更新
|
1063次组卷
|
4卷引用:2024届广东省肇庆市高三上学期二模化学试题
2024届广东省肇庆市高三上学期二模化学试题(已下线)化学(广东卷02)-2024年高考押题预测卷2024届广东省梅州市兴宁市第一中学高三下学期二模化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)






