2016·江苏·一模
名校
解题方法
1 . 从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
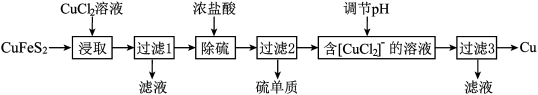
已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为_____ .
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为_____ .
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是_____ .(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有_____ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_____ .
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,化学方程式为:6CuFeS2+13O2 3Cu2S+2Fe3O4+9SO2、Cu2S+O2
3Cu2S+2Fe3O4+9SO2、Cu2S+O2 2Cu+SO2此工艺与前一工艺相比主要缺点有
2Cu+SO2此工艺与前一工艺相比主要缺点有_____ .

已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)过滤3所得滤液中可以循环使用的物质有
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,化学方程式为:6CuFeS2+13O2
 3Cu2S+2Fe3O4+9SO2、Cu2S+O2
3Cu2S+2Fe3O4+9SO2、Cu2S+O2 2Cu+SO2此工艺与前一工艺相比主要缺点有
2Cu+SO2此工艺与前一工艺相比主要缺点有
您最近一年使用:0次
2019-11-27更新
|
546次组卷
|
6卷引用:2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)
(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)2016届江苏省清江中学高三下学期考前练习化学试卷江苏省苏州市2020届高三上学期期初调研化学试题广东省深圳市龙岗区龙城高级中学2021届高三第一次模拟考试化学试题
2 . 工业上常以黄铜矿(主要成分是CuFeS2)为原料制备铜以及副产物铁红(Fe2O3),两种方法均能实现铜的冶炼,其工艺流程如图:

回答下列问题:
(1)为使“焙烧”反应充分进行,工业上可采取的措施是____ (写一条),写出“焙烧”时反应的化学方程式:___ 。
(2)“灼烧1”工序中起氧化作用的物质是____ 。
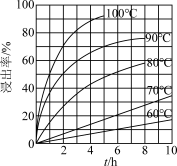
(3)FeCl3溶液“浸取”时,铜的浸出率结果如图所示。由图可知,当铜的浸出率为90%时,所采用的实验条件为____ ,写出该工序发生反应的离子方程式:______ 。
(4)“调节pH”所用试剂X是_____ ,该工序的目的是除去溶液中的Fe3+。当调节溶液的pH=3.5时,Fe3+______ (填“是”或“不是”)沉淀完全[c(Fe3+)≤1×10-5mol•L-1时可认为Fe3+沉淀完全],若滤液中c(Cu2+)=0.2mol•L-1,此时是否有Cu(OH)2析出?_______ (列式计算)。{已知:25℃时,Ksp[Fe(OH)3]=1.0×10-39、Ksp[Cu(OH)2]=2.2×10-20}
(5)方法乙比方法甲更好,其原因是_____ (写一点)。

回答下列问题:
(1)为使“焙烧”反应充分进行,工业上可采取的措施是
(2)“灼烧1”工序中起氧化作用的物质是
(3)FeCl3溶液“浸取”时,铜的浸出率结果如图所示。由图可知,当铜的浸出率为90%时,所采用的实验条件为

(4)“调节pH”所用试剂X是
(5)方法乙比方法甲更好,其原因是
您最近一年使用:0次
名校
3 . 某铜制品在潮湿环境中发生的电化学腐蚀过程可表示为如图,腐蚀后有A物质生成,某小组为分析A物质的组成,进行了如下实验:
实验①:取A样品,加过量稀硝酸完全溶解后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
实验②:另取A样品4.29g,加入含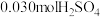 的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
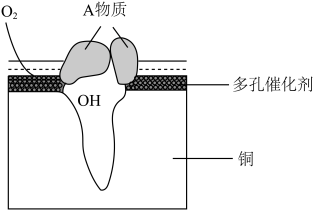
(1)该粉状锈中除了铜元素外还含有(写元素符号)___ 元素,该铜制品发生电化学腐蚀生成粉状锈时其正极电极反应式为____ 。
(2)写出该粉状锈溶于稀硫酸反应的离子方程式____ 。
(3)加热条件下,实验②中所得的黑色固体能与乙醇反应,化学方程式为____ 。
实验①:取A样品,加过量稀硝酸完全溶解后,再加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。实验②:另取A样品4.29g,加入含
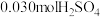 的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
(1)该粉状锈中除了铜元素外还含有(写元素符号)
(2)写出该粉状锈溶于稀硫酸反应的离子方程式
(3)加热条件下,实验②中所得的黑色固体能与乙醇反应,化学方程式为
您最近一年使用:0次
解题方法
4 . 由两种元素组成的矿物A,测定A的组成流程如下:
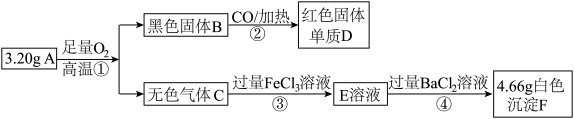
请回答:
(1)②反应中除了产生D外,还有一种气体生成,请写出该气体的电子式____________
(2)写出①的化学方程式:_______________________________________________________
(3)写出③的离子方程式:____________________________________________________
(4)检验E溶液中含有Fe2+ 的方法是:_____________________________

请回答:
(1)②反应中除了产生D外,还有一种气体生成,请写出该气体的电子式
(2)写出①的化学方程式:
(3)写出③的离子方程式:
(4)检验E溶液中含有Fe2+ 的方法是:
您最近一年使用:0次
2019-08-10更新
|
392次组卷
|
2卷引用:2019-2020学年新人教版必修2第5章第2节《氮及其化合物》作业
5 . 氯化亚铜(CuCl)广泛应用于有机合成、染料、颜料、催化剂等工业。它是一种白色粉末,微溶于水,不溶于乙醇、稀硝酸及稀硫酸,可溶于氨水、浓盐酸,并生成配合物NH4[CuCl2];能在空气中迅速被氧化成绿色;见光则分解,变成褐色。下图是实验室制备氯化亚铜的流程图及实验装置图。
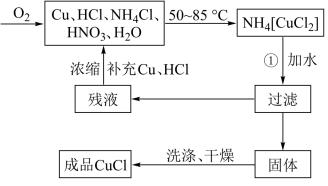
实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36%盐酸15mL、水。
(1)请写出①的化学方程式____________________________________ 。
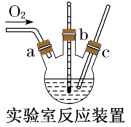
(2)本实验中通入O2的速率不宜过大,宜选择下图中的____ (填字母序号)方案,并说明选择该装置的理由__________________________________________ 。
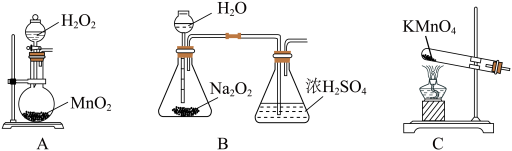
(3)电炉加热升温至50℃时停止加热,反应快速进行,当烧瓶中液面上方的现象为_____ 时,停止通入氧气,打开瓶塞,沿C口倾出反应液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出。
(4)关于该实验过程中,下列说法正确的是_________________ 。
A 实验开始时,温度计显示反应液温度可能低于室温。
B 流程中过滤操作,可以采用真空抽滤的方式,洗涤固体可以用95%的酒精。
C 该实验流程中,残液中补充HCl的主要作用是抑制产物的水解。
D 反应装置中使用长导管的目的是防止三颈烧瓶内气压过大。
(5)氯化亚铜的定量分析:
①称取成品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0 mol·L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表。(已知:CuCl + FeCl3 = CuCl2 + FeCl2,Fe2+ + Ce4+ = Fe3+ + Ce3+)
④数据处理:计算得CuCl的纯度为__________ 。


实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36%盐酸15mL、水。
(1)请写出①的化学方程式
(2)本实验中通入O2的速率不宜过大,宜选择下图中的

(3)电炉加热升温至50℃时停止加热,反应快速进行,当烧瓶中液面上方的现象为
(4)关于该实验过程中,下列说法正确的是
A 实验开始时,温度计显示反应液温度可能低于室温。
B 流程中过滤操作,可以采用真空抽滤的方式,洗涤固体可以用95%的酒精。
C 该实验流程中,残液中补充HCl的主要作用是抑制产物的水解。
D 反应装置中使用长导管的目的是防止三颈烧瓶内气压过大。
(5)氯化亚铜的定量分析:
①称取成品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0 mol·L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表。(已知:CuCl + FeCl3 = CuCl2 + FeCl2,Fe2+ + Ce4+ = Fe3+ + Ce3+)
| 实验序号 | 1 | 2 | 3 |
| 滴定起始读数(mL) | 0.75 | 0.50 | 0.80 |
| 滴定终点读数(mL) | 24.70 | 24.95 | 24.85 |
您最近一年使用:0次
2019-08-10更新
|
853次组卷
|
3卷引用:专题13 实验题大题不丢分-2021年高考化学必做热点专题
名校
6 . 氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于H2SO4、HNO3和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)3Cl]。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

(1)写出溶解过程中发生的氧化还原反应的离子方程式:_________
(2)还原过程中发生的主要反应的离子方程式:_________ 。
(3)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2h,冷却密封包装。70℃真空干燥、密封包装的原因是__________ 。
(4)写出氯化亚铜在空气中被氧化的化学方程式________
(5)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65℃时,CuCl产率会下降,其原因可能是___ 。
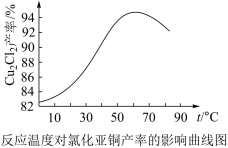
(6)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式:____

(1)写出溶解过程中发生的氧化还原反应的离子方程式:
(2)还原过程中发生的主要反应的离子方程式:
(3)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2h,冷却密封包装。70℃真空干燥、密封包装的原因是
(4)写出氯化亚铜在空气中被氧化的化学方程式
(5)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65℃时,CuCl产率会下降,其原因可能是

(6)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式:
您最近一年使用:0次
2019-06-12更新
|
1147次组卷
|
2卷引用:湖北省黄冈中学2019届高三6月适应性考试(最后一卷)理综化学试题
2019·全国·三模
7 . CuCl广泛用于颜料、电镀和有机合成等方面。已知:CuCl在干燥空气中稳定,受潮则易变蓝到棕色,露置在空气中迅速氧化成碱式盐,呈绿色,化学反应为:4CuCl+O2+2H2O=4Cu(OH)Cl。CuCl在水中水解:CuCl+H2O CuOH+HCl,2CuOH=Cu2O+H2O。工业上,常以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化法制备CuCl,其工艺流程如下:
CuOH+HCl,2CuOH=Cu2O+H2O。工业上,常以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化法制备CuCl,其工艺流程如下:
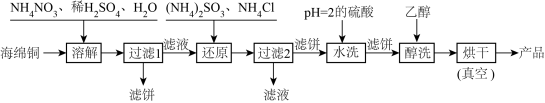
请回答下列问题:
(1)为了提高“溶解”速率,工业生产中宜采用的措施有____________ (答两条即可)。
(2)写出“溶解”过程中属于氧化还原反应的离子方程式:_________ 。
(3)“过滤2”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得一种化学肥料,它的主要成分是________ (填化学式)。写出“还原”过程中的化学方程式:_________ 。
(4)工业生产中,用pH=2的硫酸洗涤“产品”,其目的是_________ ;用乙醇洗涤的优点是________________ 。
(5)探究(NH4)2SO3、NH4Cl与Cu2+的相对用量和Cu2+沉淀率的关系如图1和图2所示。
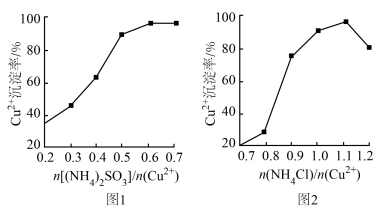
由实验表明,投料比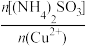 、
、 的最佳值分为
的最佳值分为______ 、_____ 。
(6)已知:现有x t工业海绵铜(铜元素的质量分数为w)经上述流程,最终得到y t CuCl产品。则CuCl的产率为____________ (用代数式表示)。
 CuOH+HCl,2CuOH=Cu2O+H2O。工业上,常以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化法制备CuCl,其工艺流程如下:
CuOH+HCl,2CuOH=Cu2O+H2O。工业上,常以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化法制备CuCl,其工艺流程如下:
请回答下列问题:
(1)为了提高“溶解”速率,工业生产中宜采用的措施有
(2)写出“溶解”过程中属于氧化还原反应的离子方程式:
(3)“过滤2”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得一种化学肥料,它的主要成分是
(4)工业生产中,用pH=2的硫酸洗涤“产品”,其目的是
(5)探究(NH4)2SO3、NH4Cl与Cu2+的相对用量和Cu2+沉淀率的关系如图1和图2所示。

由实验表明,投料比
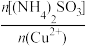 、
、 的最佳值分为
的最佳值分为(6)已知:现有x t工业海绵铜(铜元素的质量分数为w)经上述流程,最终得到y t CuCl产品。则CuCl的产率为
您最近一年使用:0次
名校
8 . 我国宋代沈括在《梦溪笔谈》中记载:信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾。熬胆矾铁釜,久之亦化为铜”。某化学兴趣小组为探究胆矾(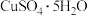 )的热分解产物,设计如图所示装置进行实验:
)的热分解产物,设计如图所示装置进行实验:

已知: 的熔点为16.8℃,沸点为46.8℃;
的熔点为16.8℃,沸点为46.8℃; 的熔点为-72℃,沸点为-10℃.
的熔点为-72℃,沸点为-10℃.
请回答下列问题:
(1)仪器a的名称是____ ,a中的棒香能复燃,说明热分解产物含有_____ (填化学式)。
(2)A中固体由蓝色变为黑色,B中的现象是____ 。
(3)C中冰水的作用是_____ 。
(4)D中品红溶液褪色,E中有 、
、 生成,写出E中生成
生成,写出E中生成 的总的离子方程式:
的总的离子方程式:____ 。
(5)若生成 和
和 的物质的量之比为1:1,则胆矾热分解的化学方程式为
的物质的量之比为1:1,则胆矾热分解的化学方程式为_____ 。
(6)小组同学用滴定法测定某胆矾样品中 的含量,取mg样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用0.1000mol/L的EDTA(
的含量,取mg样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用0.1000mol/L的EDTA(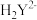 )标准溶液滴定至终点,平均消耗EDTA溶液VmL(滴定反应:
)标准溶液滴定至终点,平均消耗EDTA溶液VmL(滴定反应: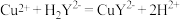 )。
)。
①样品中 的质量分数为
的质量分数为____ %(用含m、V的代数式表示)。
②下列操作会导致 含量的测定结果偏高的是
含量的测定结果偏高的是____ (填选项字母)。
a.未润洗锥形瓶
b.滴定终点时仰视读数
c.滴定终点时滴定管尖嘴中有气泡
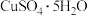 )的热分解产物,设计如图所示装置进行实验:
)的热分解产物,设计如图所示装置进行实验:
已知:
 的熔点为16.8℃,沸点为46.8℃;
的熔点为16.8℃,沸点为46.8℃; 的熔点为-72℃,沸点为-10℃.
的熔点为-72℃,沸点为-10℃.请回答下列问题:
(1)仪器a的名称是
(2)A中固体由蓝色变为黑色,B中的现象是
(3)C中冰水的作用是
(4)D中品红溶液褪色,E中有
 、
、 生成,写出E中生成
生成,写出E中生成 的总的离子方程式:
的总的离子方程式:(5)若生成
 和
和 的物质的量之比为1:1,则胆矾热分解的化学方程式为
的物质的量之比为1:1,则胆矾热分解的化学方程式为(6)小组同学用滴定法测定某胆矾样品中
 的含量,取mg样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用0.1000mol/L的EDTA(
的含量,取mg样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用0.1000mol/L的EDTA(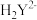 )标准溶液滴定至终点,平均消耗EDTA溶液VmL(滴定反应:
)标准溶液滴定至终点,平均消耗EDTA溶液VmL(滴定反应: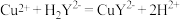 )。
)。①样品中
 的质量分数为
的质量分数为②下列操作会导致
 含量的测定结果偏高的是
含量的测定结果偏高的是a.未润洗锥形瓶
b.滴定终点时仰视读数
c.滴定终点时滴定管尖嘴中有气泡
您最近一年使用:0次
2019-04-26更新
|
773次组卷
|
3卷引用:山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题
山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)【市级联考】湖南省益阳市2019届高三下学期4月模考理科综合化学试题
9 . 2018年第十二届中国国际航空航天博览会于11月6日至11日在珠海举行。银铜合金广泛用于航空工业,从银铜合金的切割废料中回收银并制备铜化工产品的工艺如下:
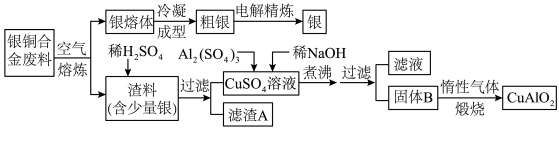
注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃。
(1)电解精炼银时,粗银作______ 极,另一电极上的电极反应式为____________ 。
(2)加快渣料(含少量银)溶于稀H2SO4的速率的措施有________ 、________ (写出两种)。
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为__________ 。
(4)煮沸CuSO4混合溶液的过程中,得到固体B,则固体B的组成为______ ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为___________ 。
(5)硫酸铜溶液可用于浸取硫铁矿中的铁元素,浸取时发生复杂的氧化还原反应。反应体系中除CuSO4和FeS2外,还有H2SO4、Cu2S、FeSO4和H2O,下列对该反应的分析正确的是______ (填字母代号)。
A.氧化剂为CuSO4和FeS2
B.反应后溶液的pH降低
C.被氧化的FeS2只占总量的30%
D.每转移2 mol电子消耗3 mol CuSO4

注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃。
(1)电解精炼银时,粗银作
(2)加快渣料(含少量银)溶于稀H2SO4的速率的措施有
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为
(4)煮沸CuSO4混合溶液的过程中,得到固体B,则固体B的组成为
(5)硫酸铜溶液可用于浸取硫铁矿中的铁元素,浸取时发生复杂的氧化还原反应。反应体系中除CuSO4和FeS2外,还有H2SO4、Cu2S、FeSO4和H2O,下列对该反应的分析正确的是
A.氧化剂为CuSO4和FeS2
B.反应后溶液的pH降低
C.被氧化的FeS2只占总量的30%
D.每转移2 mol电子消耗3 mol CuSO4
您最近一年使用:0次
10 . 氯化亚铜(CuCl)在生产中广泛用作催化剂、杀菌剂、脱色剂。某兴趣小组采用加热分解氯化铜晶体(CuCl2·xH2O)的方法制备CuCl,其装置如下(夹持仪器省略)。
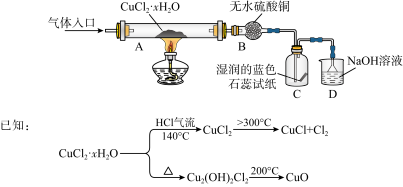
完成下列填空:
(1)在实验过程中,可以观察到C中试纸的颜色变化是___________________________ 。
(2)实验过程中需要全程通入干燥的HCl,其作用是___________________________ 。
(3)反应结束后,取出CuCl产品进行实验,发现其中含有少量的杂质,根据已知信息分析:
① 若杂质是CuCl2,则产生的原因可能是____________________________________ 。
② 若杂质是CuO,则产生的原因可能是_____________________________________ 。
(4)为测定原料CuCl2·xH2O中结晶水的数目x,可采取如下方案:
a.用电子天平称取一定质量氯化铜晶体 b.在______ (填仪器名称)中充分灼烧
c.在干燥器中冷却 d.称量所得黑色固体质量
e.重复b ~ d操作直至_____________________
① 完成上述实验操作步骤。
② 若氯化铜晶体质量为3.384 g,最终得到黑色固体质量为1.600 g,则x =________ (精确到0.1)。
③ 若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。____________________________

完成下列填空:
(1)在实验过程中,可以观察到C中试纸的颜色变化是
(2)实验过程中需要全程通入干燥的HCl,其作用是
(3)反应结束后,取出CuCl产品进行实验,发现其中含有少量的杂质,根据已知信息分析:
① 若杂质是CuCl2,则产生的原因可能是
② 若杂质是CuO,则产生的原因可能是
(4)为测定原料CuCl2·xH2O中结晶水的数目x,可采取如下方案:
a.用电子天平称取一定质量氯化铜晶体 b.在
c.在干燥器中冷却 d.称量所得黑色固体质量
e.重复b ~ d操作直至
① 完成上述实验操作步骤。
② 若氯化铜晶体质量为3.384 g,最终得到黑色固体质量为1.600 g,则x =
③ 若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。
您最近一年使用:0次
2019-04-17更新
|
386次组卷
|
3卷引用:【区级联考】上海市虹口区2019届高三下学期二模考试化学试题
【区级联考】上海市虹口区2019届高三下学期二模考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (练)-《2020年高考一轮复习讲练测》上海市上海师范大学附属中学2019-2020学年高三3月月考化学试题



